
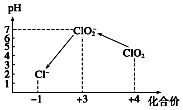
 ClO2��һ�ֻ���ɫ���Ȼ�ɫ�����壬ClO2��Cl2��������������������Ϲ���Ϊ��ȫ���Ͷ�����ɫ���������������ҹ���ClO2��������������ˮ����������
ClO2��һ�ֻ���ɫ���Ȼ�ɫ�����壬ClO2��Cl2��������������������Ϲ���Ϊ��ȫ���Ͷ�����ɫ���������������ҹ���ClO2��������������ˮ�������������� ��1��HCl�е���Ԫ���ڲ��������Cl2����Ԫ�صĻ��ϼ����ߣ���Ԫ�ر�����������NaCl����Ԫ�صĻ��ϼ�δ�仯��
��2��������Һ���ò��ᣨH2C2O4����ԭ�����ƣ�NaClO3��������������ԭ��Ӧ����ѭ���ӡ�����غ㣻
��3�������ʵ�����Ϊ1mol����ClO2��Cl2��ת��ΪCl-�õ����ӷֱ�Ϊ5mol��2mol��
��4���ٲ�������ClO2��KI����������ԭ��Ӧ��
�ڲ�������һ������Na2S2O3��Һ������2S2O32-+I2�TS4O62-+2I-����ɫ��ʧ��
��5��ClO2��CN-������ֻ�����������壬Ӧ���ɵ����������̼��ͬʱ���������ӣ�������ӷ�Ӧ���㣮
��� �⣺��1��2NaClO3+4HCl=2ClO2��+Cl2��+2H2O+2NaCl�������������ֻ�ԭ�ԡ�����NaCl�������ԣ��ʴ�Ϊ�����Ժͻ�ԭ�ԣ�
��2��������Һ���ò��ᣨH2C2O4����ԭ�����ƣ�NaClO3�������ӷ�ӦΪH2C2O4+2ClO3-+2H+=2CO2��+2ClO2��+2H2O����ѭ��ɡ������غ㣬
�ʴ�Ϊ��H2C2O4+2ClO3-+2H+=2CO2��+2ClO2��+2H2O��
��3�������ʵ�����Ϊ1mol����ClO2��Cl2��ת��ΪCl-�õ����ӷֱ�Ϊ5mol��2mol������ͬ���ʵ�����ClO2������Ч����Cl2��$\frac{5mol}{2mol}$=2.5�����ʴ�Ϊ��2.5��
��4���ٲ�������ClO2��KI����������ԭ��Ӧ�����ӷ�ӦΪ2ClO2+2I-�T2ClO2+I2���ʴ�Ϊ��2ClO2+2I-�T2ClO2+I2��
�ڲ�������һ������Na2S2O3��Һ������2S2O32-+I2�TS4O62-+2I-����ɫ��ʧ����ȷ����������ȫ��Ӧ����������ɫǡ����ʧ���ʴ�Ϊ����ɫǡ����ʧ��
��5��ClO2��CN-������ֻ�����������壬Ӧ���ɵ����������̼��ͬʱ���������ӣ����ӷ�ӦΪ2ClO2+2CN-=N2��+2CO2��+2Cl-��100m3��ˮ��CN-����=100m3��ag/m3=100ag��CN-�����ʵ���Ϊ$\frac{1000ag}{26g/mol}$=$\frac{50a}{13}$mol����2ClO2+2CN-=N2��+2CO2��+2Cl-��֪��������ҪClO2�����ʵ���Ϊ$\frac{50a}{13}$mol��
�ʴ�Ϊ��2ClO2+2CN-=N2��+2CO2��+2Cl-�� $\frac{50a}{13}$��
���� ���⿼�����ʺ����IJ�ã�Ϊ��Ƶ���㣬���շ�����������ԭ��Ӧ����Ӧ�ļ���Ϊ���Ĺؼ������ط�����Ӧ�������Ŀ��飬ע��������ԭ��Ӧ��Ӧ�ã���Ŀ�ѶȲ���


 ͨ��ѧ��Ĭд����ϵ�д�
ͨ��ѧ��Ĭд����ϵ�д� ���ƽ̸�������ѡ����ĩ���100��ϵ�д�
���ƽ̸�������ѡ����ĩ���100��ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | �٢ڢ� | B�� | �ڢۢ� | C�� | �ڢܢ� | D�� | �ڢ� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | Al3++3NH4++6OH-=Al��OH��3��+3NH3•H2O | |
| B�� | 2Al3++NH4++7OH-=2Al��OH��3��+NH3•H2O | |
| C�� | Al3++3NH4++7OH-=AlO2-+3NH3•H2O+2H2O | |
| D�� | Al3++5NH4++9OH-=AlO2-+5NH3•H2O+2H2O |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ��ɫ���� | B�� | ��Һ�� | C�� | ��������ˮ | D�� | �д̼�����ζ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
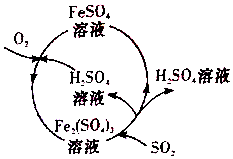 ����úȼ�ջ����������Ⱦ��Ϊ���θ���Ⱦ��ij����������µ����۷�����ͬʱ�ɵõ�������Ʒ���ù���������ͼ��ʾ��������������ȷ���ǣ�������
����úȼ�ջ����������Ⱦ��Ϊ���θ���Ⱦ��ij����������µ����۷�����ͬʱ�ɵõ�������Ʒ���ù���������ͼ��ʾ��������������ȷ���ǣ�������| A�� | �ù����пɵõ�������ƷH2SO4 | |
| B�� | �ù��������dz�ȥúȼ��ʱ������SO2 | |
| C�� | �ù����л��ϼ۷����ı��Ԫ��ΪFe��S | |
| D�� | ͼ���漰���ķ�Ӧ֮һΪFe2��SO4��3+SO2+2H2O�T2FeSO4+2H2SO4 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
 ��
�� ����Ŀ�ֱ���a��b��c��d��ʾ�����������������⣩�д��ڵĹ�ϵ�����ۣ�
����Ŀ�ֱ���a��b��c��d��ʾ�����������������⣩�д��ڵĹ�ϵ�����ۣ��鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� |  �μ�ҩƷ��ʹ�� | B�� |  �����ȵ������� | ||
| C�� | 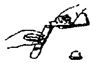 Һ��ҩƷ��ȡ�� | D�� | 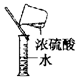 ϡ��Ũ���� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com