
【题目】某烯烃氢化后得到的饱和烃是 ![]() ,则原烯烃可能有的结构简式有( )
,则原烯烃可能有的结构简式有( )
A.1种
B.2种
C.3种
D.4种
 互动课堂系列答案
互动课堂系列答案 激活思维智能训练课时导学练系列答案
激活思维智能训练课时导学练系列答案科目:高中化学 来源: 题型:
【题目】配制100mL0.100mol/LNa2CO3溶液时,有下列步骤:①溶解②转移③定容④计算⑤称量⑥洗涤,正确的顺序为( )
A. ⑤④①⑥②③B. ⑤④②①⑥③
C. ④⑤①②⑥③D. ⑥④③⑤①②
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】实验室用少量的溴水和足量的乙醇制备1,2﹣二溴乙烷的装置如图所示: 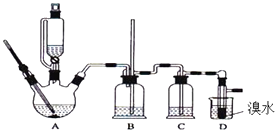
乙醇 | 1,2二溴乙烷 | 乙醚 | |
状态 | 无色液体 | 无色液体 | 无色液体 |
密度/gcm﹣3 | 0.79 | 2.2 | 0.71 |
沸点/℃ | 78.5 | 132 | 34.6 |
熔点/℃ | ﹣130 | 9 | ﹣116 |
请回答下列问题:
(1)写出制备1,2二溴乙烷的反应原理方程式:、
(2)在此制备实验中,要尽可能迅速地把反应温度升高到170℃左右,最主要的目的是(填序号).
a.引发反应 b.加快反应速度c.防止乙醇挥发 d.减少副产物乙醚生成
(3)装置B的作用是 .
(4)在装置C中应加入(填序号),其目的是吸收反应中可能生成的酸性气体.
a.水b.浓硫酸c.氢氧化钠溶液d.饱和碳酸氢钠溶液
(5)判断该制备反应已经结束的最简单方法是 .
(6)将1,2二溴乙烷粗产品置于分液漏斗中,加水振荡后静置,产物应在(填“上”或“下”)层.
(7)若产物中有少量副产物乙醚,可用的方法除去.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)实验室制取、净化并收集氯气涉及以下几个主要阶段:

现有以下3种试剂:A.饱和食盐水 B.NaOH溶液 C.浓硫酸
请在以上试剂中选择填空:
①X、Y溶液分别应选用______(填“A”、“B”或“C”)、
②尾气处理过程中,多余的氯气可用______(填“A”、“B”或“C”)吸收。
(2)某化学兴趣小组为了探究Cl2的相关性质,设计了如下的实验。

①写出Cl2与水反应的离子方程式______。
②通入Cl2后,从集气瓶A、B的现象可得出的结论是______。
(3)如图所示,上述实验过程中,不会产生气体的是______,写出反应A的化学方程式______。

(4)碘是人体中不可缺少的微量元素,碘缺乏病是目前已知的导致人类智力障碍的主要原因,我国在食盐中加入碘元素能有效防止缺碘引起的疾病。

某同学采用萃取-分液的方法从碘水中提取碘,主要操作步骤如下图:
甲.加入萃取剂后振荡乙.静置分层丙.分离
①该同学所采用的萃取剂可能是______(填“A”、“B”或“C”)。
A.酒精 B.苯C.四氯化碳
②甲、乙、丙3步实验操作中,不正确的是______(填“甲”、“乙”或“丙”)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】随着学技术的发展和环保要求的不断提高,CO2的捕集利用技术成为研究的重点.完成下列填空:
(1)目前国际空间站处理CO2的一个重要方法是将CO2还原,所涉及的反应方程式为:
CO2(g)+4H2(g) ![]() CH4(g)+2H2O(g)
CH4(g)+2H2O(g)
已知H2的体积分数随温度的升高而增加.若温度从300℃升至400℃,重新达到平衡,判断下列表格中各物理量的变化.(填“增大”、“减小”或“不变”)
v正 | v逆 | 平衡常数K | 转化率α |
(2)相同温度时,上述反应在不同起始浓度下分别达到平衡,各物质的平衡浓度如表:
[CO2]/molL﹣1 | [H2]/molL﹣1 | [CH4]/molL﹣1 | [H2O]/molL﹣1 | |
平衡Ⅰ | a | b | c | d |
平衡Ⅱ | m | n | x | y |
a、b、c、d与m、n、x、y之间的关系式为 .
(3)碳酸:H2CO3 , Ki1=4.3×10﹣7 , Ki2=5.6×10﹣11
草酸:H2C2O4 , Ki1=5.9×10﹣2 , Ki2=6.4×10﹣5 0.1mol/L Na2CO3溶液的pH0.1mol/L Na2C2O4溶液的pH.(选填“大于”“小于”或“等于”)
等浓度草酸溶液和碳酸溶液中,氢离子浓度较大的是 .
若将等浓度的草酸溶液和碳酸溶液等体积混合,溶液中各种离子浓度大小的顺序正确的是 . (选填编号)
a.[H+]>[HC2O4﹣]>[HCO3﹣]>[CO32﹣]b.[HCO3﹣]>[HC2O4﹣]>[C2O42﹣]>[CO32﹣]
c.[H+]>[HC2O4﹣]>[C2O42﹣]>[CO32﹣]d.[H2CO3]>[HCO3﹣]>[HC2O4﹣]>[CO32﹣].
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有机物分子中与“O﹣C﹣”相连的碳原子上的氢活性较大,可以与甲醛或卤代烃等发生反应.已知:
有机物J是重要的工业原料,其合成路线如下(部分产物和反应条件略):
(1)A中所含官能团的名称是 .
(2)A→B的反应类型是反应.
(3)G俗称缩苹果酸,与B以物质的量之比1:2反应,则G+B→H的化学方程式是 .
(4)J的同分异构体X属于芳香族化合物,1mol X与足量Na或NaOH反应时的物质的量之比分别是1:4和1:1,且苯环上只有一种一氯代物.符合上述条件的X有种,写出其中任意一种的结构简式: .
(5)已知E中只有一种官能团,且核磁共振氢谱显示其分子中有两种不同化学环境的氢.则下列说法正确的是(填序号);E的分子式是 . a.E与B互为同系物
b.E中含有的官能团是羟基
c.F在一定条件下也可转化为E
d.F中也有两种不同化学环境的氢
(6)J的结构简式是 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】吸烟是人类的一种不良嗜好,也是生活环境中的特殊大气污染源,它对人体健康危害极大,据分析吸烟生成的物质至少有700多种,其中大部分为有毒有害物质.危害最大的物质中有两种是尼古丁和苯并芘,前者的成人致死量约为40~60mg,相当于一包香烟产生的尼古丁的总量;后者是最强的致癌物之一.它们的结构简式分别为: 下列有关尼古丁或苯并芘的叙述正确的是( )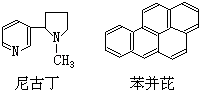
A.尼古丁的分子式为C10H14N2
B.尼古丁分子中的所有原子都在同一平面上
C.苯并芘的分子式为C20H18
D.苯并芘分子中含有苯环结构单元,是苯的同系物
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有一包铁粉和铜粉混合均匀的粉末样品,为确定其组成,某同学将不同质量的该样品分别与40 mL 1 mol/L的FeCl3溶液反应,实验结果如下表所示(忽略反应前后溶液体积的微小变化)。
实验序号 | ① | ② | ③ | ④ |
m(粉末样品)/g | 0.90 | 1.80 | 3.60 | 7.20 |
m(反应后剩余固体)/g | 0 | 0.64 | 2.48 | 6.08 |
下列实验结论不正确的是
A. 实验②反应后溶液中含有Fe2+、Cu2+ B. 实验②③④反应后剩余固体全部是Cu
C. 实验④的滤液中c(Fe2+)=1.5 mol/L D. 原粉末样品中n(Fe)∶n(Cu)=1∶1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某学习小组做电浮选凝聚法净化污水的实验时,同学们发表了如下看法,其中错误的是( )
A.两个电极都可选用Fe片
B.电源电极接反时仍能产生一定净水效果
C.反应中产生的H2会将Fe3+还原成Fe2+
D.电浮选凝聚法用于工业污水处理时要注意通风,防止爆炸
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com