
A、 |
B、 |
C、 |
D、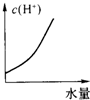 |


 浙大优学小学年级衔接导与练浙江大学出版社系列答案
浙大优学小学年级衔接导与练浙江大学出版社系列答案 小学暑假作业东南大学出版社系列答案
小学暑假作业东南大学出版社系列答案 津桥教育暑假拔高衔接广东人民出版社系列答案
津桥教育暑假拔高衔接广东人民出版社系列答案 波波熊暑假作业江西人民出版社系列答案
波波熊暑假作业江西人民出版社系列答案科目:高中化学 来源: 题型:
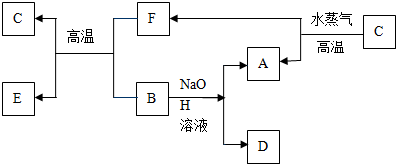
查看答案和解析>>
科目:高中化学 来源: 题型:
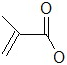 分子式
分子式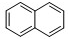 联苯:
联苯: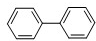 它们的分子式分别为
它们的分子式分别为查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、在标准状况下,1mol水的体积是22.4L |
| B、1mol H2所占的体积约为22.4L |
| C、3.01×1023个SO2分子的质量为32 |
| D、在标准状况下,1mol NH3和CO混合气体所占的体积约为22.4L |
查看答案和解析>>
科目:高中化学 来源: 题型:
| ||
| ||
| A、①、②两反应都是放热反应 |
| B、相同物质的量的H2、Cl2反应,①、②反应放出的热量一样多 |
| C、相同物质的量的H2、Cl2反应,①、②反应放出的热量不一样多 |
| D、①、②的能量转化方式主要是化学能转化为热能 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、为除去苯中的少量苯酚,向混合物中加入适量的溴水后过滤 |
| B、制备乙酸乙酯时,向乙醇中缓慢加入浓硫酸和冰醋酸 |
| C、用粥汤检验加碘盐中是否含碘 |
| D、在苯萃取溴水中的溴,分液时有机层从分液漏斗的下端放出 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、NH4HCO3和醋酸溶液不能发生反应 |
| B、0.1mol NH4HCO3粉末中NH4+和HCO3-总数小于1.204×1023 |
| C、醋酸凝固时释放的能量储存于NH4Cl、CO2和H2O中 |
| D、如果改加体积和pH值均与盐酸相同的稀硫酸,可能不会发生上述现象 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com