
| A、元素周期表中位于金属和非金属非界线附近的元素属于过渡元素 |
| B、短周期元素中,元素符号用一个大写英文字母表示的元素共有7种 |
| C、第三周期元素的最高正化合价等于它所处的主族序数 |
| D、共价化合物中各原子都一定满足最外层8电子稳定结构 |


 春雨教育同步作文系列答案
春雨教育同步作文系列答案科目:高中化学 来源: 题型:
 “酒是陈的香”,就是因为酒在储存过程中生成了有香味的乙酸乙酯,在实验室我们也可以用右图所示的装置制取乙酸乙酯.回答下列问题:
“酒是陈的香”,就是因为酒在储存过程中生成了有香味的乙酸乙酯,在实验室我们也可以用右图所示的装置制取乙酸乙酯.回答下列问题:查看答案和解析>>
科目:高中化学 来源: 题型:
| A、铝土矿溶于NaOH溶液中 |
| B、NaAlO2溶液的酸化 |
| C、灼烧氢氧化铝固体 |
| D、电解熔融的氧化铝 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| 步骤 | 操作 | 实验现象 | 结论 |
| ① | 取固体溶于水,得溶液X 加入几滴KSCN溶液 | 溶液X呈黄色,后呈现红色 | X含有 |
| ② | 取少量溶液X,加入氯化 钡溶液至不再生成沉淀,静置 | 上层溶液为黄色 生成白色沉淀 | X可能含有 |
| ③ | 取②中生成白色沉淀,加入稀盐酸 | 沉淀不溶解 | |
| ④ | 取②中上层溶液,加入硝酸银溶液 | 生成白色沉淀 | X含有Cl- |
| 结论:此白色固体可能是 | |||
查看答案和解析>>
科目:高中化学 来源: 题型:
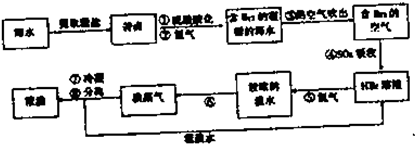
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、x=1 |
| B、达到平衡时,在相同温度下容器内混合气体的压强是反应前的8.5倍 |
| C、平衡时A的浓度为1.50?L-1 |
| D、B的转化率为20% |
查看答案和解析>>
科目:高中化学 来源: 题型:
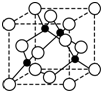 A、B、C、D、E、F均为周期表中前四周期元素,其原子序数依次增大,其中A、B、C为短周期非金属元素.A是形成化合物种类最多的元素;B原子基态电子排布中只有一个未成对电子;C是同周期元素中原子半径最小的元素,且B、C同主族.D的基态原子在前四周期元素的基态原子中单电子数最多;E 与D相邻,E的某种氧化物X与C的氢化物的浓溶液加热时反应常用于实验室制取气态单质C;F与D的最外层电子数相等.
A、B、C、D、E、F均为周期表中前四周期元素,其原子序数依次增大,其中A、B、C为短周期非金属元素.A是形成化合物种类最多的元素;B原子基态电子排布中只有一个未成对电子;C是同周期元素中原子半径最小的元素,且B、C同主族.D的基态原子在前四周期元素的基态原子中单电子数最多;E 与D相邻,E的某种氧化物X与C的氢化物的浓溶液加热时反应常用于实验室制取气态单质C;F与D的最外层电子数相等.查看答案和解析>>
科目:高中化学 来源: 题型:
| A、己烯、甲苯、苯酚溶液 |
| B、己烷、苯、四氯化碳 |
| C、庚烷、1-庚烯、1,2-二溴乙烷 |
| D、苯、酒精、硝基苯 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com