
| A. | 不是在室温下 | B. | 弱酸溶液与强碱溶液反应 | ||
| C. | 强酸溶液与强碱溶液反应 | D. | 二元强酸溶液和一元强碱溶液反应 |
分析 pH=3的酸和pH=11的碱溶液等体积混合,混合溶液呈酸性,可能是酸为弱酸、碱为强碱,混合后酸后剩余;也可能是酸、碱都是弱电解质,但酸的电离程度小于碱的电离程度,据此分析解答.
解答 解:若将pH=3的酸溶液和pH=11的碱溶液等体积混合后溶液呈酸性,可能是酸为弱酸、碱为强碱,混合后酸后剩余;也可能是酸、碱都是弱电解质,但酸的电离程度小于碱的电离程度,
A.若温度高于常温,则若pH=3的酸溶液和pH=11的碱溶液等体积混合,氢氧根离子过量,溶液不可能先酸性,故A错误;
B.如果酸是弱酸、碱为强碱,二者混合后酸有剩余,酸的电离程度大于其酸根离子水解程度而导致溶液呈酸性,故B正确;
C.如果是一元强酸和一元强碱混合,二者物质的量相等,二者恰好反应生成强酸强碱盐,其溶液呈中性,与题意不符,故C错误;
D.如果是二元强酸和一元强碱混合,氢离子与氢氧根离子恰好反应生成强酸强碱盐,其溶液呈中性,与题意不符,故D错误;
故选B.
点评 本题考查酸碱混合溶液定性判断,正确理解题给信息是解本题关键,根据混合溶液酸碱性判断酸、碱强弱,题目难度不大,侧重于考查学生的分析能力和对基础知识的应用能力.


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:实验题
 甲醇是重要的化工原料,又可称为燃料.工业上利用合成气(主要成分为CO、CO2和H2)在催化剂的作用下合成甲醇,发生的主要反应如下:
甲醇是重要的化工原料,又可称为燃料.工业上利用合成气(主要成分为CO、CO2和H2)在催化剂的作用下合成甲醇,发生的主要反应如下:| 化学键 | H═H | C═O | C≡O | H-O | C-H |
| F/(kJ•mol-1) | 435 | 343 | 1076 | 465 | X |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 用A表示的反应速率是0.4 mol•L-1•min-1 | |
| B. | 分别用B、C、D表示的反应速率之比是3:2:1 | |
| C. | 在2 min末的反应速率,用B表示是0.3 mol•L-1•min-1 | |
| D. | 在2 min内的反应速率,用C表示是0.3 mol•L-1•min-1 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 1 L水中溶解了40 g NaOH后,所得溶液浓度为1 mol/L | |
| B. | 从1 L 2 mol/L的NaCl溶液中取出0.5 L,该溶液的浓度为1 mol/L | |
| C. | 将2.24 L(标准状况)HCl气体溶于水制成100 mL溶液,其物质的量浓度为1 mol/L | |
| D. | 配制1 L 0.2 mol/L的CuSO4溶液,需用32g胆矾 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 醋酸与水能以任意比互溶 | B. | 醋酸溶液能导电 | ||
| C. | 醋酸溶液中存在醋酸分子 | D. | 醋酸能和碳酸钙反应放出CO2 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
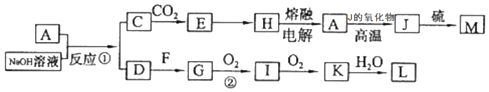
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 .
.查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
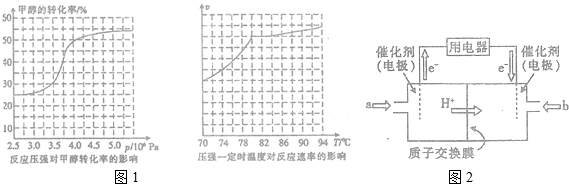
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com