
分析 (1)①Fe(s)+$\frac{1}{2}$O2(g)═FeO(s)△H1=-272.0kJ•mol-1;
②2Al(s)+$\frac{3}{2}$O2(g)═Al2O3(s)△H2=-1 675.7kJ•mol-1;
依据盖斯定律计算②-①×3得到;
(2)甲醇和氢气的燃烧热书写其热化学方程式分别为:
①2CH3OH(l)+3O2(g)=2CO2(g)+4H2O(l)△H1=-1451kJ/mol;
②2H2(g)+O2(g)=2H2O(l)△H2=-571.6KJ/mol,
根据盖斯定律,$\frac{3}{2}$②-$\frac{1}{2}$①得到;
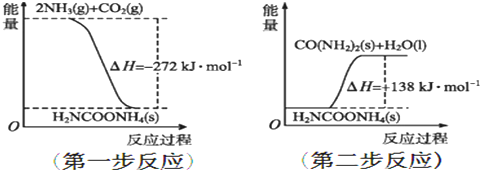
(3)第一步:2NH3(g)+CO2(g)?H2NCOONH4(l,氨基甲酸铵)△H1=-272KJ/mol,
第二步:H2NCOONH4(l)?H2O(l)+H2NCONH2(s)△H2=+138KJ/mol,
根据盖斯定律,两个过程相加得到NH3(g)与CO2(g)反应生成尿素的热化学方程式为2NH3(g)+CO2(g)?H2O(l)+H2NCONH2(s)△H=-134kJ•mol-1.
解答 解:(1)①Fe(s)+$\frac{1}{2}$O2(g)═FeO(s)△H1=-272.0kJ•mol-1;
②2Al(s)+$\frac{3}{2}$O2(g)═Al2O3(s)△H2=-1 675.7kJ•mol-1;
依据盖斯定律计算②-①×3得到:3FeO(s)+2Al(s)=Al2O3(s)+3Fe(s)△H=-859.7KJ/mol;
故答案为:3FeO(s)+2Al(s)=Al2O3(s)+3Fe(s)△H=-859.7KJ/mol;
(2)甲醇和氢气的燃烧热书写其热化学方程式分别为:
①2CH3OH(l)+3O2(g)=2CO2(g)+4H2O(l)△H1=-1451kJ/mol;
②2H2(g)+O2(g)=2H2O(l)△H2=-571.6KJ/mol,
根据盖斯定律,$\frac{3}{2}$②-$\frac{1}{2}$①得反应CO2(g)+3H2(g)═CH3OH(l)+H2O(l),所以△H=$\frac{3}{2}$×(-571.6KJ/mol)-$\frac{1}{2}$×(-1451kJ/mol)=-131.9KJ/mol,
故答案为:CO2(g)+3H2(g)═CH3OH(l)+H2O(l)△H=-131.9KJ/mol;
(3)第一步:2NH3(g)+CO2(g)?H2NCOONH4(l,氨基甲酸铵)△H1=-272KJ/mol,
第二步:H2NCOONH4(l)?H2O(l)+H2NCONH2(s)△H2=+138KJ/mol,
根据盖斯定律,两个过程相加得到NH3(g)与CO2(g)反应生成尿素的热化学方程式为2NH3(g)+CO2(g)?H2O(l)+H2NCONH2(s)△H=-134kJ•mol-1;
故答案为:2NH3(g)+CO2(g)?H2O(l)+H2NCONH2(s)△H=-134kJ•mol-1.
点评 本题考查了据图书写热化学方程式以及盖斯定律的应用,题目难度中等.


 黄冈天天练口算题卡系列答案
黄冈天天练口算题卡系列答案科目:高中化学 来源: 题型:选择题
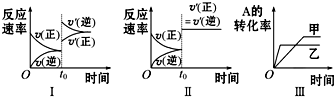
| A. | 图Ⅰ可体现t0时升高温度对反应速率的影响 | |
| B. | 图Ⅱ可体现t0时增大压强(缩小体积)或使用催化剂对反应速率的影响 | |
| C. | 图Ⅲ可体现催化剂对化学平衡的影响,且甲使用了催化剂 | |
| D. | 图Ⅲ可体现温度对化学平衡的影响,且乙的温度较高 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
 纳米级二氧化锰的活性很高,以二氧化锰为电极构成的燃料电池如图所示.下列说法不正确的是 ( )
纳米级二氧化锰的活性很高,以二氧化锰为电极构成的燃料电池如图所示.下列说法不正确的是 ( )| A. | a极为正极,发生还原反应 | |
| B. | b极的电极反应式为(CH2O)n-4ne-+n H2O=nCO2+4n H+ | |
| C. | 电子由b极流出经用电器流向a极 | |
| D. | 放电时H+由质子交换膜左侧向右侧迁移 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 甲烷的燃烧热为890.3 kJ•mol-1,则甲烷燃烧热的热化学方程式可表示为CH4(g)+2O2(g)═CO2(g)+2H2O(g)△H=-890.3 kJ•mol-1 | |
| B. | 500℃、30 MPa下,将0.5 mol N2和1.5 mol H2置于密闭容器中充分反应生成NH3(g),放热19.3 kJ,其热化学方程式为N2(g)+3H2(g)$?_{30MP}^{500℃}$ 2NH3(g)△H=-38.6 kJ•mol-1 | |
| C. | 已知在120℃、101 kPa下,1 g H2燃烧生成水蒸气放出121 kJ热量,其热化学方程式为H2(g)+$\frac{1}{2}$O2(g)═H2O(g)△H=-242 kJ•mol-1 | |
| D. | 25℃、101 kPa时,强酸与强碱的稀溶液发生中和反应的中和热为57.3 kJ•mol-1,硫酸溶液与氢氧化钾溶液反应的热化学方程式为H2SO4(aq)+2KOH(aq)═K2SO4(aq)+2H2O(l)△H=-57.3 kJ•mol-1 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 已知2H2(g)+O2(g)=2H2O(g)△H=-483.6 kJ•mol-1则氢气的燃烧热为241.8 kJ•mol-1 | |
| B. | 已知C(石墨,s)=C(金刚石,s)△H>0 则金刚石比石墨的键能大 | |
| C. | 已知NaOH(ag)+HCl(aq)=NaCl(aq)+H2O(l)△H=-57.4 kJ•mol-1则含20.0g NaOH的稀溶液与稀盐酸完全中和,放出28.7kJ的热量 | |
| D. | 已知2C(s)+2O2(g)=2CO2(g)△H1 2C(s)+O2(g)=2CO(g)△H2,则△H1>△H2 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 1.12L | B. | 2.24L | C. | 3.36L | D. | 4.48L |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com