
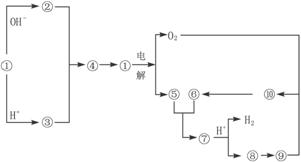
(1)①的化学式为_______,⑤和⑥反应的化学方程式为_______________________________。
(2)实验室由⑧制取⑨的离子方程式为_________,⑨转变为⑩的化学方程式为_________。由⑨转变为⑩的反应现象为___________________。
科目:高中化学 来源: 题型:



| ||
| ||
查看答案和解析>>
科目:高中化学 来源: 题型:
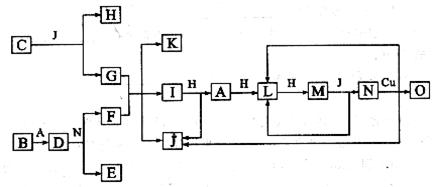
已知A-O分别代表一种物质,它们之间的转化关系如下图所示(反应条件略去)。A、B、H分别是由短周期元素组成的单质。B与冷水缓慢反应,与沸水迅速反应,放出氢气。D是一种离子化合物,其阴阳离子的个数比为2:3,且能与水反就应得到两种碱。C为淡黄色固体化合物,O能与G的水溶液反应生成蓝色沉淀。
![]()
![]() 请回答下列问题:
请回答下列问题:
![]() 组成B单质的元素位于周期表第______________周期,第_______________族。化合物C的电子式为__________________________________。
组成B单质的元素位于周期表第______________周期,第_______________族。化合物C的电子式为__________________________________。
![]() J的沸点比硒化氢(H2Se)的沸点高,其原因是_________________。
J的沸点比硒化氢(H2Se)的沸点高,其原因是_________________。
![]() 写出I与H在点燃条件下反应生成A和J的化学方程式:________________。
写出I与H在点燃条件下反应生成A和J的化学方程式:________________。
![]() 写出D与足量的N反应生成E和F的化学方程式:_____________________。
写出D与足量的N反应生成E和F的化学方程式:_____________________。
![]() 上图中,在同一反应里一种物质作氧化剂,又作还原剂,这样的反应共有_______个。
上图中,在同一反应里一种物质作氧化剂,又作还原剂,这样的反应共有_______个。
查看答案和解析>>
科目:高中化学 来源:2011-2012学年四川省高三3月月考理综部分(解析版) 题型:填空题
(12分)已知A-O分别代表一种物质,它们之间的转化关系如下图所示(反应条件略去)。A、B、H分别是由短周期元素组成的单质。B与冷水缓慢反应,与沸水迅速反应,放出氢气。D是一种离子化合物,其阴阳离子的个数比为2:3,且能与水反就应得到两种碱。C为淡黄色固体化合物,O能与G的水溶液反应生成蓝色沉淀。
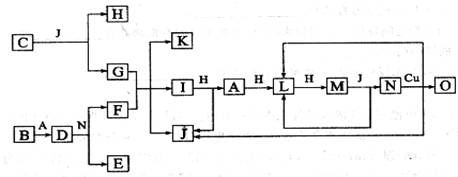
请回答下列问题:
(1)组成B单质的元素在周期表中的位置为______________,化合物C的电子式为_________________。
(2)J的沸点比硒化氢(H2Se)的沸点高,其原因是_________________。
(3)写出I与H在点燃条件下反应生成A和J的化学方程式:________________。
(4)写出D与足量的N反应生成E和F的化学方程式:_____________________。
(5)上图中,在同一反应里一种物质作氧化剂,又作还原剂,这样的反应共有______个。
查看答案和解析>>
科目:高中化学 来源:2010-2011学年新疆乌鲁木齐高三上学期第三次月考化学试卷 题型:填空题
已知A-O分别代表一种物质,它们之间的转化关系如下图所示(反应条件略去)。
A. B.H分别是由短周期元素组成的单质。B与冷水缓慢反应,与沸水迅速反应,放出氢气。D是一种离子化合物,其阴阳离子的个数比为2:3,且能与水反就应得到两种碱。C为淡黄色固体化合物,O能与G的水溶液反应生成蓝色沉淀。
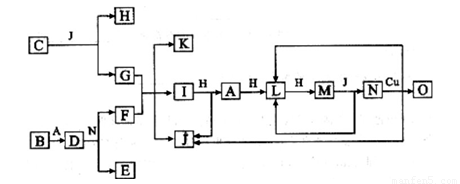
请回答下列问题:
(1)组成B单质的元素位于周期表第___周期,第____族。化合物C的电子式为______。
(2)通常情况下J为液体,用电子式表示其形成过程为_________________。
(3)写出I与H在点燃条件下反应生成A和J的化学方程式:________________。
(4)写出D与足量的N反应生成E和F的化学方程式:_____________________。
查看答案和解析>>
科目:高中化学 来源:2009年高考真题汇编-氮族元素 题型:填空题
已知A—O分别代表一种物质,它们之间的转化关系如下图所示(反应条件略)。A、B、H分别是由短周期元素组成的单质。B与冷水缓慢反应,与沸水迅速反应,放出氢气。D是一种离子化合物,其阴阳离子的个数比为2:3,且能与水反就应得到两种碱。C为淡黄色固体化合物,O能与G的水溶液反应生成蓝色沉淀。请回答下列问题:
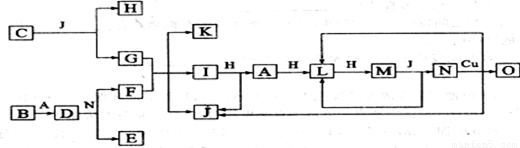
⑴组成B单质的元素位于周期表位置________________。化合物C电子式为____________。
⑵J的沸点比硒化氢(H2Se)的熔沸点高,其原因是_________________。
⑶I与H在一定条件下也可直接反应生成L和J, 写出化学方程式:_______________。
⑷写出D与水反应的化学方程式:_____________________。
⑸红棕色污染气体M的处理具有实际意义。现在常利用反应
M + NH3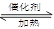 N2+H2O(方程没配平)来处理M。当转移0.4mol电子时,消耗的M在标准状况下是
L。
N2+H2O(方程没配平)来处理M。当转移0.4mol电子时,消耗的M在标准状况下是
L。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com