
【题目】设NA为阿伏加德罗常数的值,下列说法正确的是
A. 1L0.lmol·L-1的氢氧化钾溶液中O—H键的数目为0.1NA
B. 0.5mol·L-1的碳酸钠溶液中CO32-的数目小于0.5NA
C. 4.6g金属钠与500mL0.2 mol·L-1稀盐酸充分反应,转移电子数为0.1 NA
D. 标准状况下,2.24L乙烯和甲烷混合气体中含有的氢原子数目为0.4 NA
 学练快车道快乐假期寒假作业系列答案
学练快车道快乐假期寒假作业系列答案 新思维寒假作业系列答案
新思维寒假作业系列答案科目:高中化学 来源: 题型:
【题目】信息时代产生的大量电子垃圾对环境构成了极大的威胁。某“变废为宝”学生探究小组将一批废弃的线路板简单处理后,得到含 70% Cu、25% Al、4% Fe 及少量 Au、Pt 的合金,并设计出由合金制备硫酸铜和硫酸铝晶体的路线:

请回答下列问题:
(1)第①步Fe与过量的浓 HNO3 反应的离子方程式为_________,得到滤渣 1 的主要成分为__________。
(2)第②步加H2O2的作用是做氧化剂,将溶液中的 Fe2+氧化为Fe3+,用H2O2 做氧化剂的优点是______。
(3)滤渣 2 的主要成分是 Al(OH)3 和 Fe(OH)3,在生产中利用何种化学原理分离两种沉淀,写出反应的离子方程式_______。
(4)第③步蒸发所需玻璃仪器为________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有机物X、Y、Z的结构简式如下表所示。下列说法正确的是
X | Y | Z | |
结构简式 |
|
|
|
A. X的分子式为C8H7O3
B. X、Y、Z均可以和FeCl3发生显色反应
C. X、Y互为同系物,X、Z互为同分异构体
D. X、Y、Z在一定条件下都能发生取代反应、加成反应和氧化反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列各组溶液混合时,相互滴加的次序不同,现象也不同的是( )
A.氢氧化钠溶液与氯化铝溶液B.氢氧化钠溶液与盐酸
C.碳酸氢钠溶液与盐酸D.氢氧化钠溶液与氯化铁溶液
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一定温度下,0.1mol N2和0.3molH2在恒容的密闭容器中发生如下反应:N2(g)+3H2(g) ![]() 2NH3(g) △H<0下列说法不正确的是
2NH3(g) △H<0下列说法不正确的是
A. 达到平衡状态时,v正(NH3): v逆(N2)=2 : 1
B. c(N2):c(H2):c(NH3)=1:3:2时,说明反应已达到平衡状态
C. 容器内的压强不再变化时,说明反应已达到平衡状态
D. 升高温度时,v正(NH3)增大,v逆(NH3)增大
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】几种物质的能量关系如下图所示。下列说法正确的是
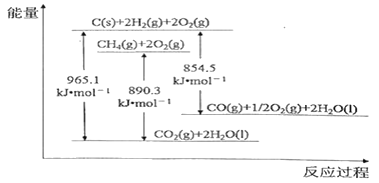
A. C(s)+O2(g)=CO2(g) △H =—965.1 kJ·mol-1
B. 2CO(g)+O2(g)=2CO2(g) △H =-221.2 kJ·mol-1
C. 由图可知,甲烷的燃烧热为779.7 kJ·mol-1
D. 通常由元素最稳定的单质生成生成1mol纯化合物时的反应热称为该化合物的标准生成焓,由图可知,CH4(g)的标准生成焓为+74.8 kJ·mol-1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】三室式电渗析法处理含Na2SO4废水的原理如图所示,采用惰性电极,ab、cd均为离子交换膜,在直流电场的作用下,两膜中间的Na+和SO42-可通过离子交换膜,而两端隔室中离子被阻挡不能进入中间隔室。下列叙述正确的是

A. 通电后中间隔室的SO42-离子向正极迁移,正极区溶液pH增大
B. 该法在处理含Na2SO4废水时可以得到NaOH和H2SO4产品
C. 负极反应为2H2O–4e–=O2+4H+,负极区溶液pH降低
D. 当电路中通过1mol电子的电量时,会有0.5mol的O2生成
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】工业废水中常含有一定量的Cr2O72—和CrO42—,它们会对人类及生态系统产生很大的伤害,必须进行处理。常用的处理方法有两种。
方法1:还原沉淀法
该法的工艺流程为
![]()
其中第①步存在平衡:2CrO42—(黄色)+2H+![]() Cr2O72—(橙色)+H2O
Cr2O72—(橙色)+H2O
(1)若平衡体系的pH=2,则溶液显 色.
(2)能说明第①步反应达平衡状态的是 。
a.Cr2O72—和CrO42—的浓度相同 b.2v (Cr2O72—) ="v" (CrO42—) c.溶液的颜色不变
(3)第②步中,还原1mol Cr2O72—离子,需要________mol的FeSO4·7H2O。
( 4 ) 第③步生成的Cr(OH)3在溶液中存在以下沉淀溶解平衡:
Cr(OH)3(s)![]() Cr3+(aq)+3OH—(aq)
Cr3+(aq)+3OH—(aq)
常温下,Cr(OH)3的溶度积Ksp=c(Cr3+)·c3(OH—)=10-32,要使c(Cr3+)降至10-5mol/L,溶液的pH应调至 。
方法2:电解法
该法用Fe做电极电解含Cr2O72—的酸性废水,随着电解进行,在阴极附近溶液pH升高,产生Cr(OH)3沉淀。
(5)用Fe做电极的原因为 。
(6)在阴极附近溶液pH升高的原因是(用电极反应解释) 。
溶液中同时生成的沉淀还有 。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有4种碳骨架如图所示的烃,下列说法正确的是
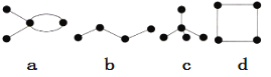
A. a和b互为同分异构体B. b和c互为同系物
C. a和b都能发生加成反应D. 只有b和c能发生取代反应
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com