
| A. | 1:3 | B. | 1:2 | C. | 2:1 | D. | 3:1 |
分析 钠和稀硫酸、水都反应,镁与稀硫酸发生Mg+H2SO4=MgSO4+H2↑,n(H2SO4)=0.1L×1mol/L=0.1mol,则Mg与硫酸恰好反应,以此计算.
解答 解:钠和稀硫酸、水都反应,则Na一定完全反应,由电子守恒可知,Na反应生成的氢气为$\frac{0.1mol×(1-0)}{2×(1-0)}$=0.05mol,
镁与稀硫酸发生Mg+H2SO4=MgSO4+H2↑,n(H2SO4)=0.1L×1mol/L=0.1mol,则Mg与硫酸恰好反应,由反应可知生成氢气为0.1mol,
同温同压下产生的气体体积比等于物质的量比,为0.05mol:0.1mol=1:2,
故选B.
点评 本题考查化学反应方程式的计算,为高频考点,把握发生的反应及过量判断、电子守恒等为解答的关键,侧重分析与计算能力的考查,题目难度不大.


科目:高中化学 来源: 题型:解答题

查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 反应速率:两者相同 | B. | 消耗的n(HNO3):后者少 | ||
| C. | 气体颜色:前者浅 | D. | 转移电子总数:前者多 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | NaNO2既具有氧化性又具有还原性 | |
| B. | 1 mol NaNO2在酸性条件下完全反应生成NO和NO2,转移电子的物质的量为1 mol | |
| C. | NaNO2和胃酸作用的离子方程式为:2NO${\;}_{2}^{-}$+2H+=NO↑+NO2↑+H2O | |
| D. | 食用“醋溜豆芽”可能会减少亚硝酸钠对人体的危害 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | O2、S、Br2 | B. | CH4、SiH4、GeH4 | C. | Li、Na、K | D. | H2O、H2S、H2Se |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 选项 | 离子组 | 条件 |
| A | K+、Na+、Cu2+、Cl- | 溶液呈无色 |
| B | Na+、Fe3+、NO3-、SO42- | 滴入酸性KMnO4溶液,溶液褪色 |
| C | Al3+、SO42-、Cl-、H+ | 加入氨水产生白色沉淀后沉淀溶解 |
| D | Na+、NO3-、I-、SO42- | 加入盐酸和淀粉溶液变蓝 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
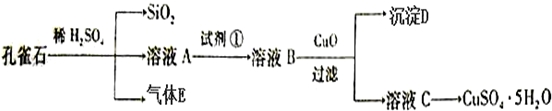
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com