
| A、标准状况下11.2L NO和11.2L O2混合后所得气体分子数为NA |
| B、7.1g Cl2与足量的NaOH溶液反应转移的电子数为0.2NA |
| C、25℃、1.01×105Pa时,80g SO3中含有的原子数为4NA |
| D、NA个CO分子和0.5mol CH4的质量比为7:4 |


 一线名师提优试卷系列答案
一线名师提优试卷系列答案 阳光试卷单元测试卷系列答案
阳光试卷单元测试卷系列答案科目:高中化学 来源: 题型:
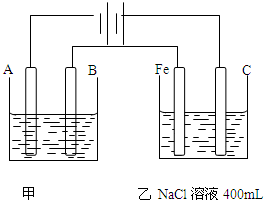 如图,外接电源为Zn-MnO2干电池,甲乙为相互串联的两个电解池,请回答:
如图,外接电源为Zn-MnO2干电池,甲乙为相互串联的两个电解池,请回答:查看答案和解析>>
科目:高中化学 来源: 题型:
 邻羟基苯甲酸(俗名水杨酸)其结构简式如图所示:
邻羟基苯甲酸(俗名水杨酸)其结构简式如图所示:查看答案和解析>>
科目:高中化学 来源: 题型:
| A、448mL |
| B、224mL |
| C、336mL |
| D、672mL |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、c(Na+)>c(HS-)>c(S2-)>c(H+)>c(OH-) |
| B、c(Na+)>c(S2-)>c(OH-)>c(HS-)>c(H+) |
| C、c(Na+)=c(HS-)+2 c(S2-)+c(OH-) |
| D、c(Na+)=c(HS-)+c(S2-)+c(H2S) |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、物质的量就是物质的质量 |
| B、阿伏加德罗常数约是6.02×1023mol-1 |
| C、气体摩尔体积一定是22.4L/mol |
| D、摩尔质量是以g为单位,数值上等于该种粒子的相对原子质量或相对分子质量 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、明矾能用于净水是冈为铝离子水解生成的氢氧化铝胶体具有强氧化性 |
| B、氯化铁溶液可用于制作印刷电路板是因为其能氧化铜 |
| C、浓硫酸可用作干燥剂是因为其具有强酸性 |
| D、光导纤维可用作通讯材料是因为其具有导电性 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、0.5mol/L CaCl2溶液中含Cl-数目为N0 |
| B、32g O2和O3的混合气体中含分子数目为N0 |
| C、标准状况下,22.4L N2和NO的混合气体中含原子数目为2N0 |
| D、常温常压下,含碳原子数目为0.5N0的CO2,质量是44g |
查看答案和解析>>
科目:高中化学 来源: 题型:
| ||
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com