
氯气是一种重要的化工原料。某学习小组在实验室中利用如图所示装置制取氯气并探究其性质。
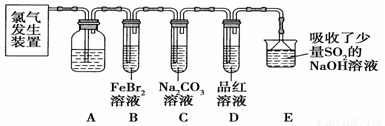
(1)实验室用二氧化锰和浓盐酸加热制取氯气,发生装置中除圆底烧瓶和导管外还需用到的玻璃仪器有 、 。
(2)装置A中盛有的试剂是: ,作用是:________________________。
(3)若D中品红溶液褪色,则B装置发生反应的离子方程式是: 。
(4)证明FeBr2与Cl2发生了(3)中氧化还原反应的实验方法是: (填操作方法)。
某研究性学习小组用刚吸收过少量SO2的NaOH溶液吸收处理上述实验后的尾气。经分析吸收尾气一段时间后,吸收液(呈强碱性)中肯定存在Cl-、OH-、CO32-和SO32-,对于可能存在的其他阴离子,研究小组提出以下3种假设:
假设1:只存在SO32-; 假设2:只存在ClO-; 假设3:既不存在SO32-,也不存在ClO-。
(5)学习小组判断同时存在SO32-和ClO-是不可能的,理由是: 。
(6)现限选以下试剂,设计实验方案,进行实验,请写出实验步骤以及预期现象和结论。
a. 3 mol·L-1 H2SO4 b.0.01 mol·L-1 KMnO4 c.1 mol·L-1 BaCl2溶液
d.淀粉碘化钾溶液 e.酚酞试液
步骤一:取少量吸收液于试管中,滴加3 mol·L-1 H2SO4至溶液呈中性,然后将所得溶液分装于A、B两试管中。
步骤二:向A试管中滴加少量 (填序号),若溶液__________________(填现象),则假设1成立。
步骤三:向B试管中滴加少量 (填序号),若溶液__________________(填现象),则假设2成立。
 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源:2016届福建省高三上12月月考化学试卷(解析版) 题型:选择题
现有物质的量浓度均为 0.1 mol·L - 1 的四种溶液各25mL:①氨水 ②NH4Cl 溶液
③Na2CO3溶液 ④NaHCO3溶液,下列说法正确的是:
A.4种溶液pH的大小顺序:①>④>③>②
B.①、②混合后pH>7,则混合溶液中c(NH4+)<c(NH3·H2O)
C.①、②中分别加入25mL 0.1 mol·L – 1盐酸后,溶液中c(NH4+):①>②
D.③、④中分别加入12.5mL 0.1 mol·L – 1NaOH溶液后,两溶液中离子种类相同
查看答案和解析>>
科目:高中化学 来源:2015-2016学年湖南省高二上第三次月考化学试卷(解析版) 题型:实验题
某小组以CoCl2·6H2O、NH4Cl、H2O2、浓氨水为原料,在活性炭催化下,合成了橙黄色晶体X。为确定其组成,进行如下实验。
①氨的测定:精确称取w g X,加适量水溶解,注入如图所示的三颈瓶中,然后逐滴加入足量10%NaOH溶液,通入水蒸气,将样品液中的氨全部蒸出,用V1 mL c1 mol·L-1的盐酸标准溶液吸收。蒸氨结束后取下接收瓶,用c2 mol·L-1 NaOH标准溶液滴定过剩的HCl,到终点时消耗V2 mL NaOH溶液。

②氯的测定。
回答下列问题:
(1)装置中安全管的作用原理是______________。
(2)用NaOH标准溶液滴定过剩的HCl时,应使用________式滴定管,可使用的指示剂为________。
(3)样品中氨的质量分数表达式为_________________。
(4)测定氨前应该对装置进行气密性检查,若气密性不好测定结果将_________(填“偏高”或“偏低”)。
(5)氯的测定采用莫尔法,莫尔法是一种沉淀滴定法,用标准硝酸银溶液滴定,进行测定溶液中Cl-的浓度。已知:
银盐 性质 | AgCl | AgBr | AgCN | Ag2CrO4 | AgSCN |
颜色 | 白 | 浅黄 | 白 | 砖红 | 白 |
溶解度(mol·L-1) | 1.3410-6 | 7.110-7 | 1.110-8 | 6.510-5 | 1.010-6 |
①若用AgNO3溶液滴定待测液,可选为滴定指示剂的是__________。
A.NaCl B.BaBr2 C.Na2CrO4 D KSCN
②滴定终点的现象是_____________________________________。
查看答案和解析>>
科目:高中化学 来源:2016届黑龙江省高三上期末理综化学试卷(解析版) 题型:选择题
X、Y、Z、W、Q是原子序数依次增大的五种短周期主族元素。其中只有Z是金属,W的单质是黄色固体,X、Y、W在周期表中的相对位置关系如图所示。下列说法正确的是
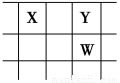
A.五种元素中,原子半径最大的是W
B.Y的简单阴离子比W的简单阴离子还原性强
C.Y与Z形成的化合物都可以和盐酸反应
D.Z与Q形成的化合物水溶液一定显酸性
查看答案和解析>>
科目:高中化学 来源:2016届吉林省高三上四次模拟化学卷(解析版) 题型:选择题
除去下列物质中所含的杂质,选用的试剂正确的是
选项 | 物质(杂质) | 试剂 |
A | Al2O3(SiO2) | NaOH溶液 |
B | CO2(SO2) | Na2CO3溶液 |
C | NO(NO2) | 水 |
D | NaHCO3(Na2CO3) | Ca(OH)2溶液 |
查看答案和解析>>
科目:高中化学 来源:2016届陕西省高三上12月模拟化学试卷(解析版) 题型:选择题
已知Fe3O4纳米颗粒稳定、容易生产且用途广泛,是临床诊断、生物技术和环境化学领域多种潜在应用的有力工具,水热法制备Fe3O4纳米颗粒的总反应为:3Fe2++2S2O32-+O2+4OH—=Fe3O4+S4O62-+2H2O,下列说法不正确的是
A.参加反应的氧化剂与还原剂的物质的量之比为1:5
B.若有2molFe2+被氧化,则被Fe2+还原的O2为0.5mol
C.每生成1molFe3O4,则转移电子数为4mol
D.O2是氧化剂,S2O32-和Fe2+是还原剂
查看答案和解析>>
科目:高中化学 来源:2015-2016学年江西省宜春市高一上学期第三次月考化学试卷(解析版) 题型:选择题
将15.6 g Na2O2和5.4 g Al同时放入一定量的水中,充分反应后得到200 mL溶液,再向该溶液中缓慢通入标准状况下的HCl气体6.72 L,若反应过程中溶液的体积保持不变,则
A. 反应过程中得到8.96 L的气体
B. 最终得到的溶液中溶质为NaCl
C. 最终Al元素全部以沉淀形式存在
D. 最终得到的溶液中n(NaCl)=0.3 mol
查看答案和解析>>
科目:高中化学 来源:2015-2016学年浙江省高二上学期第一次质检化学试卷(解析版) 题型:选择题
下列有关热化学方程式的叙述正确的是
A.已知2H2(g)+O2(g)=2H2O(g);△H=-483.6kJ/mol,则氢气的燃烧热为241.8 kJ/mol
B.已知C(石墨,s)=C(金刚石,s);△H>0,则金刚石比石墨稳定
C.含20.0g NaOH的稀溶液与稀盐酸完全中和,放出28.7kJ的热量,则表示该反应中和热的热化学方程式为:NaOH(aq)+HCl(aq)=NaCl(aq)+H2O(l);△H=-57.4kJ/mol
D.己知2C(s)+2O2(g)=2CO2(g);△H1 2C(s)+O2(g)=2CO(g);△H2 则△H1>△H2
查看答案和解析>>
科目:高中化学 来源:2015-2016年陕西西藏民族学院附属中学高二上期末化学卷(解析版) 题型:填空题
(1)化学反应可视为旧键断裂和新键形成的过程。化学键的键能是形成(或拆开)1 mol化学键时释放(或吸收)的能量。已知:N≡N键的键能是948.9kJ·mol-1,H-H键的键能是436.0 kJ·mol-1;由N2和H2合成1mol NH3时可放出46.2kJ的热量。N-H键的键能是_________
(2)由氢气和氧气反应生成1mol水蒸气,放热241.8KJ。写出该反应的热化学方程式:① 。
已知常温下NO与O2反应生成1molNO2的焓变为-57.07KJ,1molNO2与H2O反应生成HNO3溶液和NO的焓变为-46KJ,写出NO与O2及水生成HNO3溶液的热化学方程式② 。
(3)某温度下纯水中的c(H+) = 2×10-7mol/L,则此时c(OH-) =________mol/L,该纯水的pH_______(填“>7”、“<7”、“=7”)。若温度不变,滴入稀硫酸使c(H+) = 5×10-6mol/L,则c(OH-) =________mol/.
(4)(3分)纳米MgO可用于尿素与氯化镁合成。某小组研究该反应在温度为378~398K时的反应时间、反应物配比等因素对其产率的影响。请完成以下实验设计表:
编号 | 温度/K | 反应时间/h | 反应物物质的量配比 | 实验目的 |
① | 378 | 3 | 3:1 | 实验②和④探究a 实验②和b 探究反应时间对产率的影响 |
② | 378 | 4 | 4:1 | |
③ | 378 | 3 | c | |
④ | 398 | 4 | 4:1 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com