
| A. | 简单离子的半径:B>C>D>A | |
| B. | 氢化物的稳定性:C>D | |
| C. | B和其他3种元素均能形成离子化合物 | |
| D. | B与D形成的化合物溶于水所得溶液显酸性 |
分析 短周期主族元素A、B、C、D的原子序数依次增大,A、C的原子序数的差为8,说明A、C同主族,结合A、B、C 三种元素原子的最外层电子数之和为15,B原子最外层电子数等于A原子最外层电子数的一半,令B的最外层电子数为x,则x+2x+2x=15,解得x=3,再根据短周期元素A、B、C、D,原子序数依次递增,则A为氧元素,B为铝元素,C为硫元素,D为氯元素,以此解答该题.
解答 解:短周期主族元素A、B、C、D的原子序数依次增大,A、C的原子序数的差为8,说明A、C同主族,结合A、B、C 三种元素原子的最外层电子数之和为15,B原子最外层电子数等于A原子最外层电子数的一半,令B的最外层电子数为x,则x+2x+2x=15,解得x=3,再根据短周期元素A、B、C、D,原子序数依次递增,则A为氧元素,B为铝元素,C为硫元素,D为氯元素.
A.A为氧元素,B为铝元素,离子核外电子排布相同,核电荷数越大,离子半径越小,所以离子半径A>B,故A错误;
B.C为硫元素、D为氯元素,非金属性越强,对应的氢化物的稳定性越强,则稳定性D>C,故B错误;
C.氯化铝是共价化合物,故C错误;
D.B为铝元素、D为氯元素,二者形成的化合物是氯化铝,氯化铝是强酸弱碱盐,铝离子水解溶液呈酸性,故D正确.
故选D.
点评 本题考查学生利用原子的结构和位置来推断元素,为高频考点,侧重于学生的分析能力的考查,明确半径、金属性非金属性、最高价氧化物对应水化物的酸性的比较规律.


 通城学典默写能手系列答案
通城学典默写能手系列答案科目:高中化学 来源: 题型:多选题
| A. | 1mol 羟基(-OH)中电子数为9NA | |
| B. | 100 mL 2.0 mol•L-1的盐酸与醋酸溶液中氢离子数均为0.2NA | |
| C. | 将10.6 g Na2CO3固体溶于水,所得离子总数为0.3NA | |
| D. | 常温常压下,14g由N2与CO组成的混合气体含有的原子数目为NA |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
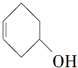 的叙述不正确的是( )
的叙述不正确的是( )| A. | 与HBr、溴水发生加成反应,产物都只有一种 | |
| B. | 分子式为C6H10O | |
| C. | 可发生加成、酯化和氧化反应 | |
| D. | 分子中有两种官能团 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
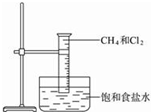 图是研究甲烷与氯气反应的实验装置图
图是研究甲烷与氯气反应的实验装置图查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 )偶联可由下列两个途径制备有机化合物Ⅵ.
)偶联可由下列两个途径制备有机化合物Ⅵ.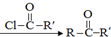
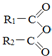 +H2O→R1-COOH+R2-COOH
+H2O→R1-COOH+R2-COOH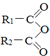

 .
. 、
、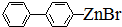 .
.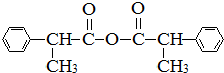 .
.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 | |
| 第2周期 | ⑦ | ⑧ | ||||||
| 第3周期 | ① | ③ | ⑤ | ④ | ⑨ | ⑩ | ||
| 第4周期 | ② | ⑥ |
 .
.查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | 14 | B. | 15 | C. | 16 | D. | 17 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com