
实验测得常温下0.1 mol/L某一元酸(HA)溶液的pH不等于1,0.1 mol/L某一元碱(BOH)溶液里:c(H+)/c(OH-)=10-12。将这两种溶液等体积混合后,所得溶液里各离子的物质的量浓度的关系正确的是( )
A.c(B+)=c(A-)>c(OH-)>c(H+) B.c(A-)>c(B+)>c(H+)>c(OH-)
C.c(B+)+c(H+)=c(A-)+c(OH-) D.c(B+)>c(A-)>c(H+)>c(OH-)
 互动英语系列答案
互动英语系列答案科目:高中化学 来源: 题型:
能正确表示下列反应的离子方程式是( )
A.Cl2通入NaOH溶液:Cl2+OH-===Cl-+ClO-+H2O
B.NaHCO3溶液中加入稀HCl:CO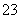 +2H+===CO2↑+H2O
+2H+===CO2↑+H2O
C.AlCl3溶液中加入过量稀氨水:Al3++4NH3·H2O===AlO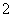 +4NH
+4NH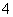 +2H2O
+2H2O
D.Cu溶于稀HNO3:3Cu+8H++2NO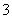 ===3Cu2++2NO↑+4H2O
===3Cu2++2NO↑+4H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
在100 mL 0.1 mol·L-1的醋酸溶液中,欲使醋酸的电离程度增大,H+浓度减小,可采用的方法是( )
A.加热
B.加入100 mL 0.1 mol·L-1的醋酸溶液
C.加入少量的0.5 mol·L-1的硫酸
D.加入少量的1 mol·L-1的NaOH溶液
查看答案和解析>>
科目:高中化学 来源: 题型:
在一定浓度的FeCl3溶液中,存在如下水解平衡:Fe3++3H2O Fe(OH)3+3H+,在此溶液中滴入饱和的FeCl3溶液,下列说法中正确的是( )
Fe(OH)3+3H+,在此溶液中滴入饱和的FeCl3溶液,下列说法中正确的是( )
A.水解平衡向正反应方向移动 B.水解平衡向逆反应方向移动
C.溶液中H+浓度不变 D.Fe3+的水解程度增大
查看答案和解析>>
科目:高中化学 来源: 题型:
判断以下几种叙述中不正确的是( )
A.某温度下,不论何种水溶液中c(H+)·c(OH-)乘积相等,即水的离子积是一个常数
B.醋酸钠和醋酸的混合液中若c(Na+)=c(CH3COO-),则溶液中c(H+)=c(OH-)
C.如果定义pOH=-lgc(OH-),则常温下某水溶液中的pOH和pH之和等于14
D.某水溶液由于条件的改变,如果氢离子浓度变小,则氢氧根离子浓度一定变大
查看答案和解析>>
科目:高中化学 来源: 题型:
(1)Fe2(SO4)3水溶液呈________性,原因是(用离子方程式表示) ;
实验室在配制Fe2 (SO4)3溶液时,需要加入________来抑制水解。
(2)泡沫灭火器中装有Al2(SO4)3溶液、NaHCO3溶液及起泡剂。写出使用时发生反应的离子方程式:_____________________________________________________。
| 实验编号 | HA物质的量浓度(mol/L) | NaOH物质的量浓度(mol/L) | 混合溶液的pH |
| ① | 0.1 | 0.1 | pH=9 |
| ② | C | 0.2 | pH=7 |
| ③ | 0.2 | 0.1 | pH<7 |
查看答案和解析>>
科目:高中化学 来源: 题型:
下列溶液中,各组离子可能大量共存的是 ( )
A.pH=7的溶液中:K+、Fe3+、Cl-、NO3—
B.强酸性溶液中:Cu2+、ClO-、Cl-、Ba2+
C.0.1 mol·L-1 的NaHCO3溶液中:K+、Al3+、Fe3+、NO3—
D.由水电离出的c(H+)=10-13 mol·L-1的溶液中:Al3+、K+、NO3—、SO42—
查看答案和解析>>
科目:高中化学 来源: 题型:
X、Y、Z、W四种物质的转化关系如图所示。下列组合中不符合转化关系的是( )
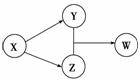
| 选项 | X | Y | Z | W |
| A | 浓盐酸 | FeCl2 | Cl2 | FeCl3 |
| B | Na2O2 | NaOH | Na2CO3 | NaHCO3 |
| C | Na2CO3 | CO2 | CaCO3 | Ca(HCO3)2 |
| D | SO2 | Na2SO3 | H2SO4 | NaHSO3 |
查看答案和解析>>
科目:高中化学 来源: 题型:
V L Fe2(SO4)3溶液中含有a g SO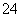 ,取此溶液0.5V L,用水稀释至2V L,则稀释后溶液中Fe3+的物质的量浓度为( )
,取此溶液0.5V L,用水稀释至2V L,则稀释后溶液中Fe3+的物质的量浓度为( )
A.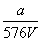 mol·L-1 B.
mol·L-1 B.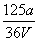 mol·L-1
mol·L-1
C.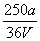 mol·L-1 D.
mol·L-1 D.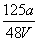 mol·L-1
mol·L-1
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com