

| A�� | 25��ʱ��NaHCO3��ˮ�е��ܽ�ȱ�Na2CO3�Ĵ� | |
| B�� | ͼ����ʾת����Ӧ����������ԭ��Ӧ | |
| C�� | �����¸����Cl2���ø�ƿ���棬����Cl2��������Ӧ | |
| D�� | H2��Cl2��Ӧʱ������ɫ���沢�γɰ��� |
���� A������ת����֪���Ȼ�����Һ�백����������̼��Ӧ����̼�������жϣ�
B������Ԫ�صĻ��ϼ��Ƿ�仯�жϣ�
C��������������ȼ�������ػ�ɫ����FeCl3��
D��������������Ӧʱ������ɫ��������HCl��
��� �⣺A����ת����֪���Ȼ�����Һ�백����������̼��Ӧ����̼�����ƣ���25��ʱ��NaHCO3��ˮ�е��ܽ�ȱ�Na2CO3��С����A����
B���Ȼ��ƺ�ˮ��������������̼�ķ�Ӧ�Լ�̼�����ƵķֽⷴӦ������������ԭ��Ӧ����B����
C��3Cl2+2Fe$\frac{\underline{\;��ȼ\;}}{\;}$2FeCl3����C����
D��������������Ӧʱ������ɫ��������HCl��HCl�ӷ����������γ�����СҺ���γɰ�������D��ȷ��
��ѡD��
���� ���⿼�����ε��ܽ��ԡ�������ԭ��Ӧ�����⣬��С���ۺ��⣻������ԭ��Ӧ���ݻ��ϼ۵ı仯�жϼ��ɣ�



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ʵ����
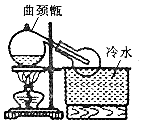 ʵ���ҳ���ŨH2SO4��NaNO3��ĩ��Ӧ��ȡHNO3��ʵ��װ����ͼ��
ʵ���ҳ���ŨH2SO4��NaNO3��ĩ��Ӧ��ȡHNO3��ʵ��װ����ͼ���鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
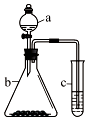 ������ͼ��ʾװ�ý���ʵ�飬������a�е���Һ����b�У�����c����ʢ��Һ��Ԥ������������ȷ���ǣ�������
������ͼ��ʾװ�ý���ʵ�飬������a�е���Һ����b�У�����c����ʢ��Һ��Ԥ������������ȷ���ǣ�������| ѡ�� | a | b | c | c�Թ������� |
| A | Ũ���� | KMnO4 | FeCl2��Һ | ��Һ���ػ�ɫ |
| B | ϡ���� | Na2S2O3 | ��ˮ | ����dz��ɫ���� |
| C | ���� | Na2CO3 | Na2SiO3��Һ | ������ɫ���� |
| D | Ũ���� | ��Ƭ | KI-������Һ | ��Һ����ɫ |
| A�� | A | B�� | B | C�� | C | D�� | D |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ͭ˿�ܵ��磬������ǵ���� | |
| B�� | BaSO4������ˮ��������Ƿǵ���� | |
| C�� | NaC1����״̬ʱ�ܵ��磬������ǵ���� | |
| D�� | ����������������ɢϵ�ı����Ǿ��ж����ЧӦ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ����ˮ��Ӧ��Na+2H2O�TNa++2OH-+H2�� | |
| B�� | ��������������������Һ��Al+2OH-�TAlO2-+H2�� | |
| C�� | Fe3O4�������Fe3O4+8H+�T3Fe3++4H2O | |
| D�� | �����Ȼ�����Һ��Ӧ��Fe+2Fe3+�T3Fe2+ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | 0.05mol/L �� H2SO4��Һ PH=1 | |
| B�� | 0.001mol/L �� NaOH��Һ PH=11 | |
| C�� | 0.005mol/L��H2SO4��Һ��0.0lmol/LNaOH��Һ������˺ϣ����ҺpH=6����Һ������ | |
| D�� | ��ȫ�к�PH=3��H2SO4��Һ50mL����ҪpH=11��NaOH��Һ50mL |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
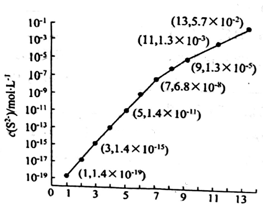
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ���ѡ��

| A�� | ���߱�ʾAlO2-�����ʵ����ı仯 | B�� | x��ʾAlCl3�����ʵ��� | ||
| C�� | ���߱�ʾAl��OH��3�����ʵ����ı仯 | D�� | ���߱�ʾAlO2-�����ʵ����ı仯 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ��ʹ������Ӧ������������KMnO4 | |
| B�� | ��������ԭ��Ӧ�����ӷ���ʽ��ˮ�ļ�����Ϊ5 | |
| C�� | ��������ԭ��Ӧ����������Fe2O42-������������Ӧ | |
| D�� | ��1mol��ԭ�����뷴Ӧʱ��ת��4NA������ |
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com