
��ͼ��Ϊ������ԭ����ͭ���Ϳ���ʵ��װ�á�ʵ��ǰ�Ƚ�ͭ˿1�������¶�������СԲ���������������ɴ�С��С�ף���ͭ˿2һ������������״���Իش��������⣺
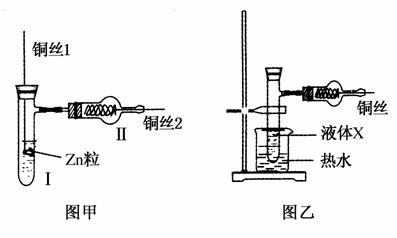
(1)���Թܢ����ȼ�����Լ���______________________��
(2)����ͭ˿2�ķ�����________________________________��
(3)ʵ��������___________________________________������______________________________________________��
(4)��������ͭ˿1���ŵ���__________________________����������ͭ˿2��Ŀ����____________________________��
(5)ijѧ����ͼ�ij�ͼ�ң������ڼ�����������ζ��Һ��X���Լ��ȣ�ͭ˿�IJ�������ͬͭ˿2��������ͭ˿���������ɺڱ�죬��Һ�������________��������������������________��
�𰸡�(1)�����ϡ���ᡡ(2)�ڢ��п�ʼ����H2��ͭ˿2�ھƾ����ϼ��ȵ����ȣ�Ѹ���������
(3)Zn�������ܽ⣬С���²���Zn��������д������ݲ��������ȵ�ͭ˿�ɺ�ɫ����Ϻ�ɫ
(4)�γ�ͭпԭ��أ�����H2�����ʿ죬ʵ�����ʱ�ɽ�ͭ˿�������𣬷�Ӧ�漴ֹͣ�������ڡ����շ�������ԭ����ͭ˿2����������״��Ϊ�˱���ͭ˿�ֲ����¶ȣ�����������ͭ�ڿ����г������ٵر���ԭ��(5)�Ҵ�(��������)���ǻ�
�����������ۺ���������ԭ����ͭ���Ҵ�����������ʵ�顣��ԭ����ͭ��ʵ��ؼ����¶ȵı��֣��Ƴ�����״��Ȼ��Ϊ�˱��ֽϸߵ��¶ȡ�



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
(1)�뽫���������ܹ������ķ�Ӧ��д���±��С�
������ϩ��������
����������������
����ϩʹ������Ȼ�̼��Һ��ɫ
����ϩͨ�����Ը��������Һ
�������ڿ�����ȼ��
���ɱ���ȡ������
| ��Ӧ���� | ȡ����Ӧ | �ӳɷ�Ӧ | ������Ӧ |
| ��Ӧ |
(2)���顢��ϩ���������л����о����������ʵ���(��д�ṹ��ʽ)
���ڼ��ȵ��������ܹ���Ũ���ᡢŨ��������Һ��Ӧ������ʹ���Ը��������Һ��ɫ����________��
�ڼ����ܸ�������Ӧ������ʹ���Ը��������Һ��ɫ����________��
���ڴ��������¼����������飬��ˮ���ɾƾ�����________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
���б仯��Ҫ��������������ʵ�ֵ���(����)
A��N2��NH3 B��MnO2��MnCl2
C��KI��KIO3 D��SO2��H2S
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
�������ʼ��������Լ�����ȷ����(����)
A���Ҵ���������CaCO3����
B���������ϩ��NaOH��Һ
C������CCl4�ͼ�����ˮ
D����ϩ����������ˮ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
Ӳ�ʲ������ǻ�ѧʵ���о���ʹ�õ�һ�����������������ʵ�飨�̶�װ���ԣ����ش����⡣
������ʵ�飺��ͼ��ʾ����Ũ�������װ��Na2SO3�����������һ��ʱ���a��b��c��������仯���±�������д���еĿհף�
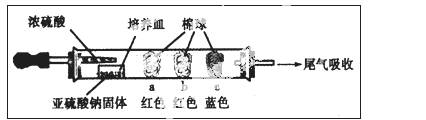
| ���� | �����ϵμӵ��Լ� | ʵ������ | ���ͺͽ��� |
| a |
| �����ף��Ⱥ��ָֻ���ɫ |
|
| b | ����̪��NaOH��Һ | �����Ϊ��ɫ | ���ӷ���ʽ�� |
| c |
| �����Ϊ��ɫ | ��������� (ѡ������ԡ���ԭ�ԡ�) |
��Ӳ�ʲ�����������װ�ý����ɶ��Ի���ʵ�顣��ͼ��ij�о���ѧϰС���ij����ʯ������������Ļ�ѧʽ����̽����װ�á�
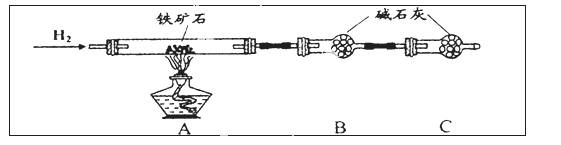
ʵ��һ������ʯ�к������IJⶨ
��1������ͼ��װ����(�г�������ʡ��)�����װ�õ������ԣ�
��2����10��0g����ʯ����Ӳ�ʲ������У�
��3������˵����ܿڴ����ϵػ���ͨ��H2�� ��ȼA���ƾ��ƣ�
��4����ַ�Ӧ�����ƾ��ƣ��ٳ���ͨ����������ȫ��ȴ��
��5����÷�Ӧ��װ��B����2.70g��������ʯ��������������Ϊ______________________��
ʵ���������ʯ�к������IJⶨ
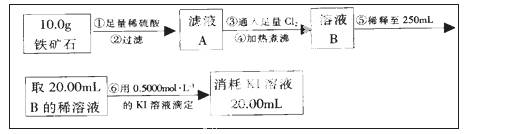
��1������ں͢��ж�Ҫ�õ��IJ��������� __��
��2�������йز���IJ�����˵������ȷ����_______��
a���ζ���������ˮϴ�Ӻ����ô�װҺ��ϴ
b����ƿ��Ҫ�ô���Һ��ϴ
c����Ϊ��ˮΪ��ɫ�����Եζ������в����ָʾ��
ʵ����ۣ������������������ɣ���ʵ��һ�����ó�������ʯ������������Ļ�ѧʽΪ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
�����������һ����Ҫ�Ļ�����Ʒ��ij��ȤС�����Ʊ���������ƾ��壨Na2S2O3·5H2O����
I��[��������]
��1��Na2S2O3·5H2O����ɫ�����壬������ˮ����ϡ��Һ��BaCl2��Һ����������ɡ�
��2����Na2CO3��Na2S���Һ��ͨ��SO2���Ƶ�Na2S2O3�����ò�Ʒ�г���������Na2SO3��Na2SO4��
��3��Na2SO3�ױ�������BaSO3������ˮ��������ϡHCl��
��[�Ʊ���Ʒ]
ʵ��װ����ͼ��ʾ��ʡ�Լг�װ�ã�
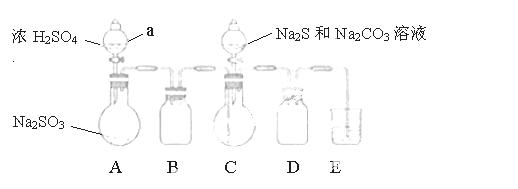
ʵ�鲽�裺
��1�����װ�������ԣ���ͼʾ�����Լ�������a��������____��E�е��Լ���___��ѡ��������ĸ��ţ���
A��ϡH2SO4 B��NaOH��Һ C������NaHSO3��Һ
��2������C����ƿ����Na2S��Na2CO3�����Һ������A����ƿ�μ�ŨH2SO4��
��3����Na2S��Na2CO3��ȫ���ĺ�����Ӧ������C�л��Һ����Һ��____����д�������ƣ����ᾧ�����ˡ�ϴ�ӡ�����õ���Ʒ��
��[̽���뷴˼]
��1��Ϊ��֤��Ʒ�к���Na2SO3��Na2SO4����С�����������ʵ�鷽�����뽫���������������������Լ���ϡHNO3��ϡH2SO4��ϡHCl������ˮ��ѡ��
ȡ������Ʒ���ϡ��Һ���μ�����BaCl2��Һ���а�ɫ�������ɣ�_____��������δ��ȫ�ܽ⣬���д̼�����ζ��������������ȷ����Ʒ�к���Na2SO3��Na2SO4��
��2��Ϊ����װ��C�����ɵ�Na2SO4�������ڲ��ı�ԭ��װ�õĻ����϶�ԭ��ʵ�鲽�裨2�������˸Ľ����Ľ���IJ�����_______��
��3��Na2S2O3·5H2O���ܽ�����¶����������������ò�Ʒͨ��_____�����ᴿ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����ȷ��ʾ���л�ѧ��Ӧ�����ӷ���ʽ�ǣ�������
| �� | A�� | ��̼������Һ����������������2CO32��+SO2+H2O=2HCO3��+SO32�� |
| �� | B�� | ����������������Al+2H+=Al3++H2�� |
| �� | C�� | ��������ˮ�У�S2��+2H2O=H2S��+2OH�� |
| �� | D�� | ̼��þ���������У�CO32��+2H+=H2O+CO2�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
��ͼ��ʾ�����Թܷ���ʢ��25�汥��ʯ��ˮ���ձ��У��Թܿ�ʼ���뼸С��þƬ�����õιܵ���5mL�������Թ��С��Իش��������⣺
��1��ʵ���й۲쵽������________________________________��
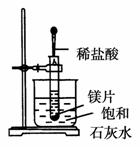 ��2���������������ԭ����_____________________________��
��2���������������ԭ����_____________________________��
��3�����÷�Ӧ��Ƴ�һ��ԭ��أ�����װ��ͼ������ԭ��ظ��������ƣ� ������������
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com