
下列说法不正确的是
A.为除去FeSO4溶液中的Fe2(SO4)3,可加入铁粉,再过滤
B.为除去溴苯中的溴,可用NaOH溶液洗涤,再分液
C.为除去乙炔气中少量的H2S,可使其通过CuSO4溶液
D.为除去CO2中少量的SO2,可使其通过饱和Na2CO3溶液
科目:高中化学 来源:2014-2015云南省高一3月月考化学试卷(解析版) 题型:选择题
合乎实际并用于工业生产的是
A、金属钠在氯气中燃烧制氯化钠 B、氢气和氯气混合经光照制氯化氢
C、氯气通入澄清石灰水中制漂白粉 D、高温分解石灰石制生石灰
查看答案和解析>>
科目:高中化学 来源:2014-2015学年广东湛江高三第二次模拟考试理综化学试卷(解析版) 题型:填空题
(16分)乙酰水杨酸是一种使用广泛的解热镇痛剂。合成原理是:
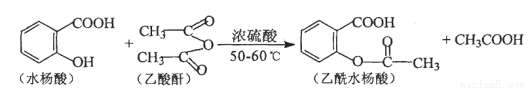
(1)乙酰水杨酸的分子式为 ,1 mol乙酰水杨酸最多能与 mol H2 反应。
(2)上面反应的反应类型是 。
(3)有关水杨酸的说法,不正确的是 。
A.能与溴水发生取代反应和加成反应
B.可发生酯化反应和水解反应
C.1 mol水杨酸最多能与2 mol NaOH反应
D.遇FeCl3溶液显紫色
(4)乙酰水杨酸与足量KOH溶液反应的化学方程式为 。
(5)乙酰氯(CH3COCl )也可以与水杨酸反应生成乙酰水杨酸,请写出化学反应方程式(不写条件) 。
(6)写出一种符合下列条件的乙酰水杨酸的同分异构体的结构简式: 。
Ⅰ.能遇FeCl3溶液显色
Ⅱ.苯环上只有2种一溴取代物
Ⅲ.1 mol该化合物能分别与含4 mol Br2的溴水或4 mol H2 反应
查看答案和解析>>
科目:高中化学 来源:2014-2015学年甘肃省天水市高三下学期二模考试理综化学试卷(解析版) 题型:选择题
卤素互化物与卤素单质性质相似。已知CH2=CH—CH=CH2(1,3—丁二烯)与氯气发生加成产物有三种:
①CH2Cl—CHCl—CH=CH2 (1,2—加成)
②CH2Cl—CH=CH—CH2Cl (1,4—加成)
③CH2Cl—CHCl—CHCl—CH2Cl(完全加成)
据此推测CH2=C(CH3)—CH=CH2(异戊二烯)与卤素互化物BrCl的加成产物有几种(不考虑顺反异构和镜像异构
A.6种 B.10种 C.12种 D.14种
查看答案和解析>>
科目:高中化学 来源:2014-2015学年北京市西城区高三二模理综化学试卷(解析版) 题型:简答题
(13分)氯气是重要的化工原料,有广泛的用途。
(1)氯气的电子式是______。
(2)电解饱和食盐水制氯气的离子方程式是______。
(3)工业上用H2和Cl2反应制HCl,反应的能量变化如图所示:

①该反应的热化学方程式是______。
②实验室配制FeCl3溶液时,将FeCl3固体溶解在稀盐酸中,请结合离子方程式用平衡移动原理解释原因______。
(4)新制饱和氯水中存在:Cl2+H2O HCl+HClO,为使平衡向正反应方向移动,下列措施可行的是______。
HCl+HClO,为使平衡向正反应方向移动,下列措施可行的是______。
a.加少量NaOH固体 b.加CaCO3固体 c.加NaCl固体
(5)“氯胺(NH2Cl)消毒法”是在用液氯处理自来水的同时通入少量氨气,发生反应:Cl2+NH3=NH2Cl+HCl。NH2Cl能与水反应生成可以杀菌消毒的物质,该反应中元素的化合价不变。
①NH2Cl与水反应的化学方程式是______。
②在Cl2+NH3=NH2Cl+HCl中,每消耗11.2 L Cl2(标准状况下),转移电子______mol。
查看答案和解析>>
科目:高中化学 来源:2014-2015学年北京市海淀区高三第二学期期末练习理综化学试卷(解析版) 题型:简答题
(14分)某种锂离子电池的正极材料是将含有钴酸锂(LiCoO2)的正极粉均匀涂覆在铝箔上制成的,可以再生利用。某校研究小组尝试回收废旧正极材料中的钴。
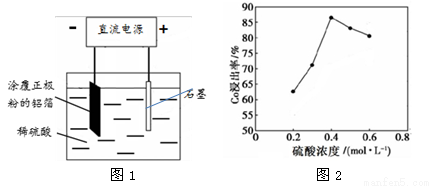
(1)25℃时,用图1所示装置进行电解,有一定量的钴以Co2+的形式从正极粉中浸出,且两极均有气泡产生,一段时间后正极粉与铝箔剥离。
①阴极的电极反应式为:LiCoO2 + 4H+ + e- === Li+ + Co2+ + 2H2O 、 。
阳极的电极反应式为 。
②该研究小组发现硫酸浓度对钴的浸出率有较大影响,一定条件下,测得其变化曲线如图2所示。当c(H2SO4) > 0.4 mol·L-1时,钴的浸出率下降,其原因可能为 。
(2)电解完成后得到含Co2+的浸出液,且有少量正极粉沉积在电解槽底部。用以下步骤继续回收钴。
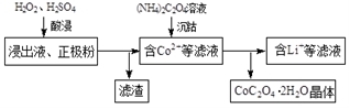
①写出“酸浸”过程中正极粉发生反应的化学方程式 。该步骤一般在80℃以下进行,温度不能太高的原因是 。
②已知(NH4)2C2O4溶液呈弱酸性,下列关系中正确的是 (填字母序号)。
a.c (NH4+)> c(C2O42-)>c (H+)>c (OH-)
b.c (H+) +c (NH4+) =c (OH-) + c(HC2O4-)+c(C2O42-)
c.c (NH4+)+ c (NH3H2O ) = 2[c(C2O42-) + c(HC2O4-) + c(H2C2O4)]
(3)已知所用锂离子电池的正极材料为x g,其中LiCoO2(M = 98 g·mol-1)的质量分数为a%,则回收后得到CoC2O42H2O (M = 183 g·mol-1)的质量不高于 g。
查看答案和解析>>
科目:高中化学 来源:2014-2015学年北京市海淀区高三第二学期期末练习理综化学试卷(解析版) 题型:选择题
下列说法不正确的是
A.甲苯和环己烯都能使酸性高锰酸钾溶液褪色
B.用银氨溶液可以鉴别乙醛和葡萄糖溶液
C.甲醛和乙二醇都可作为合成高分子化合物的单体
D.丙烷和2-甲基丙烷的一氯代物均为两种
查看答案和解析>>
科目:高中化学 来源:2014-2015学年北京市丰台区高三第二次模拟理综化学试卷(解析版) 题型:推断题
(16分)苯酚是一种重要的化工原料,可以合成长效缓释阿司匹林。阿司匹林能迅速解热、镇痛和消炎,长效缓释阿司匹林可在人体内逐步水解使疗效更佳。
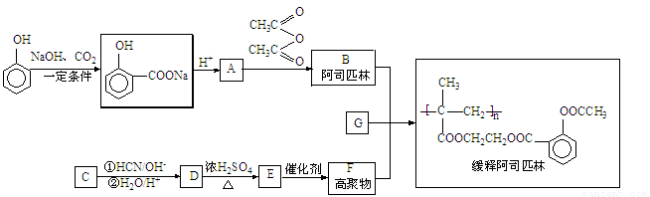
已知:
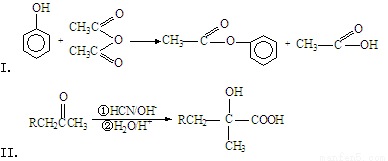
(1)A的结构简式为____________,写出E→F的反应类型____________。
(2)若阿司匹林中混有A物质,可选择的检验试剂是(填字母)____________。
a.NaHCO3溶液 b.石蕊溶液 c.FeCl3溶液
(3)写出A→B的化学反应方程式____________。
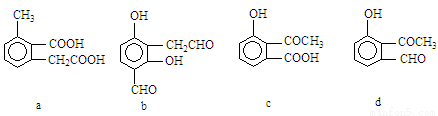
(4)下列物质与阿司匹林互为同分异构体的有(填字母)____________。
(5)C的结构简式为____________。
(6)写出D→E的化学反应方程式____________。
(7)写出一定条件下生成缓释阿司匹林的化学方程式____________。
查看答案和解析>>
科目:高中化学 来源:2014-2015浙江省高二4月月考化学试卷(解析版) 题型:填空题
(12分)
(1)请写出下列物质的结构简式:
①2-甲基-3-乙基戊烷: ;
②2,3-二甲基-1-丁烯: 。
(2)请写出下列物质的名称:

(3)在有机反应中,反应条件尤为重要。条件(如温度、溶剂、催化剂等)改变,反应产物可能会随之改变。
①已知苯与浓硝酸、浓硫酸的混合物在50-60℃反应时生成硝基苯;若反应条件升温至100-110℃时,反应的化学方程式为 。
②卤代烃与碱反应时,溶剂不同则产物不同。若溴乙烷与氢氧化钾的水溶液反应,反应的化学方程式为: 。
③甲苯能与溴蒸汽在光照条件下发生反应生成一溴代物,反应的化学方程式为: 。
(4)某有机分子结构如下:
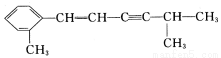
该分子中至少有 个C原子在同一平面,最多有 个C原子在同一平面。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com