
有关热化学方 程式书写与对应表述均正确的是( )
程式书写与对应表述均正确的是( )
A.稀醋酸与0.1 mol·L-1 NaOH溶液反应:
H+(aq)+OH-(aq)====H2O(l) ΔH=-57.3 kJ·mol-1
B.氢气的燃烧热为285.5 kJ·mol-1, 则水分解的热化学方程式
2H2O(l)====2H2(g)+O2(g) ΔH=+285.5 kJ·mol-1
C.密闭容器中,9.6 g硫粉与11.2 g铁粉混合加热生成硫化亚铁17.6 g时,放出19.12 kJ热量。 则Fe(s)+S(s)====FeS(s) ΔH=-95.6 kJ·mol-1
D.已知2C(s)+O2(g)====2CO(g) ΔH=-221 kJ·mol-1,则可知C的燃烧热为110.5 kJ·m ol-1
ol-1
 第三学期赢在暑假系列答案
第三学期赢在暑假系列答案 学练快车道快乐假期暑假作业新疆人民出版社系列答案
学练快车道快乐假期暑假作业新疆人民出版社系列答案 浙大优学小学年级衔接导与练浙江大学出版社系列答案
浙大优学小学年级衔接导与练浙江大学出版社系列答案科目:高中化学 来源: 题型:
煤燃烧的反应热可通过以下两个途径来利用:a.利用煤在充足的空气中直接燃烧产生的反应热;b.先使煤与水蒸气反应得到氢气和一氧化碳,然后使得到的氢气和一氧化碳在充足的空气中燃烧。这两个过程的热化学方程式为:
a.C(s)+O2(g)===CO2(g) ΔH=E1①
b.C(s)+H2O(g)===CO(g)+H2(g) ΔH=E2②
H2(g)+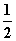 O2(g)===H2O(g) ΔH=E3③
O2(g)===H2O(g) ΔH=E3③
CO(g)+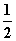 O2(g)===CO2(g) ΔH=E4④
O2(g)===CO2(g) ΔH=E4④
回答:
(1)上述四个热化学方程式中的哪些反应ΔH<0?
________________________________________________________________________。
(2)等质量的煤分别通过以上两条不同的途径产生的可利用的总能量关系正确的是( )
A.a比b多 B.a比b少 C.a与b在理论上相同
(3)根据能量守恒定律,E1、E2、E3、E4之间的关系为________________________
________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
据报道,我国拥有的完全自主产权的氢氧燃料电池车已在北京奥运会期间为运动员提供了服务。某种氢氧燃料电池的电解液为KOH溶液,下列有关该电池的叙述不正确的是( )
A.正极反应式为O2+2H2O+4e-—→4OH-
B.工作一段时间后,电解液中KOH的物质的量不变
C.该燃料电池的总反应方程式为2H2+O2===2H2O
D.用该电池电解CuCl2溶液,产生2.24 L Cl2(标准状况)时,有0.1 mol电子转移
查看答案和解析>>
科目:高中化学 来源: 题型:
我国卫星发射所用的长征2号火箭的主要燃料是偏二甲肼(C2H8N2),氧化剂是NO2,燃烧产物只有N2、CO2和H2O。有的国家用肼(N2H4)作为火箭发动机的燃料。NO2为氧化剂,反应生成N2和水蒸气。已知:
N2(g)+2O2(g)====2NO2(g) ΔH=+67.7 kJ·mol-1
N2H4(g)+O2(g)====N2(g)+2H2O(g) ΔH=-534 kJ·mol-1。
下列关于肼和NO2反应的热化学方程式中正确的是( )
A.2N2H4(g)+2NO2(g)====3N2(g)+4H2O (l) ΔH=+1 135.7 kJ·mol-1
B.2N2H4(g)+2NO2(g)====3N2(g)+4H2O(l) ΔH=-1 135.7 kJ·mol-1
C.N2H4(g)+NO2(g)====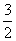 N2(g)+2H2O(g) ΔH=+1 135.7 kJ·mol-1
N2(g)+2H2O(g) ΔH=+1 135.7 kJ·mol-1
D.2N2H4(g)+2NO2(g)====3N2(g)+4H2O(g) ΔH=-1 135.7 kJ·mol-1
查看答案和解析>>
科目:高中化学 来源: 题型:
将NaCl溶液滴在一块光亮清洁的铁板表面上,一段时间后发现液滴覆盖的圆周中心区(a)已被腐蚀而变暗,在液滴外沿形成棕色铁 锈环(b),如图所示。导致该现象的主要原因是液滴之下氧气含量比边缘少。下列说法正确的是( )
锈环(b),如图所示。导致该现象的主要原因是液滴之下氧气含量比边缘少。下列说法正确的是( )
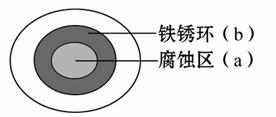
A.液滴中的Cl-由a区向b区迁移
B.液滴边缘是正极区,发 生的电极反应为O2+2H2O+4e-====4OH-
生的电极反应为O2+2H2O+4e-====4OH-
C.液滴下的Fe因发生还原反应而被腐蚀,生成的Fe2+由a区向b区迁移,与b区的OH―形成Fe(OH)2,进一步氧化、脱水形成铁锈
D.若改用嵌有一铜螺丝钉的铁板,在铜铁接触处滴加NaCl溶液,则负极发生的电极反应为Cu-2e-====Cu2+
查看答案和解析>>
科目:高中化学 来源: 题型:
可燃冰中蕴藏着大量的甲烷,有望成为未来新能源。已知1 mol CH4气体完全燃烧生成CO2气体和液态H2O时放出的热量为890.3 kJ,当它不完全燃烧生成CO气体和液态H2O时,放出的热量为519 kJ。如果1 mol CH4在n g O2中燃烧生成CO、CO2气体和液态H2O,放出731.25 kJ热量。
(1)写出表示甲烷燃烧热的热化学方程式。
(2)写出甲烷气体不完全燃烧的热化学方程式。
(3)计算n的值。
查看答案和解析>>
科目:高中化学 来源: 题型:
温度为T时,向2.0 L 恒容密闭容器中充入1.0 mol PCl5,反应PCl5(g)====PCl3(g)+Cl2(g)经过一段时间后达到平衡。反应过程中测定的部分数据见下表:
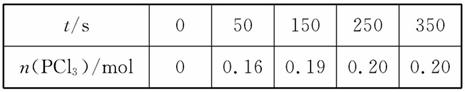
下列说法正确的是( )
A.反应在前50 s的平均速率
v(PCl3)=0.003 2 mol·L-1·s-1
B.保持其他条件不变,升高温度,平衡时c(PCl3)=0.11 mol·L-1,则反应的ΔH<0
C.相同温度下,起始时向容器中充入1.0 mol PCl5、0.20 mol  PCl3 和0.20 mol Cl2,反应达到平衡前v(正)>v(逆)
PCl3 和0.20 mol Cl2,反应达到平衡前v(正)>v(逆)
D.相同温度下,起始时向容器中充入2.0 mol PCl3和2.0 mol Cl2,达到平衡时,PCl3 的转化率小于80%
查看答案和解析>>
科目:高中化学 来源: 题型:
已知下列反应的热化学方程式:
6C(s)+5H2(g)+3N2(g)+9O2(g)===2C3H5(ONO2)3(l)ΔH1
2H2(g)+O2(g)===2H2O(g)ΔH2
C(s)+O2(g)===CO2(g)ΔH3
则反应4C3H5(ONO2)3(l)===12CO2(g)+10H2O(g)+O2(g)+6N2(g)的ΔH为
( )
A.12ΔH3+5ΔH2-2ΔH1 B.2ΔH1-5ΔH2-12ΔH3
C.12ΔH3-5ΔH2-2ΔH1 D.ΔH1-5ΔH2-12ΔH3
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com