
25℃时,0.1 mol Na2CO3与盐酸混合所得的一组体积为1 L的溶液,溶液中部分微粒与pH的关系如下图所示。下列有关溶液中离子浓度关系叙述正确的是( )
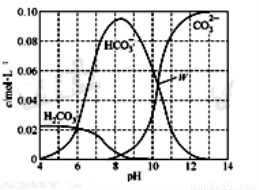
A.W点所示的溶液中:c(Na+)+c(H+)=2c(CO32-)+c(OH-)+c(Cl-)
B.pH=4的溶液中:c(H2CO3)+c(HCO3-)+c(CO32-)<0.1mol·L-1
C.pH=8的溶液中:c(H+)+c(H2CO3)+c(HCO3-)=c(OH-)+c(Cl-)
D.pH=11的溶液中:c(Na+)>c(Cl-)>c(CO32-)>c(HCO3-)>c(H2CO3)
科目:高中化学 来源:2016-2017学年甘肃省高二上10月月考化学试卷(解析版) 题型:选择题
相同体积、相同pH的某一元强酸溶液①和某一元弱酸溶液②分别与足量的锌粉发生反应,下列关于氢气体积(V)随时间(t)变化的示意图正确的是( )
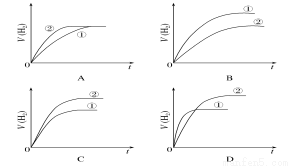
查看答案和解析>>
科目:高中化学 来源:2017届安徽省黄山市高三上月考二化学卷(解析版) 题型:推断题
【化学—选修5:有机化学基础】
盐酸普鲁卡因(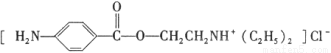 )是一种局部麻醉剂,麻醉作用较快、较强,毒性较低,其合成路线如下:
)是一种局部麻醉剂,麻醉作用较快、较强,毒性较低,其合成路线如下:
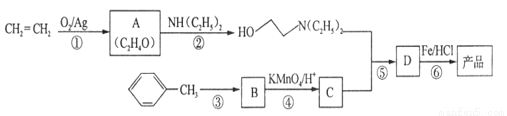
已知:①
②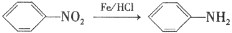
③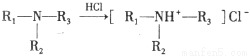
请回答以下问题:
(1)A的核磁共振氢谱只有一个峰,则A的结构简式为 。
(2)C的结构简式为 ,C中含有的含氧官能团的名称为 。
(3)合成路线中属于氧化反应的有 (填序号),反应③的反应类型为 。
(4)反应⑤的化学反应方程式为 。
(5)B的某种同系物E,相对分子质量比B大14,其中—NO2与苯环直接相连,分子的核磁共振氢谱有3个峰,则E的结构简式为 (写一种)。
(6)符合下列条件的E的同分异构体的数目有 种。
① 结构中含有一个“—NH2”与一个“—COOH”
② 苯环上有三个各不相同的取代基
(7)苯丙氨酸(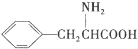 )是人体必需的氨基酸之一,写出其发生缩聚反应的化学方程式 。
)是人体必需的氨基酸之一,写出其发生缩聚反应的化学方程式 。
查看答案和解析>>
科目:高中化学 来源:2017届安徽省黄山市高三上月考二化学卷(解析版) 题型:选择题
某同学组装了如图所示的电化学装置,其中电极I为Al,其它均为Cu,下列说法正确的是( )
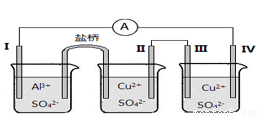
A.装Al2(SO4)3 溶液的烧杯是原电池,其余两个为电解(电镀)池
B.盐桥中电子从右侧流向左侧
C.电极II逐渐溶解
D.电极IV的电极反应:Cu2+ + 2e- = Cu
查看答案和解析>>
科目:高中化学 来源:2017届安徽省黄山市高三上月考二化学卷(解析版) 题型:选择题
设NA为阿伏加德罗常数的值,下列叙述正确的是( )
A.常温常压下,22.4 L乙烯中C—H键数为4 NA
B.1 mol羟基中电子数为10 NA
C.在反应KIO3 + 6 HI = KI + 3 I2 + 3 H2O中,每生成3 mol I2转移的电子数为6 NA
D.常温下,1 L 0.1 mol·L-1 的NH4NO3溶液中氮原子数为0.2 NA
查看答案和解析>>
科目:高中化学 来源:2017届重庆一中高三上学期第二次月考化学试卷(解析版) 题型:选择题
下列实验操作、现象及由此得出的结论均正确的是
选项 | 实验操作 | 现象 | 结论 |
A | 将铜粉加入1.0 mol·L-1Fe2(SO4)3溶液中 | 铜粉溶解 | 金属铜比铁活泼 |
B | 将pH试纸放在玻片上,用玻璃棒蘸取某新制氯水,点在pH试纸中央,与标准比色卡对照 | pH=2 | 氯气与水反应生成了强酸 |
C | 向含有Fe2+的MgSO4溶液中,先加H2O2溶液,然后再调溶液的pH约为5 | 有红褐色沉淀生成 | Fe2+被H2O2氧化为Fe3+ |
D | 将KI和FeCl3溶液在试管中混合后,加入汽油,振荡,静置 | 下层溶液显紫红色 | 生成的I2全部溶于汽油中 |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
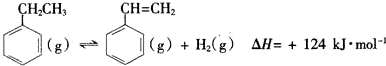
| 化学键 | C-H | C-C | C=C | H-H |
| 键能/kJ•mol-1 | 412 | 348 | x | 436 |
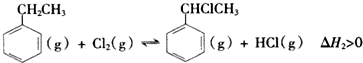
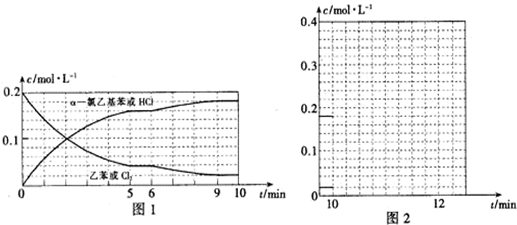
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
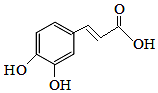
| A. | 能发生加聚反应 | |
| B. | 能与碳酸钠溶液反应 | |
| C. | 1 mol咖啡酸最多能与3 mol NaOH反应 | |
| D. | 1 mol咖啡酸最多能与 3 mol Br2反应 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com