
向一定量的Fe、FeO和Fe2O3的混合物中加入120 mL 4 mol·L-1的稀硝酸,恰好使混合物完全溶解,放出1.344 L NO(标准状况),向所得溶液中加入KSCN溶液,无血红色出现。若用足量的氢气在加热条件下还原相同质量的混合物能得到铁的物质的量为( )
A.0.21 mol B.0.24 mol
C.0.16 mol D.0.14 mol
科目:高中化学 来源: 题型:
重水(D2O)是重要的核工业原料,下列说法错误的是( )
A.重水是原子反应堆的导热剂
B.氘(D)原子核内有1个中子
C.H2O与D2O的物理性质不相同
D.1H、D与16O、18O形成的水分子,其相对分子质量不相同的有5种
查看答案和解析>>
科目:高中化学 来源: 题型:
下列与有机物的结构、性质有关的叙述正确的是( )
A.苯、油脂均不能使酸性KMnO4溶液褪色
B.医用酒精的浓度通常为95%
C.乙醇可以被氧化为乙酸,二者都能发生取代反应
D.淀粉和蛋白质均可作为生产葡萄糖的原料
查看答案和解析>>
科目:高中化学 来源: 题型:
下列说法正确的是( )
A.甲苯和乙烯均可使酸性KMnO4溶液褪色
B.纤维素、淀粉和蛋白质都是高分子化合物
C.煤的干馏和石油的分馏均属化学变化
D.酯类和糖类均能发生水解反应
查看答案和解析>>
科目:高中化学 来源: 题型:
在水中加入等物质的量的Ag+、Pb2+、Na+、SO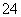 、NO
、NO 、Cl-,该溶液放在用惰性电极材料作电极的电解槽中,通电片刻,则氧化产物与还原产物质量比为( )
、Cl-,该溶液放在用惰性电极材料作电极的电解槽中,通电片刻,则氧化产物与还原产物质量比为( )
A.35.5∶108 B.16∶207
C.8∶1 D.108∶35.5
查看答案和解析>>
科目:高中化学 来源: 题型:
通过化学反应原理猜测可能生成哪些物质,对这些物质逐一进行检验来确定究竟含有哪些物质。正确解答此类试题的关键:(1)猜测要全面;(2)熟记常见物质的检验方法。
| [典例] | 审题指导 |
| 某研究性学习小组用下列装置(铁架台等夹持仪器略)探究氧化铁与乙醇的反应,并检验反应产物。 | 联想:乙醇的催化氧化。 |
| (1)用2%的CuSO4溶液和10%的NaOH溶液配制Cu(OH)2悬浊液的注意事项是________________________________________________________________________。 | 新制Cu(OH)2悬浊液与醛基的反应需要碱性条件。 |
| (2)为快速得到乙醇气体,可采用的方法是________________________________________________________________________。 若实验时小试管中的溶液已经开始发生倒吸,可采取的措施是________(填字母)。 a.取下小试管 b.移去酒精 c.将导管从乳胶管中取下 d.以上都可以 | ①升高温度可加速乙醇的挥发。 ②若液体倒吸入加热的反应管,可能会造成反应管炸裂,取下小试管已无济于事,因“溶 液已经开始发生倒吸”。 |
| (3)如图实验,观察到红色的Fe2O3全部变为黑色固体M,充分反应后停止加热。取下小试 管,加热,有砖红色沉淀生成。 为了检验M的组成,进行下列实验。 ①M能被磁铁吸引;加入足量稀硫酸,振荡,固体全部溶解,未观察到有气体生成; ②经检验溶液中有铁离子和亚铁离子,检验铁离子的方法是_____________________;证明溶液含有亚铁离子的方法是________________________________________________________________________。 能得出的结论是________(填字母)。 a.M中一定有+3价和+2价铁,不能确定是否有0价铁 b.M中一定有+3价和0价铁,无+2价铁 c.M中一定有+3价铁,0价和+2价铁至少有一种 d.M中一定有+3价、+2价和0价铁 | 破题关键 分析黑色固体(M)可能的成分,铁的氧化物Fe3O4、FeO和铁粉均为黑色,Fe3O4中既有+3价铁又有+2价铁,且具有磁性,Fe3+能溶 解单质铁。 易错警示 已知溶液中有Fe3+,检验Fe2+不能用KSCN 溶液。 |
| (4)若M的成分可表达为FexOy,用CO还原法定量测定其化学组成。称取m g M样品进行定量测定,实验装置和步骤如下:
①组装仪器;②点燃酒精灯;③加入试剂;④打开分液漏斗活塞;⑤检查气密性;⑥停止加热;⑦关闭分液漏斗活塞;⑧…… 正确的操作顺序是________(填字母)。 a.①⑤④③②⑥⑦⑧ b.①⑤③④②⑥⑦⑧ c.①③⑤④②⑦⑥⑧ d.①③⑤②④⑥⑦⑧ 若M完全被还原后碱石灰增重n g,则 | 破题关键 Ⅰ.检查气密性属于实验的准备阶段,应在加药品前进行。 Ⅱ.类比氢气还原氧化铜。 Ⅲ.碱石灰增加的质量即为反应产生的CO2的质量,得关系式M中n(O)=n(CO2)。 |
查看答案和解析>>
科目:高中化学 来源: 题型:
分析下图所示的四个原电池装置,其中结论正确的是( )
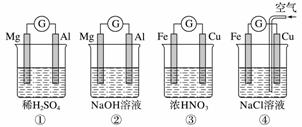
A.①②中Mg作负极,③④中Fe作负极
B.②中Mg作正极,电极反应式为6H2O+6e-===6OH-+3H2↑
C.③中Fe作负极,电极反应式为Fe-2e-===Fe2+
D.④中Cu作正极,电极反应式为2H++2e-===H2↑
查看答案和解析>>
科目:高中化学 来源: 题型:
液体燃料电池相比于气体燃料电池具有体积小,无需气体存储装置等优点。一种以肼(N2H4)为燃料的电池装置如图所示。该电池用空气中的氧气作为氧化剂,KOH作为电解质。下列关于该燃料电池的叙述不正确的是( )
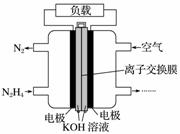
A.电流从右侧电极经过负载后流向左侧电极
B.负极发生的电极反应式为N2H4+4OH--4e-===N2+4H2O
C.该燃料电池的电极材料应采用多孔导电材料,以提高电极反应物质在电极表面的吸附量,并使它们与电解质溶液充分接触
D.该燃料电池持续放电时,K+从负极向正极迁移,因而离子交换膜需选用阳离子交换膜
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com