
| A、醋酸能与碳酸钠反应,并有二氧化碳气体生成 |
| B、醋酸溶液能使紫色石蕊试液变红 |
| C、用醋酸溶液做导电性实验时,灯泡较暗 |
| D、在pH相等的醋酸和盐酸中,前者的物质的量浓度大得多 |


科目:高中化学 来源: 题型:
| A、保存液溴时,上层用水液封并装在带橡胶塞的试剂瓶中 |
| B、在蒸发皿中加热Na2CO3?10H2O使其脱水 |
| C、用酸式滴定管量取6.55mL的KMnO4溶液 |
| D、用分液漏斗分离溴乙烷与氢氧化钠溶液发生反应后的生成物 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、1% | B、2% | C、3% | D、4% |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、①②③ | B、②④⑤ |
| C、①③⑥ | D、①②⑤ |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、碘升华 |
| B、NaCl的晶体加热熔化 |
| C、加热NH4HCO3分解 |
| D、HCl溶于水 |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| 温度 | 27℃ | 2000℃ |
| K值 | 3.84×10-31 | 0.1 |
| 温度 | 25℃ | 350℃ | 400℃ | 450℃ |
| K值 | 5×108 | 1.847 | 0.507 | 0.152 |
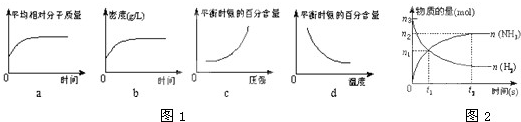
查看答案和解析>>
科目:高中化学 来源: 题型:
| ||
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com