
| A. | HCl、HBr、HI的熔、沸点依次升高与分子间作用力大小有关 | |
| B. | H2O的熔、沸点高于H2S是由于H2O分子之间存在氢键 | |
| C. | I2易溶于CCl4可以用相似相溶原理解释 | |
| D. | 甲烷可与水形成氢键这种化学键 |
分析 A、HCl、HBr、HI都是分子晶体,所以熔、沸点依次升高与分子间作用力有关;
B、氢键是比范德华力大的一种分子间作用力;
C、极性分子易溶于极性分子组成的溶剂,非极性分子组成的溶质易溶于非极性分子组成的溶剂;
D、与电负性很大的原子形成共价键的氢原子与另一个电负性很大的原子之间的作用力为氢键.
解答 解:A、HCl、HBr、HI都是分子晶体,所以熔、沸点依次升高与分子间作用力有关,故A正确;
B、氢键是比范德华力大的一种分子间作用力,水分子间可以形成氢键,H2S分子间不能形成氢键,因此H2O的熔、沸点高于H2S,故B正确;
C、碘是非极性分子易溶于非极性溶剂四氯化碳,甲烷属于非极性分子难溶于极性溶剂水,所以都可用相似相溶原理解释,故C正确;
D、甲烷中C原子电负性不大,所以甲烷分子和水分子之间不能形成氢键,并且氢键不是化学键,是分子间作用力,故D错误.
故选:D.
点评 本题考查氢键对物质性质的影响以及不同晶体中影响物质熔沸点的因素,综合性较强,首先判断属于何种晶体,然后再根据同种晶体中粒子作用力的差异进行判断.


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:解答题
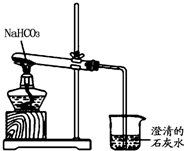 Na2CO3和NaHCO3是两种常见的钠盐.
Na2CO3和NaHCO3是两种常见的钠盐.查看答案和解析>>
科目:高中化学 来源: 题型:解答题

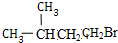 +NaOH$→_{△}^{乙醇}$
+NaOH$→_{△}^{乙醇}$ +NaBr+H2O;
+NaBr+H2O; +HBr$\stackrel{△}{→}$
+HBr$\stackrel{△}{→}$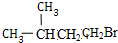 +H2O;
+H2O; ;
; 和
和 ;
;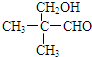 .
.查看答案和解析>>
科目:高中化学 来源: 题型:实验题
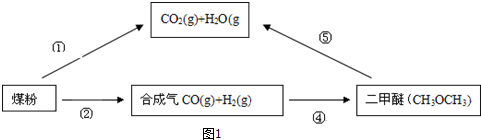
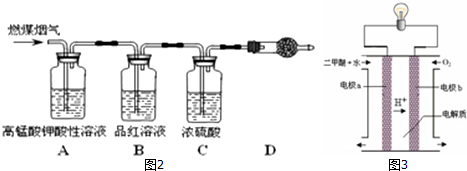
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ①④ | B. | ②⑤ | C. | ②③④⑤ | D. | ①②③④ |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
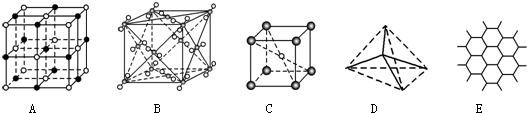
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 阳光通过门缝有光亮通路 | |
| B. | 一支钢笔使两种不同牌号的墨水,容易出现堵塞 | |
| C. | 向氯化铁溶液中加 NaOH溶液,会出现红褐色沉淀 | |
| D. | 在河水与海水的交界处,易形成三角洲 |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
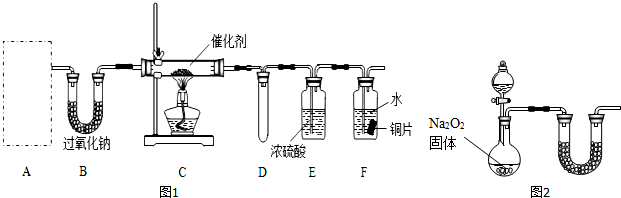
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com