
【题目】次氯酸溶液是常用的消毒剂和漂白剂。某学习小组根据需要欲制备浓度不小于0.8mol/L的次氯酸溶液。
资料1:常温常压下,Cl2O为棕黄色气体,沸点为3.8℃,42 ℃以上会分解生成Cl2和O2,Cl2O易溶于水并与水立即反应生成 HClO。
资料2:将氯气和空气(不参与反应)按体积比1∶3混合通入潮湿的碳酸钠中发生反应2Cl2+2Na2CO3+H2O=Cl2O+2NaCl+2NaHCO3,用水吸收Cl2O(不含Cl2)制得次氯酸溶液。
(装置及实验)用以下装置制备次氯酸溶液。
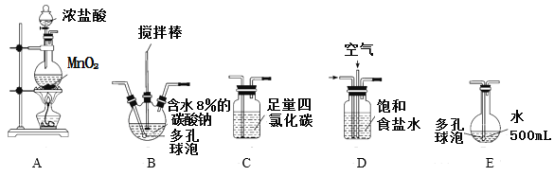
回答下列问题:
(1)各装置的连接顺序为_____→_____→_____→____→E。
(2)装置A中反应的离子方程式是__________________________。
(3)实验中控制氯气与空气体积比的方法是_____________________。
(4)反应过程中,装置B需放在冷水中,其目的是_________________________。
(5)装置E采用棕色圆底烧瓶是因为______________________。
(6)若装置B中生成的Cl2O气体有20%滞留在E前各装置中,其余均溶于装置E的水中,装置E所得500mL次氯酸溶液浓度为0.8mol/L,则至少需要含水8%的碳酸钠的质量为_________g。
(7)已知次氯酸可被H2O2、FeCl2等物质还原成Cl-。测定E中次氯酸溶液的物质的量浓度的实验方案为:用________________准确量取20.00 mL次氯酸溶液,加入足量的________溶液,再加入足量的________溶液,过滤,洗涤,真空干燥,称量沉淀的质量。(可选用的试剂:H2O2溶液、FeCl2溶液、AgNO3溶液。)
【答案】A D B C MnO2 + 4H++2Cl- ![]() Mn2++ Cl2 ↑+ 2H2O 通过观察B中产生气泡的速率调节流速 防止反应放热后温度过高导致 Cl2O 分解 HClO见光易分解 57.6 酸式滴定管 H2O2 AgNO3
Mn2++ Cl2 ↑+ 2H2O 通过观察B中产生气泡的速率调节流速 防止反应放热后温度过高导致 Cl2O 分解 HClO见光易分解 57.6 酸式滴定管 H2O2 AgNO3
【解析】
A装置用二氧化锰和浓盐酸制备氯气,由D装置饱和食盐水吸收氯气中的氯化氢气体,与空气形成1:3的混合气体通入B装置,发生反应2Cl2+2Na2CO3+H2O=Cl2O+2NaCl+2NaHCO3,防止反应放热后温度过高导致Cl2O分解,装置B需放在冷水中,在搅拌棒的作用下与含水8%的碳酸钠充分反应制备Cl2O,通入C装置吸收除去Cl2O中的Cl2,并在E装置中用水吸收Cl2O制备次氯酸溶液,据此分析作答。
(1)A装置制备氯气,D装置吸收吸收氯气中的氯化氢气体,与空气形成1:3的混合气体通入B装置,与含水8%的碳酸钠充分反应制备Cl2O,C装置吸收除去Cl2O中的Cl2,E装置中用水吸收Cl2O制备次氯酸溶液,所以各装置的连接顺序为A→D→B→C→E;
(2)二氧化锰与浓盐酸在加热条件下反应生成氯气,反应方程式为:MnO2+4HCl(浓)![]() MnCl2+Cl2↑+2H2O,对应离子方程式为:MnO2+4H++2Cl-
MnCl2+Cl2↑+2H2O,对应离子方程式为:MnO2+4H++2Cl-![]() Mn2++Cl2↑+2H2O;
Mn2++Cl2↑+2H2O;
(3)将氯气和空气(不参与反应)以体积比约1:3混合通入含水8%的碳酸钠中制备Cl2O,可通过观察A中产生气泡的速率调节流速,从而控制氯气与空气体积比;
(4)由题可知:Cl2O42℃以上会分解生成Cl2和O2,故为防止反应放热后温度过高导致Cl2O分解,装置B需放在冷水中;
(5)装置C中使用棕色平底烧瓶可以避光,防止反应生成的HClO见光分解;
(6)装置E所得500mL次氯酸溶液浓度为0.8mol/L,n=cv=0.5mol×0.8mol/L=0.4mol,Cl2O+H2O![]() 2HClO,反应的二氧化氯为0.2mol,装置B中生成的Cl2O气体有20%滞留在E前各装置中,制得的二氧化氯的物质的量为
2HClO,反应的二氧化氯为0.2mol,装置B中生成的Cl2O气体有20%滞留在E前各装置中,制得的二氧化氯的物质的量为![]() =0.25mol,2Cl2+2Na2CO3+H2O=Cl2O+2NaCl+2NaHCO3,需碳酸钠的物质的量为0.5mol,质量为0.5mol×106g/mol=53g,则至少需要含水8%的碳酸钠的质量为
=0.25mol,2Cl2+2Na2CO3+H2O=Cl2O+2NaCl+2NaHCO3,需碳酸钠的物质的量为0.5mol,质量为0.5mol×106g/mol=53g,则至少需要含水8%的碳酸钠的质量为![]() ≈57.6g;
≈57.6g;
(7)次氯酸具有酸性和强氧化性,需要选用酸式滴定管盛放;FeCl2溶液中含有氯离子,本实验中需要用硝酸银溶液测定氯离子,干扰了检验结果,故应该选用双氧水,具体实验操作方法是:用酸性滴定管准确量取20.00mL次氯酸溶液,加入足量的H2O2溶液,再加入足量的AgNO3溶液,过滤,洗涤沉淀,在真空干燥箱中干燥,用电子天平称量沉淀质量。


 每课必练系列答案
每课必练系列答案 巧学巧练系列答案
巧学巧练系列答案科目:高中化学 来源: 题型:
【题目】探究氢氧化铝的两性,最适宜的试剂是( )
A.AlCl3、氨水、稀盐酸B.![]() 、氨水、稀盐酸
、氨水、稀盐酸
C.Al、NaOH溶液、稀盐酸D.![]() 溶液、NaOH溶液、稀盐酸
溶液、NaOH溶液、稀盐酸
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】I碘是人类发现的第二个生命科学必需微量元素。回答下列问题:
(1)碘在元素周期表的位置为______________;HF的沸点比HI_________(填“高”或“低”)。原因是_____________________________
(2)自然界中的碘有的以NaIO3形态存在于硝石(NaNO3)中,向硝石母液中加入NaHSO3可以制得I2,请写出NaIO3溶液和NaHSO3溶液反应的离子方程式___________________。
II:2019年有科学家发表在《自然》科学杂志上的研究认为:细菌和灵长类动物铁元素争夺战是物种存活的一个决定性因素。请结合你所学的知识回答下列问题:
(1)铁(26号元素)的原子结构示意图为_______________________
(2)写出氢氧化亚铁接触空气变色过程中发生的化学方程式_________________________
(3)Na2FeO4是新型水处理剂,简述其在水处理中的作用和原因_______________________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】设NA为阿伏加德罗常数的值,下列说法正确的是
A. 18g氨基(-ND2)中含有的电子数为10NA
B. 一定质量的乙烷与22.4L(标准状况)Cl2在光照条件下发生取代反应,形成C-Cl键的数目为2NA
C. 用惰性电极电解100mL0.1mol·L-1的CuSO4溶液,当阴、阳两极产生相同条件下等体积的气体时,电路中转移电子数为0.04NA
D. n(H2SO3)和n(HSO3-)之和为1mol的KHSO3溶液中,含有的K+数目为NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】以“物质的量”为中心的计算是化学计算的基础,下列与“物质的量”相关的计算正确的是( )
A. 现有CO、CO2、O3三种气体,它们分别都含有1 mol O,则三种气体的物质的量之比为3∶2∶1
B. 28 g CO和22.4 L CO2中含有的碳原子数一定相等
C. 标准状况下,11.2 L X气体分子的质量为16 g,则X气体的摩尔质量是32
D. a g Cl2中有b个氯原子,则阿伏加德罗常数NA的数值可表示为![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】工业上采用酸性高浓度含砷废水(砷主要以亚砷酸H3AsO3形式存在)提取中药药剂As2O3。工艺流程如下:
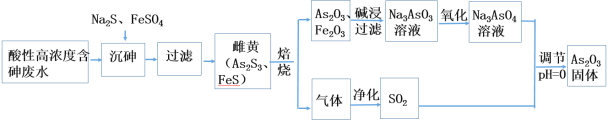
回答下列问题:
(1)已知砷元素与N同一主族,原子比N原子多两个电子层,则砷元素的原子序数为________,“沉砷”中所用Na2S的电子式为_____________。
(2)已知:As2S3与过量的S2-存在以下反应:As2S3(s)+3S2-(aq) ![]() 2AsS33- ;“沉砷”中FeSO4的作用是___________________________。
2AsS33- ;“沉砷”中FeSO4的作用是___________________________。
(3)“焙烧”过程中由于条件的原因,生成的三氧化二铁中混有四氧化三铁,证明四氧化三铁存在的试剂是_________________________________。(写名称)
(4)调节pH=0时,由Na3AsO4制备As2O3的离子方程式为:_______________。
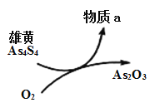
(5)一定条件下,用雄黄(As4S4)制备As2O3的转化关系如图所示。若反应中,1molAs4S4(其中As元素的化合价为+2价)参加反应时,转移28mole-,则物质a为___________。(填化学式)
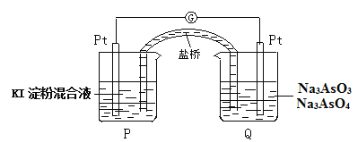
(6)某原电池装置如图,电池总反应为:AsO43-+2I-+H2O![]() AsO33-+I2+2OH-。当P池中溶液由无色变成蓝色时,正极上的电极反应式为____________________________。一段时间后电流计指针不发生偏转。欲使指针偏转方向与起始时相反,可采取的措施是____________(举一例)。
AsO33-+I2+2OH-。当P池中溶液由无色变成蓝色时,正极上的电极反应式为____________________________。一段时间后电流计指针不发生偏转。欲使指针偏转方向与起始时相反,可采取的措施是____________(举一例)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知在101kPa、25℃条件下,2 mol氢气完全燃烧生成水蒸气放出484kJ的热量,下列热化学方程式正确的是( )
A.H2O(g)=H2(g)+![]() O2(l) △H=+242kJ/mol
O2(l) △H=+242kJ/mol
B.2H2 (g)+O2(g)=2H2O(l) △H=-484kJ/mol
C.H2(g)+![]() O2(g)=H2O(g) △H=-242kJ/mol
O2(g)=H2O(g) △H=-242kJ/mol
D.2H2(g)+O2(g)=2H2O(g) △H=+484kJ/mol
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图装置所示,C、D、E、F、X、Y都是惰性电极,甲、乙中溶液的体积和浓度都相同(假设通电前后溶液体积不变),A、B为外接直流电源的两极。将直流电源接通后,F极附近呈红色。
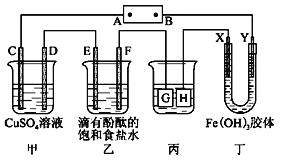
请回答:(1)B极是电源的___极,电极C的电极反应式为:___。
(2)若C、D、E、F电极均只有一种单质生成时,对应单质的物质的量之比为___。
(3)现用丙装置给铜件镀银,则H电极材料是___(填“铜”或“银”),电镀液是___溶液。当乙中溶液的pH是13时(此时乙溶液体积为500mL),丙中镀件上析出银的质量为___。
(4)一段时间后,丁中X极附近的颜色逐渐变浅,Y极附近的颜色逐渐变深,这表明__在电场作用下向Y极移动。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】Ⅰ.现有下列几种物质:①盐酸 ②石墨 ③酒精 ④SO2 ⑤熔融KHSO4 ⑥Ba(OH)2固体 ⑦氨水⑧硝酸
(1)属于强电解质的有_____________;属于非电解质的有_____________。(填序号)
(2)⑧和铜在一定条件下可发生如下反应:3Cu+8HNO3(稀)=3Cu(NO3)2+2NO↑+4H2O,酸性介质与氧化剂的物质的量之比为________;请用双线桥法分析电子转移方向和数目_______。
Ⅱ.向Ba(OH)2溶液中逐滴加入稀硫酸,请完成下列问题:
(1)写出反应的离子方程式__________________________________________________ 。
(2)下列三种情况下,离子方程式与(1)相同的是______(填字母)。
A.向NaHSO4溶液中,逐滴加入Ba(OH)2溶液至溶液显中性
B.向NaHSO4溶液中,逐滴加入Ba(OH)2溶液至SO42-恰好完全沉淀
C.向NaHSO4溶液中,逐滴加入Ba(OH)2溶液至过量
(3)若缓缓加入稀硫酸至过量,整个过程中混合溶液的导电能力(用电流强度I表示)可近似地用下图中的______曲线表示(填字母)。

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com