
| A. | 甲的分子数比乙的分子数多 | |
| B. | 甲的物质的量比乙的物质的量少 | |
| C. | 甲的密度比乙的密度小 | |
| D. | 甲的相对分子质量比乙的相对分子质量大 |
分析 同温同压下,气体摩尔体积相等,体积甲<乙,则物质的量:甲<乙,二者质量相同,要使其物质的量相对,则摩尔质量乙<甲,结合N=nNA、ρ=$\frac{M}{{V}_{m}}$及摩尔质量与相对分子质量的关系分析解答.
解答 解:同温同压下,气体摩尔体积相等,体积甲<乙,则物质的量:甲<乙,二者质量相同,要使其物质的量相对,则摩尔质量乙<甲,
A.根据N=nNA知,分子数与物质的量成正比,物质的量甲<乙,所以其分子数甲<乙,故A错误;
B.同温同压下,气体摩尔体积相等,体积甲<乙,则物质的量:甲<乙,故B正确;
C.根据ρ=$\frac{M}{{V}_{m}}$知,相同条件下,气体密度与摩尔质量成正比,摩尔质量甲>乙,则密度甲>乙,故C错误;
D.摩尔质量在数值上等于其相对分子质量,摩尔质量甲>乙,所以甲的相对分子质量比乙的相对分子质量大,故D正确;
故选BD.
点评 本题考查阿伏伽德罗定律及其推论,明确物质的量公式中各个物理量的关系是解本题关键,易错选项是C,注意相同条件下摩尔质量与密度关系,题目难度不大.


 世纪百通期末金卷系列答案
世纪百通期末金卷系列答案科目:高中化学 来源: 题型:选择题
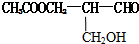 具有光学活性,当它发生下列反应后生成的有机物仍然一定具有光学活性的是( )
具有光学活性,当它发生下列反应后生成的有机物仍然一定具有光学活性的是( )| A. | 与甲酸发生酯化反应 | B. | 与NaOH溶液共热 | ||
| C. | 与氧气发生催化氧化 | D. | 在催化剂存在下与H2作用 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 第ⅠA族元素铯的两种位素${\;}_{\;}^{137}$Cs比${\;}_{\;}^{133}$Cs多4个质子 | |
| B. | 第ⅦA族元素从上到下,其氢化物的还原性逐渐减弱 | |
| C. | 同主族元素原子半径越大,单质的熔点越高 | |
| D. | 同周期元素(除0族元素外)从左到右,简单阴离子半径逐渐减小 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 加入少量MgCl2固体 | B. | 继续加水 | ||
| C. | 加入少量Na2CO3固体 | D. | 升高温度 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | 甲烷的燃烧热为-890.3kJ•mol-1,则甲烷燃烧的热化学方程式可表示为:CH4(g)+2O2(g)=CO2(g)+2H2O(l)△H=-890.3kJ•mol-1 | |
| B. | 500℃、30MPa下,将0.5mol N2和1.5molH2置于密闭的容器中充分反应生成NH3(g),放热19.3kJ,其热化学方程式为: N2(g)+3H2(g)$?_{500℃、30MPa}^{催化剂}$ 2NH3(g)△H=-38.6kJ•mol-1 | |
| C. | 硫酸与氢氧化钡发生中和反应的热化学方程式为:H+(aq)+SO42-(aq)+Ba2+(aq)+OH-(aq)=BaSO4(s)+H2O(l)△H=-57.3kJ•mol-1 | |
| D. | 氯化镁溶液与氨水反应:Mg2++2NH3•H2O=Mg(OH)2↓+2NH4+ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 常温下,0.1mol•L-1的NH4NO3溶液中氮原子数为0.2NA | |
| B. | 标准状况下,5.6L CCl4含有的分子数为0.25 NA | |
| C. | 在标准状况下,2.8g N2和2.24LCO所含质子数均为1.4NA | |
| D. | 常温下,1 L pH=1的硫酸溶液中含有的H+数为0.05NA |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com