
【题目】在强酸性溶液中能大量共存的无色透明离子组是( )
A.K+、Na+、NO3-、MnO4-B.Mg2+、Na+、Cl-、SO42-
C.K+、Na+、Br-、Cu2+D.Na+、Ba2+、OH-、SO42-
科目:高中化学 来源: 题型:
【题目】设NA表示阿伏加德罗常数,下列叙述不正确的是
A. 通常状况下,1 mol SO3含有的分子数为NA
B. 1 mol OH-参与电解,转移的电子数目为NA
C. 标准状况下,含NA个氩原子的氩气体积约为22.4 L
D. 标准状况下,V L水含有的氧原子数约为VNA/22.4
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】元素周期表的形式多种多样,下图是扇形元素周期表的一部分(1-36号元素),对比中学常见元素周期表,思考扇形元素周期表的填充规律,并回答下列问题:

(1) D代表的元素处于常见元素周期表的位置是第 _____ 周期________ 族。
(2)元素F、G、I、K、M的原子半径由大到小的顺序是___________________(用元素符号表示)。
(3)B、F、G三种元素三种元素最高价氧化物对应水化物碱性最强的碱是_________(填化学式)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列各溶液中的反应,不论反应物量的多少,都只能用同一个离子方程式来表示的是
A.FeBr2与Cl2B.Ba(OH)2与CO2
C.HCl与Na2CO3D.AlCl3与氨水
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】能正确表示下列反应的离子方程式是
A. NaNO2溶液与酸性KMnO4溶液:2MnO4﹣+5NO2﹣+6H+═2Mn2++5NO3﹣+3H2O
B. 碳酸氢铵溶液与足量氢氧化钡溶液:NH4++HCO3﹣+2OH﹣═CO32﹣+NH3H2O+H2O
C. Fe(NO3)3溶液中加入过量的HI溶液:2Fe3++2I﹣═2Fe2++I2
D. 用惰性电极电解氯化钠溶液:2Cl﹣+2H2O═Cl2↑+H2↑+2OH﹣
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下表中物质的分类全部正确的一组是
单质 | 氧化物 | 盐 | 混合物 | |
A | 臭氧 | 氯化氢 | 小苏打 | 漂白粉 |
B | 水银 | 氧化钠 | 纯碱 | 生理盐水 |
C | 溴水 | 水 | 硫酸钡 | 空气 |
D | 硫粉 | 干冰 | 氯化铵 | 冰水混合物 |
A.AB.BC.CD.D
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列各组离子能够大量共存且溶液呈无色的是
A.H+、Ag+、Cl-、SO42-B.Mg2+、Al3+、OH-、SO42-
C.K+、Na+、Cl-、CO32-D.NH4+、MnO4-、Na+、NO3-
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】电池在我们的生活中有着重要的应用,请回答下列问题:
(1)为了验证Fe2+与Cu2+氧化性强弱,下列装置能达到实验目的的是______(填序号),写出正极的电极反应式_______。若构建原电池时两个电极的质量相等,当导线中通过0.05mol电子时,两个电极的质量差为________。
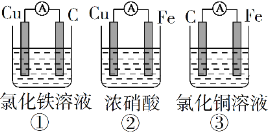
(2)将CH4设计成燃料电池,其利用率更高,装置如图所示(A、B为多孔碳棒)。
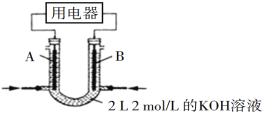
实验测得OH定问移向B电极,则_____(填“A”或“B”)处电极入口通甲烷,其电极反应式为___________。当消耗甲院的体积为33.6 L(标准状况下)时,假设电池的能量转化率为80%,则导线中转移电子的物质的量为________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知某“84消毒液”瓶体部分标签如图所示,该“84消毒液”通常稀释100倍(体积之比)后使用。请回答下列问题:
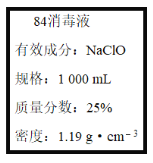
(1)某同学取100 mL该“84消毒液”,稀释后用于消毒,稀释后的溶液中c(Na+)=____mol·L-1。
(2)该同学参阅该“84消毒液”的配方,欲用NaClO固体配制480 mL含NaClO质量分数为25%的消毒液。下列说法正确的是____(填字母)。
a.如图所示的仪器中,有三种是不需要的,还需要一种玻璃仪器
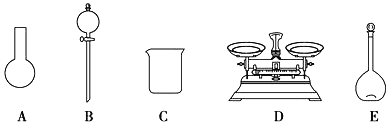
b.容量瓶用蒸馏水洗净后,应烘干后才能用于溶液配制
c.配制过程中,未用蒸馏水洗涤烧杯和玻璃棒可能导致结果偏低
d.需要称量NaClO固体的质量为143.0 g
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com