
����Ŀ��������ѧ֪ʶ���ش��������⣺
(1)��������(Na2FeO4)����Ϊ��Ч�����ˮ����������Ħ��������__________���������ƿ���ˮ��Ӧ����Fe(OH)3���塢�������ƺ�������д����Ӧ�����ӷ���ʽ��_____________��
(2)��άͨ����ⷨ�����Ƶ��˽����ƣ����ʮ���ڣ���ҵ�ϲ������ۺ��������Ƹ������ڵķ����Ƶ���������ͬʱ���Fe3O4��������д���÷�Ӧ�Ļ�ѧ����ʽ_____________���÷�Ӧ�����ڵ���ʵ��������������������________________���ѧʽ�������Ƶ�22.4L(����Ϊ��״����)��������ת�Ƶ��ӵ���ĿΪ________________��
(3)Ư�۳�������ˮ����ˮ����й�P����Ⱦ�Ļ�������������Ҫ�ɷ����Ȼ��ƺʹ������[Ca(ClO)2]����Ч�ɷ�Ϊ������ơ�Ϊ���ijƯ�۵���Ч�ɷֺ�������ȡA gƯ����Ʒ�ܽ⣬��������Һ��ͨ��CO2�����ٲ�������Ϊֹ����Ӧ�Ļ�ѧ����ʽΪCa(ClO)2+CO2+H2O=CaCO3��+2HClO������Ӧ���ɴ�����(HClO)�����ʵ���ΪKmol�����Ư������Ч�ɷֵ���������Ϊ___________%���ú�A��K��ʽ�ӱ�ʾ����
���𰸡�166g/mol 4FeO42-+10H2O=4Fe(OH)3(����)+8OH-+3O2�� 3Fe+4NaOH=4Na��+Fe3O4+2H2�� NaOH 2NA��1.204��1024 ![]()
��������
(1)Ħ��������g/molΪ��λ����ֵ�ϵ�������Է������������ݵ���ת���غ㡢����غ㡢ԭ���غ���ƽ��д���ӷ���ʽ��
(2)�������֪��Fe��NaOH�ڸ�������������Na������Fe3O4��H2����ƽ��д��ѧ����ʽ����Ӧ�����ڵ���ʵ��������������������NaOH����Ӧ��Na��HԪ�ػ��ϼ۽��ͣ����ݷ���ʽ����������������������NaԪ�ء�HԪ�ػ��ϼ۱仯����ת�Ƶ�����Ŀ��
(3)����HClO��������Ca(ClO)2���������ٸ������������Ķ���ʽ���㡣
(1)Na2FeO4����Է�������Ϊ166������Ħ������Ϊ166g/mol���������ƿ���ˮ��Ӧ����Fe(OH)3���塢�������ƺ���������Ӧ�����ӷ���ʽ��4FeO42-+10H2O=4Fe(OH)3(����)+8OH-+3O2����
(2)�������֪��Fe��NaOH�ڸ�������������Na������Fe3O4��H2����Ӧ����ʽΪ��3Fe+4NaOH![]() 4Na��+Fe3O4+2H2������Ӧ�����ڵ���ʵ��������������������NaOH��Na�����ʵ���n(Na)=224L��22.4L/mol=1mol���ɷ���ʽ��֪��������Ϊ1mol��
4Na��+Fe3O4+2H2������Ӧ�����ڵ���ʵ��������������������NaOH��Na�����ʵ���n(Na)=224L��22.4L/mol=1mol���ɷ���ʽ��֪��������Ϊ1mol��![]() =0.5mol����ת�Ƶ��ӵ����ʵ���n(e-)=1mol��1+0.5mol��2=2mol����ת�Ƶ�����ĿN(e-)=2mol��NA/mol=2mol��(6.02��1023mol-1)=1.204��1024��
=0.5mol����ת�Ƶ��ӵ����ʵ���n(e-)=1mol��1+0.5mol��2=2mol����ת�Ƶ�����ĿN(e-)=2mol��NA/mol=2mol��(6.02��1023mol-1)=1.204��1024��
(3)��Ca(ClO)2+CO2+H2O=CaCO3��+2HClO��֪��n[Ca(ClO)2]=![]() n(HClO)=
n(HClO)=![]() ��Kmol=0.5Kmol�����Ư������Ч�ɷֵ���������
��Kmol=0.5Kmol�����Ư������Ч�ɷֵ���������![]() ��100%=
��100%=![]() %��
%��



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��һ�����ںϳ�����������ҩ������ʣ���ṹ��ͼ��ʾ������X��Y��Z��Q��WΪ1~20��Ԫ����ԭ��������������Z��Qͬ���壬Q��W�ļ����Ӿ�����ͬ�ĵ��Ӳ�ṹ������������ȷ���ǣ� ��
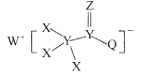
A.WX�ǹ��ۻ�����
B.ԭ�Ӱ뾶��W>Z>Y
C.����������Ӧ��ˮ��������ԣ�Q<Y
D.Z��X��Y��W��Q���γ��������ֶ�Ԫ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������£���50mL����0.1molCl2����ˮ�еμ�2mol��L-1��NaOH��Һ���õ���ҺpH������NaOH��Һ����ı仯ͼ����ͼ��ʾ������˵����ȷ���ǣ� ��
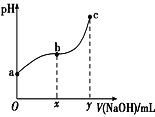
A.a����Һ�д��ڣ�N(HClO)+N(Cl-)+N(ClO-)=0.2NA(N��ʾ������������������a����Һ��Ư������������Һ�м���̼��ƹ���
B.��a��pH=4����c(Cl��)=m��c(ClO-)����Ka(HClO)=![]()
C.b��c�Σ���NaOH��Һ�ĵ��룬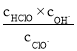 ������
������
D.��y=200����c���Ӧ��Һ�У�c(HClO)+c(H+)=c(OH-)��2c(Cl-)
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ͼ�Ǽ��ֳ����л���֮���ת����ϵͼ��AΪ����ҽ������ҩƷ��C����Ũ����ζ��
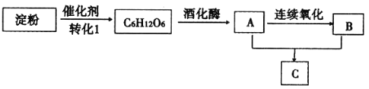
����������Ϣ�������ʵ�ת����ϵ��������и��⣺
��1��A�Ľṹ��ʽΪ_____��д����ҵ������ϩ����A�Ļ�ѧ����ʽ_________��
��2��B�Ĺ���������Ϊ______��
��3��A+B��C�Ļ�ѧ����ʽΪ______����Ӧ����Ϊ��Ӧ_______��
��4������˵����ȷ����_____
a.��ͼ������ֻ��C6H12O6��������
b.ת��1�������������
c.����C������֬
d.����A��B�������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������ͼ��ʾװ�ý���ʵ�飬���ж�ʵ������Ľ��Ͳ���������

ѡ�� | ���Լ� | �������� | ���� |
A | Ʒ����Һ | ��Һ��ɫ | SO2����Ư���� |
B | Na2SiO3��Һ | ������״���� | ���ԣ� H2SO3 ��H2SiO3 |
C | ����KMnO4��Һ | ��ɫ��ȥ | SO2���л�ԭ�� |
D | Ba(NO3)2��Һ | ���ɰ�ɫ���� | SO32����Ba2������ ��ɫBaSO3���� |
A.AB.BC.CD.D
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ʵ�����Ʊ�������ʱ���������ƻ��ᡢ������Ӧ(50~60��)��ϴ�ӷ��롢��������Ȳ��裬����ͼʾװ�ú�ԭ���ܴﵽĿ�ĵ�
A. ���ƻ��� B. ������Ӧ
B. ������Ӧ
C. ���������� D. ����������
D. ����������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������������Ϣ�ϳɺ���Ԫ���л�������N��·����ͼ��
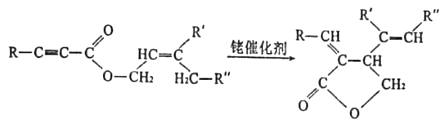
(R��R����R����ʾ�⡢�����)
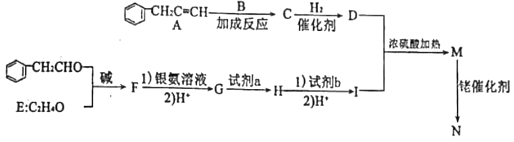
��֪��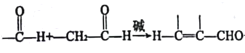 +H2O��B��Eͬϵ�����ʺɱ���30
+H2O��B��Eͬϵ�����ʺɱ���30
��ش��������⣺
��1���л���A��ϵͳ����___��
��2��C��D��Ϊ�����ʹ���D�к��й�����������___��
��3�����ʵ�飬д������F�����������ŵķ���___��
��4���Լ�a��___��H��I�����Լ�b�ķ�Ӧ����ʽΪ___��
��5��д��������������G�����У�����G��ͬ���칹����___��
����G������ͬ�Ĺ����Ţڱ��������������ȡ����
��6��д��N�Ľṹ��ʽ___��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ijͬѧΪ̽������Һ��ķ�Ӧ�����������ͼ��ʾʵ��װ�ý��С�
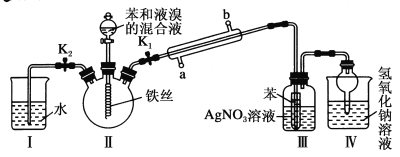
�ش��������⣺
(1)�����ܵĽ�ˮ����________(�a����b��)��
(2)�ر�K2������K1�ͷ�Һ©���������μӱ���Һ��Ļ��Һ����Ӧ��ʼ��װ�â���С�Թ��ڱ���������______________��
(3)��ʵ���ܷ�֤������Һ�巢����ȡ����Ӧ��_____(��ܡ����ܡ�)��������______��
(4)��Ӧ�����ر�K1�ͷ�Һ©����������K2����ʱװ�â��е�ˮ������װ�â��У�����������Ŀ����_____________��
(5)���������ƿ�ڵ�Һ�����ν�������ʵ������Ϳɵõ��ϴ������屽��
a��������ˮϴ�ӣ�����Һ��
b����5%��NaOH��Һϴ�ӣ�����Һ��
c��������ˮϴ�ӣ�����Һ��
d��������ˮCaCl2��ĩ���
e��________(���������)��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������ܱ��ʼ�����һ�ֿ����ӳ����ڵ��Լ��������500mL���ʻ����ʼ����к��еijɷ֣��Ķ���ش��������⣺
�ɷ� | ����(g) | Ħ������(gmol1) |
���� | 25.00 | 342 |
����� | 0.87 | 174 |
��˾ƥ�� | 0.17 | 180 |
������� | 0.316 | 158 |
������ | 0.0075 | 170 |
(1)���������ܱ��ʼ����ijɷ��У����ڷǵ���ʵ���______������ɱ��������____
A. �������B. �����C. ����D. ������E. ˮ
(2) ����1L�������ʻ����ʼ�����Ҫ�������______mol��
(3)����Һ���ƹ����У����в�����ʹ���ƽ����Ӱ�����______��
A.����ʱ��������ƿ�̶���
B.����ƿ��ʹ��ǰδ�����������������ˮ
C.����ƿ��ʹ��ǰ��������һ�����ʵ���Ũ�ȵ��Ȼ�����Һδϴ��
D.����ҡ�Ⱥ���Һ���������ƿ�Ŀ̶��ߣ���δ���κδ���
(4)���ʻ����ʼ�����K+(��˾ƥ���в���K+)�����ʵ���Ũ��Ϊ______mol/L��
(5)����ø�����أ�K2FeO4������������Ч������ã�ʪ���Ʊ�������صķ�Ӧ��ϵ������������Fe(OH)3��ClO-��OH-��FeO42-��Cl-��H2O.���������£��������뻹ԭ�������ʵ����ı�Ϊ3:2������Ӧ��д������ƽʪ���Ʊ�������ص����ӷ�Ӧ����ʽ___________________________________________________________
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com