
| A�� | �����������������ٷ����仯ʱ��˵����Ӧ�ﵽƽ��״̬ | |
| B�� | ��M��ʾ�˷�Ӧ������0.1 amol•��L•min��-1 | |
| C�� | ��X��ʾ�˷�Ӧ�ķ�Ӧ�����ǣ�0.1-0.2 a��mol•��L•min��-1 | |
| D�� | ����������ѹǿ���ٷ����仯ʱ��˵����Ӧ�ﵽƽ��״̬ |
���� A���淴Ӧ���У���Ӧ��������������С�����������������䣬˵������ƽ�⣻
B��M�ǹ���Ũ����һ�����������Բ���M��ʾ��Ӧ���ʣ�
C���������ʵ����仯��֮�ȵ��ڻ�ѧ������֮�ȼ���X�����ʵ����仯�����ٸ���v=$\frac{\frac{��n}{V}}{��t}$���㣻
D����������ļ�������ȣ�����ѹǿʼ���Dz��������
��� �⣺A��WΪ���壬�淴Ӧ���У���Ӧ��������������С�����������������䣬˵������ƽ�⣬��A��ȷ��
B��M�ǹ���Ũ����һ�����������Բ���M��ʾ��Ӧ���ʣ���B����
C��5min��ﵽƽ�⣬����2amolZ����μӷ�Ӧ��X�����ʵ���Ϊ2amol��$\frac{1}{2}$=amol����v��X��=$\frac{\frac{amol}{2L}}{5min}$=0.1amol/��L•min������C����
D����������ļ�������ȣ�����ѹǿʼ���Dz�����������Բ�����ƽ��״̬�ı�־����D����
��ѡA��
���� ������Ҫ�����˻�ѧ��Ӧ���ʡ���ѧƽ��״̬�жϵȣ��ѶȲ���ע��Ի���֪ʶ���������գ�


 �Ķ��쳵ϵ�д�
�Ķ��쳵ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | PH3��NH3�ȶ� | |
| B�� | S2-�뾶��Cl-��С | |
| C�� | Na��Cs���ڵڢ�A��Ԫ�أ�Csʧ����������Naǿ | |
| D�� | �Ѽط����Ȼ��Ƶ�ˮ��Һ�п��Ƶý����� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | �ܢڢۢ٢� | B�� | �ޢ� | C�� | �ڢ٢� | D�� | �ޢߢ٢� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ԭ�Ӱ뾶�Ĵ�С˳��r��W����r��Z����r��Y����r��X�� | |
| B�� | X������������Ӧ��ˮ��������Ա�W���� | |
| C�� | Y����̬���⻯������ȶ��Ա�W��ǿ | |
| D�� | Y�ֱ���Z��W�γɵĻ������л�ѧ��������ͬ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A | B | C | D | |
| ���� | Fe | Fe | Cu | Cu |
| ���� | Cu | Cu | Fe | Fe |
| �������Һ | CuSO4 | H2SO4 | CuCl2 | �ƾ� |
| A�� | A | B�� | B | C�� | C | D�� | D |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
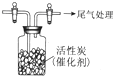 ijѧϰС���Ʋ�SO2����ǿ������Cl2��Ӧ����SO2Cl2��Ϊ�˽���̽����
ijѧϰС���Ʋ�SO2����ǿ������Cl2��Ӧ����SO2Cl2��Ϊ�˽���̽�����鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ������̼�ĵ���ʽ��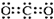 | B�� | 14C��ԭ�ӽṹʾ��ͼ�� | ||
| C�� | C3H8�ĽṹʽCH3-CH2-CH3 | D�� | ������ĵ���ʽ��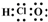 |
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com