
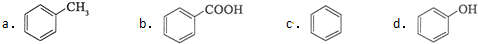
 $”ś_{H+}^{KMnO_{4}}$[B]$”ś_{ÅØĮņĖį£¬”÷}^{CH_{3}OH}$
$”ś_{H+}^{KMnO_{4}}$[B]$”ś_{ÅØĮņĖį£¬”÷}^{CH_{3}OH}$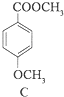
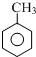 $\stackrel{KMnO_{4}£ØH+£©}{”ś}$
$\stackrel{KMnO_{4}£ØH+£©}{”ś}$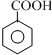
 £®
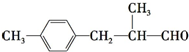
£®
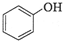
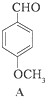
·ÖĪö £Ø1£©¢ŁōĒ»ł»ņĀ±Ō×ÓĮŚĪ»Ģ¼ÉĻÓŠĒāŌ×Ó£¬æÉŅŌ·¢ÉśĻūČ„·“Ó¦£»
¢Ś·ÓōĒ»łæÉŅŌ±»æÕĘųŃõ»Æ£»
¢Ū¼ģŃéC3H7BrÖŠäåŌŖĖŲ£¬Ó¦ĻČĖ®½ā£¬ŗó¼ÓĖįÖŠŗĶÖĮĖįŠŌ£¬Č»ŗó¼ÓĻõĖįŅųÉś³É°×É«³Įµķ£¬ŅŌ“ĖæÉČ·¶Øŗ¬äåŌŖĖŲ£»
£Ø2£©øł¾Ż×Ŗ»Æ¹ŲĻµ£¬A±»Ńõ»Æ£¬-CHO×Ŗ»ÆĪŖ-COOH£¬ĖłŅŌBĪŖ £¬B·¢Éśõ„»Æ·“Ӧɜ³É C£¬¾Ż“Ė“šĢā£»
£¬B·¢Éśõ„»Æ·“Ӧɜ³É C£¬¾Ż“Ė“šĢā£»
£Ø3£©øł¾ŻXµÄ½į¹¹¼ņŹ½æÉÖŖĘäÖŠĖłŗ¬ÓŠµÄŗ¬Ńõ¹ŁÄÜĶÅ£¬øł¾ŻXÖŠµÄ¹ŁÄÜĶÅæÉČ·¶ØÄÜ·¢Éś·“Ó¦µÄĄąŠĶ£®
½ā“š ½ā£ŗ£Ø1£©¢ŁōĒ»ł»ņĀ±Ō×ÓĮŚĪ»Ģ¼ÉĻÓŠĒāŌ×Ó£¬æÉŅŌ·¢ÉśĻūČ„·“Ó¦£¬
¹ŹŃ”bc£»
¢Ś·ÓōĒ»łæÉŅŌ±»æÕĘųŃõ»Æ£¬
¹ŹŃ”d£»
¢Ū¼ģŃéC3H7BrÖŠäåŌŖĖŲ£¬Ó¦ĻČĖ®½ā£¬ŗó¼ÓĖįÖŠŗĶÖĮĖįŠŌ£¬Č»ŗó¼ÓĻõĖįŅųÉś³É°×É«³Įµķ£¬ŅŌ“ĖæÉČ·¶Øŗ¬äåŌŖĖŲ£¬Ōņ¾ßĢåŹµŃé²½ÖčĪŖ¢ŪȔɣĮæøĆĀ±“śĢž£»¢Ż¼ÓČėNaOHČÜŅŗ£»¢Ł¼ÓČČ£»¢ŽĄäČ“£¬¢Ü¼ÓČėHNO3ŗóĖį»Æ£»¢Ś¼ÓČėAgNO3ČÜŅŗ£¬¼“ĪŖ¢Ū¢Ż¢Ł¢Ž¢Ü¢Ś£¬
¹Ź“š°øĪŖ£ŗ¢Ü¢Ś£»
£Ø2£©øł¾Ż×Ŗ»Æ¹ŲĻµ£¬A±»Ńõ»Æ£¬-CHO×Ŗ»ÆĪŖ-COOH£¬ĖłŅŌBĪŖ £¬B·¢Éśõ„»Æ·“Ӧɜ³É C£¬
£¬B·¢Éśõ„»Æ·“Ӧɜ³É C£¬
¢Łøł¾ŻCµÄ½į¹¹¼ņŹ½æÉÖŖ£¬CÖŠŗ¬Ńõ¹ŁÄÜĶŵÄĆū³ĘĪŖĆŃ¼üŗĶõ„»ł£¬
¹Ź“š°øĪŖ£ŗõ„»ł£»
¢Śøł¾ŻÉĻĆęµÄ·ÖĪöæÉÖŖ£¬BµÄ½į¹¹¼ņŹ½ĪŖ  £¬
£¬
¹Ź“š°øĪŖ£ŗ £»
£»
¢Ūøł¾ŻÉĻĆęµÄ·ÖĪöæÉÖŖ£¬B”śCµÄ·“Ó¦ĄąŠĶĪŖõ„»Æ·“Ó¦£¬
¹Ź“š°øĪŖ£ŗõ„»Æ·“Ó¦£»
£Ø3£©¢Łøł¾ŻXµÄ½į¹¹¼ņŹ½æÉÖŖĘäÖŠĖłŗ¬ÓŠµÄŗ¬Ńõ¹ŁÄÜĶÅĪŖČ©»ł£¬
¹Ź“š°øĪŖ£ŗČ©»ł£»
¢Śøł¾ŻXÖŠµÄ¹ŁÄÜĶÅæÉÖŖ£¬XÖŠŗ¬ÓŠČ©»ł£¬æÉ·¢Éś»¹Ō·“Ó¦”¢¼Ó³É·“Ó¦£¬²»ÄÜ·¢ÉśĻūČ„”¢õ„»Æ£¬
¹ŹŃ”b”¢c£®
µćĘĄ ±¾Ģāæ¼²éÓŠ»śĪļŗĻ³ÉÓėŠŌÖŹ£¬ĪŖøßĘµæ¼µć£¬Éę¼°Ķ¬·ÖŅģ¹¹Ģå¼°Ā±“śĢž”¢“¼”¢Č©”¢·Ó”¢ōČĖįŠŌÖŹµÄ漲飬°ŃĪÕ¹ŁÄÜĶÅÓėŠŌÖŹµÄ¹ŲĻµ¼“æɽā“š£¬ĢāÄæÄѶČÖŠµČ£®



| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
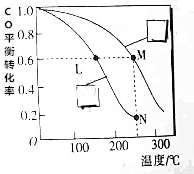 ÓĆĒāĘųŗĶŅ»Ńõ»ÆĢ¼æĖÖʱø½ą¾»ÄÜŌ“¶ž¼×ĆŃ£ØCH3OCH3£©£¬¹¤ŅµÖʱø¶ž¼×ĆŃŹ±ŌŚ“߻Ʒ“Ó¦ŹŅ£ØŃ¹ĒæĪŖ2.0”«10.0MPa£¬ĪĀ¶ČĪŖ230”«280”ę£©ÖŠ½ųŠŠĻĀĮŠ·“Ó¦£ŗ
ÓĆĒāĘųŗĶŅ»Ńõ»ÆĢ¼æĖÖʱø½ą¾»ÄÜŌ“¶ž¼×ĆŃ£ØCH3OCH3£©£¬¹¤ŅµÖʱø¶ž¼×ĆŃŹ±ŌŚ“߻Ʒ“Ó¦ŹŅ£ØŃ¹ĒæĪŖ2.0”«10.0MPa£¬ĪĀ¶ČĪŖ230”«280”ę£©ÖŠ½ųŠŠĻĀĮŠ·“Ó¦£ŗ²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
 »Æѧ¶ŌČĖĄąÉē»į½ų²½ŗĶ·¢Õ¹µÄ¹±Ļ×Ö®Ņ»ŹĒ·¢ĻÖŗĶŃŠÖĘĮĖø÷ÖÖ²ÄĮĻ£¬ĄżČē£¬½šŹō¾ĶŹĒĪŅĆĒÉś»īÖŠ²»æÉ»ņȱµÄÖŲŅŖ²ÄĮĻ£¬øł¾ŻÄćѧ¹żµÄÓŠ¹Ų½šŹōµÄÖŖŹ¶£¬»Ų“šĻĀĮŠĪŹĢā£ŗ
»Æѧ¶ŌČĖĄąÉē»į½ų²½ŗĶ·¢Õ¹µÄ¹±Ļ×Ö®Ņ»ŹĒ·¢ĻÖŗĶŃŠÖĘĮĖø÷ÖÖ²ÄĮĻ£¬ĄżČē£¬½šŹō¾ĶŹĒĪŅĆĒÉś»īÖŠ²»æÉ»ņȱµÄÖŲŅŖ²ÄĮĻ£¬øł¾ŻÄćѧ¹żµÄÓŠ¹Ų½šŹōµÄÖŖŹ¶£¬»Ų“šĻĀĮŠĪŹĢā£ŗ²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | ĻūČ„”ś¼Ó³É”śČ”“ś | B£® | ¼Ó³É”śĻūČ„”śČ”“ś | C£® | Č”“ś”śĻūČ„”ś¼Ó³É | D£® | ĻūČ„”ś¼Ó³É”śĻūČ„ |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā

| A£® | ×°ÖĆ¢ŁæÉÓĆÓŚ·ÖĄėI2ÓėNH4Cl»ģŗĻĪļ | |
| B£® | ×°ÖĆ¢ŚŹÕ¼Æ²¢²āĮæCuÓėÅØĮņĖį·“Ó¦²śÉśµÄĘųĢåµÄĢå»ż | |
| C£® | ×°ÖĆ¢ŪÖĘČ”ĀČĘų | |
| D£® | ×°ÖĆ¢ÜÖĘČ”ĪŽĖ®MgCl2 |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | NO2 | B£® | CO | C£® | C6H6£Øg£© | D£® | CO2 |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
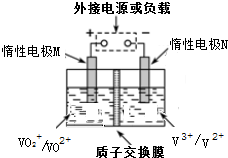 Č«·°ŅŗĮ÷“¢Äܵē³ŲŹĒŅŌČܽāÓŚŅ»¶ØÅضČĮņĖįČÜŅŗÖŠ²»Ķ¬¼ŪĢ¬·°Ąė×ÓµÄŃõ»Æ»¹Ō·“Ó¦Ą“ŹµĻÖ»ÆѧÄÜŗĶµēÄÜĻą»„×Ŗ»Æ£¬³äµēŹ±£¬¶čŠŌµē¼«M”¢N·Ö±šĮ¬½ÓµēŌ“µÄÕż¼«ŗĶøŗ¼«£®µē³Ų¹¤×÷ŌĄķČēĶ¼ĖłŹ¾£¬ĻĀĮŠĖµ·Ø²»ÕżČ·µÄŹĒ£Ø””””£©
Č«·°ŅŗĮ÷“¢Äܵē³ŲŹĒŅŌČܽāÓŚŅ»¶ØÅضČĮņĖįČÜŅŗÖŠ²»Ķ¬¼ŪĢ¬·°Ąė×ÓµÄŃõ»Æ»¹Ō·“Ó¦Ą“ŹµĻÖ»ÆѧÄÜŗĶµēÄÜĻą»„×Ŗ»Æ£¬³äµēŹ±£¬¶čŠŌµē¼«M”¢N·Ö±šĮ¬½ÓµēŌ“µÄÕż¼«ŗĶøŗ¼«£®µē³Ų¹¤×÷ŌĄķČēĶ¼ĖłŹ¾£¬ĻĀĮŠĖµ·Ø²»ÕżČ·µÄŹĒ£Ø””””£©| A£® | ·Åµē¹ż³ĢÖŠ£¬Mµē¼«·“Ó¦ĪŖV02++2H++eŅ»=V02++H20 | |
| B£® | ·Åµē¹ż³ĢÖŠ£¬ÖŹ×ÓĶعż½»»»Ä¤“Óøŗ¼«ĒųŅĘĻņÕż¼«Ēų | |
| C£® | ³äµē¹ż³ĢÖŠ£¬Nµē¼«ÉĻV3+±»»¹ŌĪŖV2+ | |
| D£® | ³äµē¹ż³ĢÖŠ£¬Mµē¼«ø½½üĖįŠŌ¼õČõ |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
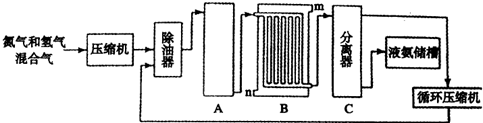
 2NH3£¬Éč±øAµÄĆū³ĘŹĒŗĻ³ÉĖž£»
2NH3£¬Éč±øAµÄĆū³ĘŹĒŗĻ³ÉĖž£»| ŌĮĻ | ĢģČ»Ęų | ÖŲÓĶ | Ćŗ |
| Ļą¶ŌĶ¶×Ź·ŃÓĆ | 1.0 | 1.5 | 2.0 |
| ÄÜĮæĻūŗÄ/J•t-1 | 28109 | 38109 | 48109 |
²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com