
【题目】A,B,C,D均为中学化学中常见的单质或化合物,它们之间的关系如图所示(部分产物已略去). 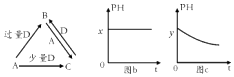
(1)若A为金属单质,D是某强酸的稀溶液,则反应C+D→B的离子方程式为 .
(2)若A为强碱,D为气态氧化物.常温时,将B的水溶液露置于空气中,其pH随时间 t变化可能如上图的图b或图c所示(不考虑D的溶解和水的挥发). ①若图b符合事实,则D的化学式为;
②若图c符合事实,则其pH变化的原因是(用离子方程式表示)
【答案】
(1)3Fe2++4H++NO3﹣═3Fe3++NO↑+2H2O
(2)CO2;2HSO3﹣+O2=2H++2SO42﹣
【解析】解:(1)若A为金属单质,D为某强酸的稀溶液,A和D反应的产物与D的量有关,且B和A反应生成C、C和D反应生成B,说明A为变价金属,为Fe,D为HNO3 , 则B为Fe(NO3)3、C为Fe(NO3)2 , 反应C+D→B的离子方程式为:3Fe2++4H++NO3﹣═3Fe3++NO↑+2H2O, 所以答案是:3Fe2++4H++NO3﹣═3Fe3++NO↑+2H2O;(2)A为强碱,D为气态氧化物,由转化图可知,A可为NaOH,D为CO2或SO2 , B为NaHCO3或NaHSO3 , 常温时将B的水溶液露置于空气中,若为b,则碳酸氢钠符合,若为c则亚硫酸氢钠符合,
①若图b符合事实,则D的化学式为CO2 , 所以答案是:CO2;②若图c符合事实,亚硫酸氢钠易被氧化生成硫酸氢钠,酸性增强,离子反应为:2HSO3﹣+O2═2H++2SO42﹣ ,
所以答案是:2HSO3﹣+O2=2H++2SO42﹣ .


科目:高中化学 来源: 题型:
【题目】在2L的密闭容器中,发生以下反应:2A(g)+ B(g) ![]() 2C(g)+D(g) 。若最初加入的A和B都是4 mol,在前10秒钟A的平均反应速度为0.12 mol/(L·s),则10秒钟时,容器中B的物质的量是( )
2C(g)+D(g) 。若最初加入的A和B都是4 mol,在前10秒钟A的平均反应速度为0.12 mol/(L·s),则10秒钟时,容器中B的物质的量是( )
A. 1.6 mol B. 2.8 mol C. 2.4 mol D. 1.2 mol
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用一种阴、阳离子双隔膜三室电解槽处理废水中的![]() ,模拟装置如图所示。下列说法正确的是
,模拟装置如图所示。下列说法正确的是

A.阳极室溶液由无色变成棕黄色
B.阴极的电极反应式为4OH4e![]() 2H2O+O2↑
2H2O+O2↑
C.电解一段时间后,阴极室溶液中的pH升高
D.电解一段时间后,阴极室溶液中的溶质一定是(NH4)3PO4
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图是由![]() 个碳原子构成的
个碳原子构成的![]() 种有机物(氢原子没有画出):
种有机物(氢原子没有画出):
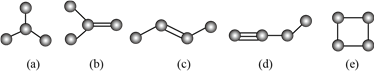
下列说法不正确的是
A. (![]() )、(
)、(![]() )、(
)、(![]() )互为同分异构体
)互为同分异构体
B. (![]() )和(
)和(![]() )的一氯代物都只有一种
)的一氯代物都只有一种
C. (![]() )和(
)和(![]() )都不能使溴在四氯化碳溶液褪色
)都不能使溴在四氯化碳溶液褪色
D. (![]() )、(
)、(![]() )、(
)、(![]() )都能使酸性高锰酸钾溶液褪色
)都能使酸性高锰酸钾溶液褪色
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】化学与生产、生活密切相关,下列说法不正确的是
A.碳酸钠俗称纯碱,可用于去除餐具的油污
B.盐碱地不利于作物生长,可通过施加生石灰进行改良
C.用K2FeO4处理自来水,既可杀菌消毒又可除去悬浮杂质
D.生产医用口罩的聚丙烯树脂原料属于合成有机高分子材料
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】据图回答下列问题:

Ⅰ.①若烧杯中溶液为稀硫酸,则观察到的现象是 ,负极反应式为 。
②若烧杯中溶液为氢氧化钠溶液,则负极为 (填“Mg”或“Al”),总反应的化学方程式为 。
Ⅱ.中国科学院长春应用化学研究所在甲醇燃料电池技术方面获得新突破,组装出了自呼吸电池及主动式电堆。甲醇燃料电池的工作原理如图所示。

①该电池工作时,b口通入的物质为 ,c口通入的物质为 。
②该电池负极的电极反应式为 。
③工作一段时间后,当12.8 g甲醇完全反应生成CO2时,有 NA个电子转移。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列实验操作或实验仪器使用正确的是
A.将高锰酸钾溶液盛装在碱式滴定管中
B.容量瓶、滴定管使用前均需用蒸馏水洗净并烘干
C.用10 mL量筒量取2.5 mL浓硫酸用于配制一定浓度的稀硫酸
D.溶液蒸发浓缩时,用坩埚钳夹持蒸发皿直接加热
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com