
【题目】有A、B、C、D、E五种短周期元素,A与B可形成BA型化合物,且A元素是卤族元素中非金属性最强的元素;金属B的原子核内质子数比它前一周期同主族元素原子的质子数多8;C元素有3种同位素C1、C2、C3,自然界中含量最多的是C1,C3原子的质量数是C1的3倍,C2原子的质量数是C1的2倍;D的气态氢化物的水溶液呈碱性;而其最高价氧化物对应的水化物为强酸;E元素原子的最外层电子数比次外层电子数多4。
(1)写出下列元素的元素符号:A.________,B.______,C.________,D.________,E.________。
(2)写出C1、C2、C3三种原子的符号:C1________,C2________,C3________。
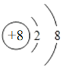
(3)E2-的结构示意图为________。
(4)A与B形成的化合物的化学式是_______,最常见的E原子与C2形成的分子中含________个中子。
【答案】FNaHNO![]()
![]()
![]()
 NaF10
NaF10
【解析】
A、B、C、D、E五种短周期元素,A元素是非金属性最强的元素,即A为F;A与B可形成BA型化合物,金属B的原子核内质子数比它前一周期同主族元素原子的质子数多8个,且B能形成+1价离子,则B为Na元素;C元素有三种同位素C1、C2、C3,自然界里含量最多的是C1,C3原子的质量数是C1的3倍,C2原子的质量数是C1的2倍,故C是H元素;D的气态氢化物水溶液显碱性,而其最高价氧化物水化物为强酸,即D为N元素;E元素原子的最外层电子数比次外层电子数多4个,其次外层含有6个电子,则E为O元素,据此解答。
根据以上分析可知A为F、B为Na、C为H、D为N、E为O,则
(1)根据以上分析可知五种元素的元素符号分别是F、Na、H、N、O;
(2)C为H元素,则C1、C2、C3三种原子分别为氢元素的三种核素原子符号分别是![]() 、
、![]() 、
、![]() ;
;
(3)E为O元素,E2-离子为氧离子,核电荷数为8,最外层达到8电子稳定结构,其离子结构示意图为 ;
;
(4)A为F元素、B为Na元素,A与B形成的化合物为氟化钠,且化学式为NaF;C为H元素、E为O元素,最常见的E原子与![]() 形成的分子为水,该水分子中含有10个中子。
形成的分子为水,该水分子中含有10个中子。


科目:高中化学 来源: 题型:
【题目】实验小组测定某蛋白质的组成(假定只含C、H、O、N元素),设计如下实验(夹持装置略去)。
I.样品中碳、氢含量的测定

(1)仪器a的名称为___________________________。
(2)导管g的作用为______________________________________。
(3)选择上述装置,按气流从左到右的方向,合理的连接顺序为____________________(填大写字母,仪器可重复使用)→排水法收集气体装置。
(4)称取4.65g蛋白质样品,用上述连接好的装置进行实验。
①充分反应后,熄灭D处酒精灯之前,需继续通入O2至硬质玻璃管冷却,原因为__________________。
②充分反应后,测得用于接收气体产物的碱石灰和P2O5分别增重7.7g、2.25g。
Ⅱ.样品中氮元素含量的测定
已知:在催化剂存在下,浓硫酸能将样品中的氮元素转化为铵盐。
i.重新称取4.65g蛋白质样品,将其中的氮元素全部转化为铵盐;
ii.所得铵盐与足量NaOH溶液反应,并用100mLl mol·L-l盐酸将生成的氨气全部吸收;
iii.将吸收液稀释至500mL;
iv.取25.00mL稀释后的溶液,用0.1000 mol·L-l的NaOH溶液平行滴定,平均消耗标准液25.00mL。
(5)蛋白质样品中C、H、N、O的原子数目之比为_____________________。若步骤iii中定容时仰视容量瓶刻度线,则所测氮元素含量___________(填“偏高”“偏低”或“无影响”)。
(6)有同学认为,通过(3)中收集到的气体体积即可得到氮元素的含量,你认为其观点___________(填“正确”或“不正确”),理由为________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用Pb电极电解含有Cu2+和X3+均为0.1mol的溶液,阴极析出金属的质量m与溶液中通过电子的物质的量n关系如图,则离子的氧化性能力由大到小排列正确的是( )

A. Cu2+>X3+>H+ B. H+>X3+>Cu2+
C. X3+>H+>Cu2+ D. Cu2+>H+>X3+
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】全钒电池以惰性材料作电极,在电解质溶液中发生的电池总反应为:
VO2+(蓝色)+H2O+V3+(紫色)![]() VO2+(黄色)+V2+(绿色)+2H+
VO2+(黄色)+V2+(绿色)+2H+
下列说法错误的
A. 充电时,反应每生成2mol H+时电子转移的物质的量为2mol
B. 放电过程中,正极附近溶液的酸性减弱
C. 放电时,正极反应为VO2++2H++e-=VO2++H2O
D. 充电时,阳极附近溶液由蓝色逐渐变为黄色
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】对于可逆反应:4NH3(g)+5O2(g)![]() 4NO(g)+6H2O(g),下列叙述正确的是( )
4NO(g)+6H2O(g),下列叙述正确的是( )
A. 达到化学平衡时,4v正(O2)=5v逆(NO)
B. 若单位时间内生成xmol NO的同时,消耗xmol NH3,则反应达到平衡状态
C. 若有5 mol O===O键断裂,同时有12 mol H—O键形成,此时必为化学平衡状态
D. 化学平衡时,化学反应速率关系是2v正(NH3)=3v逆(H2O)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有机物A为烃类化合物,质谱图表明其相对分子质量为70,其相关反应如下图所示,其中B、D、E的结构中均含有2个-CH3,它们的核磁共振氢谱中均出现4个峰。
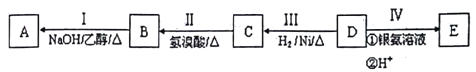
请回答:
(1)D的分子式为______;
(2)B中所含官能团的名称为_______;
(3)Ⅲ的反应类型为_______(填字丹序号);
a. 还原反应 b.加成反应 c.氧化反应 d.消去反应
(4)写出下列反应的化学方程式:
I:_____________________________;
C和E可在一定条件下反应生成F,F为有香味的有机化合物,该反应的化学方程式为______________________________________;
(5)A的同分异构体中有一对互为顺反异构,且结构中有2个-CH3,它们的结构简式为_____和__________________________;
(6)E有多种同分异构体,其中含有![]() 结构的有________种;(不包括E)E的另一种同分异构体能发生银镜反应,能与足量金属钠生成氢气,不能发生消去反应,其结构简式为_______。
结构的有________种;(不包括E)E的另一种同分异构体能发生银镜反应,能与足量金属钠生成氢气,不能发生消去反应,其结构简式为_______。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用铁和石墨作电极电解酸性废水,可将废水中的PO43-以FePO4(不溶于水)的形式除去,其装置如图所示。
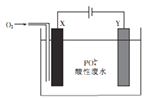
下列说法正确的是
A. 若X、Y电极材料连接反了,则仍可将废水中的PO43-除去
B. X极为石墨,该电极上发生氧化反应
C. 电解过程中Y极周围溶液的pH减小
D. 电解时废水中会发生反应:4Fe2++02-4H++4P043-=4FePO4↓+2H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】乙炔是一种重要的有机化工原料,以乙炔为原料在不同的反应条件下可以转化成以下化合物。

完成下列各题:
(1)正四面体烷的分子为_________,其二氯取代产物有_______种。
(2)关于乙烯基乙炔分子的说法错误的是:____________。
a.能使酸性KMnO4溶液褪色
b.乙烯基乙炔分子内含有两种官能团
c.1摩尔乙烯基乙炔能与3摩尔Br2发生加成反应
d.等质量的乙炔与乙烯基乙炔完全燃烧时的耗氧量不相同
(3)写出与环辛四烯互为同分异构体且属于芳香烃(含有苯环的烃)的分子的结构简式:_________________________________________。
(4)写出与苯互为同系物且一氯代物只有两种的物质的结构简式(举两例):_______、_____。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】元素①~⑧在元素周期表中的位置如下,回答有关问题:
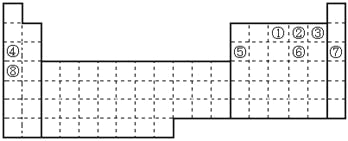
(1)画出⑥的离子结构示意图__________。
(2)在②、③、④、⑤四种元素中,其简单离子半径按由大到小的排列顺序为______(示例:用r(A2-)>r(B-)的形式表示)。
(3)元素②、③氢化物的稳定性由强到弱的顺序为________(填化学式)。
(4)与③同一主族并且在短周期的元素的某种含氧酸可以消毒杀菌,写出该物质的电子式___________________________。
(5)表中能形成两性氢氧化物的元素是_______(填元素符号),写出该元素的单质与⑧的最高价氧化物的水化物反应的离子方程式____________________________。
(6)比较①与其同族短周期元素的氢化物的熔沸点高低,并说明理由_____________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com