
Ⅰ、下列实验操作不正确的是 ;
①用分液漏斗分离环己烷和苯的混合液体
②将10滴溴乙烷加入到1 mL 10%的烧碱溶液中,加热片刻后,冷却,先加过量的硝酸,再滴加2滴2%的硝酸银溶液,以检验水解生成的溴离子。
③分离苯和苯的同系物,可以采用蒸馏的方法。
④实验室制溴苯时选用的试剂可以是溴水、苯和铁屑
Ⅱ、为检验利用溴乙烷发生消去反应后生成的气体中是否含乙烯的装置如右图所示。回答: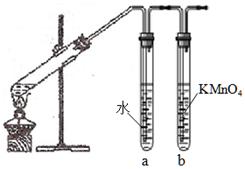
(1)溴乙烷发生消去反应的化学方程式为: ;
(2)试管a的作用是 ;
(3)若省去试管a,试管b中试剂为 。
(9分)Ⅰ、①④(2分,少选给1分,多选不给分),
Ⅱ、(1)CH3CH2Br + NaOH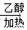 CH2=CH2↑+ NaBr + H2O(3分),
CH2=CH2↑+ NaBr + H2O(3分),
(2)除去挥发出来的乙醇(2分),
溴水或溴的四氯化碳溶液(2分)。
解析试题分析:Ⅰ.①正己烷和苯都是有机物,互溶,分液漏斗分离的物质必须是两种相互不溶的液体,所以,不可分离互溶的环己烷和苯的混合液体,故①错误;②将10滴溴乙烷加入到1mL 10%的烧碱溶液中,加热片刻后,发生取代反应,生成乙醇和溴化钠,冷却,先加过量的硝酸,中和多余的碱,再滴加2滴2%的硝酸银溶液,溴离子和硝酸银中的银离子反应生成浅黄色的溴化银沉淀,以检验水解生成的溴离子,故②正确;③分离苯和苯的同系物,互溶,但它们的沸点不同,可以采用蒸馏的方法进行分离,故③正确;④实验室制溴苯时选用的试剂可以是溴水、苯和铁屑,应该是苯和纯溴在铁作催化剂的作用下,反应,该题用溴水错误,故④错误;故答案为:①④;
Ⅱ.(1)溴乙烷从一个分子中脱去一个溴化氢分子,溴乙烷中的碳碳单键变为双键,故答案为:CH3CH2Br+NaOH CH2=CH2↑+NaBr+H2O;
CH2=CH2↑+NaBr+H2O;
(2)乙醇沸点低,易挥发,但乙醇与水可以任意比互溶,故答案为:除去挥发出来的乙醇;
(3)乙烯和溴水中的溴发生加成反应,溴水褪色,可检验乙烯的存在,故答案为:溴水或溴的四氯化碳溶液
考点:溴乙烷的化学性质
点评:本题考查了卤代烃的性质,注意溴乙烷发生取代反应,生成乙醇与氢溴酸;发生消去反应,生成乙烯和氢溴酸。


 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:
| ||
| ||
| 11200 |
| V |
| 11200 |
| V |
查看答案和解析>>
科目:高中化学 来源: 题型:
(2012?南京二模)下列实验操作与实验目的不一致的是( )
|
查看答案和解析>>
科目:高中化学 来源: 题型:

| ||
| ||
| 11200m |
| V |
| 11200m |
| V |
查看答案和解析>>
科目:高中化学 来源: 题型:
| 选项 | 实验操作 | 实验目的 |
| A | 向某钾盐溶液中加入澄清石灰水 | 证明该钾盐是K2CO3 |
| B | 测定0.1mol/L醋酸溶液的pH | 证明醋酸在水溶液中部分电离 |
| C | 向试管中加入相同体积的浓度为0.005mol/L的FeCl3溶液和0.01mol/L的KSCN溶液,再加入几滴饱和FeCl3溶液 | 证明增大反应物浓度,平衡向正反应方向移动 |
| D | 向试管a中加入1mL甲苯,向试管b中加入1mL苯,再分别向其中加入几滴KMnO4酸性溶液 | 证明甲苯中苯环使甲基的活性增强 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| 操作、现象 | 解释或结论 |
| A.铝箔在酒精灯火焰上加热,熔化但不滴落 | 铝箔对熔化的铝有吸附作用 |
| B.向盛有0.005mol/L FeCl3溶液的试管中加入5mL 0.01mol/LKSCN溶液,溶液呈红色,再加入5滴饱和FeCl3溶液,红色加深 | 增大反应物的浓度,化学平衡向正反应方向移动 |
| C.证明Mg(OH)2沉淀可以转化为Fe(OH)3 沉淀 |
向2mL 1mol/L NaOH溶液中先加入3滴1mol/L MgCl2溶液,再加入3滴1mol/L FeCl3溶液 |
| D.取某溶液少量,加入盐酸酸化的硝酸钡溶液,出现白色沉淀 | 该溶液中一定含有大量的SO42- |
| A、铝箔在酒精灯火焰上加热,熔化但不滴落 |
| B、向盛有0.005mol/L FeCl3溶液的试管中加入5mL 0.01mol/LKSCN溶液,溶液呈红色,再加入5滴饱和FeCl3溶液,红色加深 |
| C、证明Mg(OH)2沉淀可以转化为Fe(OH)3沉淀 |
| D、取某溶液少量,加入盐酸酸化的硝酸钡溶液,出现白色沉淀 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com