
【题目】升高温度能加快化学反应速率的主要原因是
A. 增加活化分子百分数 B. 降低活化分子的能量
C. 活化分子能量明显增加 D. 降低反应所需的能量
科目:高中化学 来源: 题型:
【题目】化学关系着我们的生活,我们的未来。下列说法正确的是
A. 石墨烯(由碳原子构成的六角形蜂巢晶格)材料属于一种新型化合物
B. 可从海水中提取氯化镁,使氯化镁分解获得镁并释放能量
C. 推广用原电池原理制成的太阳能电池汽车,可减少化石能源的使用
D. 采煤工业爆破时把干冰和炸药放在一起,既能增强爆炸威力又能预防火灾
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】漂白粉在工业上有着重要的应用,某同学利用下列仪器在实验室进行制备漂白粉的实验。请回答下列问题:
I.氯气的制备
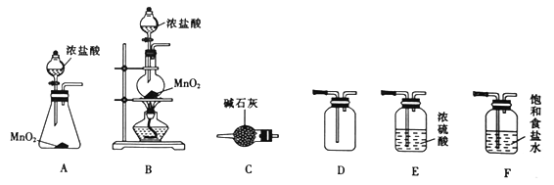
(1)装置C的名称为_______________。
(2)实验室选择上图中的装置制备并收集干燥氯气,其连接顺序为_______________(填字母)。
(3)装置F的作用为___________________________。
Ⅱ.漂白粉的制备
(4)已知:氯气和石灰乳在反应的过程中会放热,当温度较高时会生成Ca(ClO3)2。为了制得纯度较高的漂白粉并提高产率,实验中可采取的措施有__________________、____________________(不改变石灰乳的浓度和体积)。
(5)若将100 mL 12.0 molL-1盐酸与3.48 g MnO2反应制得的氯气全部通入足量的石灰乳中,理论上最多可制得Ca(ClO)2_________g。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下图表示A、B、C、D、E五种物质的相互转化关系,其中A为淡黄色固体,C为金属单质,D为最常用的调味品。写出下列转化的方程式:

(1)C→A的化学方程式:____________________________ ;
(2)C→E的离子方程式:______________________________,
(3)A→B的化学方程式:______________________________,
(4)金属Al和E溶液反应的离子方程式:__________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氯及其化合物有广泛用途。
(1)二氧化氯是一种新型的消毒剂。
①NaClO2中Cl的化合价为____________。
②实验室用氯酸钾与浓盐酸反应制备ClO2,产物除ClO2外,还有Cl2,KCl等,写出该反应的化学方程式 __________。若生成11.2L氯气(标准状况),转移电子数为 _________。
③ClO2和Cl2在消毒时自身均被还原为Cl-,则常温常压下,等体积的ClO2的消毒能力是Cl2的_________倍。
④自来水厂用ClO2处理后的水中,要求ClO2的浓度在0.1﹣0.8 mgL-1之间。碘量法可以检测水中ClO2的浓度(不同pH环境中粒子种类如图所示),步骤如下:
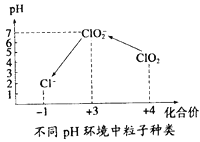
Ⅰ.取一定体积的水样,加入一定量的碘化钾,再将反应后溶液调至中性,并加入淀粉溶液,溶液变蓝。
Ⅱ.加入一定量的Na2S2O3溶液。(己知:2S2O32-+I2═S4O62-+2I-)
Ⅲ.加硫酸调节水样pH至1﹣3。
请问答:
若水样的体积为1.0L,在操作II时消耗了1.0×10-3molL-1的Na2S2O3溶液10mL.则水样中ClO2的浓度是_____ mgL-1。
(2)ICl,ICl3的化学性质与卤素相似,被称为卤素互化物。三氯化碘(ICl3,其中Cl为-1价)常以二聚体的I2Cl6形式存在,经电导仪测定知,它能发生部分电离,生成的两种离子的摩尔质量分别为198 g/mol和269 g/mol,则其电离方程式为 ________________ 。
(3)向盛有一定量的溴化亚铁溶液和四氯化碳溶液的试管中持续通入氯气,反应完毕后,振荡、静置、分层,发现有机层呈红棕色,经检验生成了BrCl(其中Cl为-1价)。可能发生如下反应:
①2Br-+Cl2=2Cl-+Br2 ②Br2+Cl2=2BrCl ③2Fe2++Cl2=2Fe3++2Cl-
按通入氯气,发生先后反应的顺序为 ____________(填序号)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知RxO![]() +MnO
+MnO![]() +H+―→RO2+Mn2++H2O变化过程中,0.2 mol RxO
+H+―→RO2+Mn2++H2O变化过程中,0.2 mol RxO![]() 参加反应,共转移0.4 mol 电子。
参加反应,共转移0.4 mol 电子。
(1)反应的氧化产物为________。
(2)x=________。
(3)参加反应的氢离子的物质的量为________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法不正确的是
A. 淀粉、纤维素水解的最终产物均为葡萄糖
B. 葡萄糖既可以与银氨溶液反应,又可以与新制氢氧化铜悬浊液反应
C. 糖类、油脂、蛋白质都是高分子化合物,都能发生水解反应
D. 天然油脂没有固定的熔点和沸点,所以天然油脂是混合物
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】白磷有剧毒,白磷中毒可用硫酸铜溶液解毒,白磷与硫酸铜可以发生如下两个反应:
(1)2P+5CuSO4+8H2O![]() 5Cu+2H3PO4+5H2SO4
5Cu+2H3PO4+5H2SO4
(2)11P+15CuSO4+24H2O![]() 5Cu3P+6H3PO4+15H2SO4
5Cu3P+6H3PO4+15H2SO4
下列有关说法中错误的是
A. 在上述两个反应中,水既不是氧化剂也不是还原剂
B. 在上述两个反应中,氧化产物都是H3PO4
C. 在反应(2)中,当有5molCuSO4发生反应时,共转移10mol电子
D. 在上述两个反应中,氧化剂都只有硫酸铜
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com