
【题目】下列变化过程不属于金属冶炼的是( )
A. 电解氧化铝B. 铁在氧气中燃烧
C. 金属氧化物与焦炭在高温下反应D. 高温下CO还原CuO
 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
【题目】下列有关图像的叙述正确的是
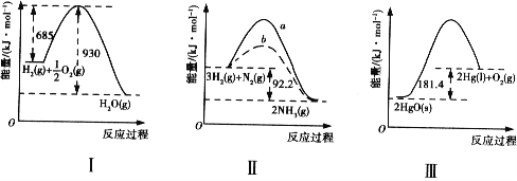
A. 图 I:H2 的燃烧热为 245 kJ/mol
B. 图 II:b 可能为使用催化剂的曲线,活化能降低
C. 图 II:向容器中充入 1 mol N2、3 mol H2,充分反应后放出热量 92.2 kJ
D. 图 III:HgO(s) = Hg(l) + 1/2O2(g) △H = - 90.7 kJ/mol
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某课外活动小组为了研究“干燥的CO2不能与Na2O2反应”和“CO2在有水存在时才能与Na2O2反应”,设计了如下实验装置:

(1)如图装置,在干燥管中装入Na2O2后,打开活塞加入稀硫酸,生成CO2。打开K1,关闭K2,加热铜丝,目的是_____,X是_____。实验观察到铜丝未变化,则得出结论______。
(2)若打开K2,关闭K1,出现________现象,可证明有水时CO2与Na2O2反应产生了O2。
(3)根据以上的实验结论,写出生成CO2、O2反应的化学方程式:_______________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】聚氯乙烯是制作装修材料的最常用原料,失火时聚氯乙烯在不同的温度下,发生一系列复杂的化学变化,产生大量有害气体,其过程大体如下:

下列说法不正确的是
A. 聚氯乙烯的单体可由乙烯与HCl加成而得
B. 上述反应中①属于消去反应,④属于(脱氢)氧化反应
C. 火灾中由聚氯乙烯产生的有害气体中含HCl、CO、C6H6等
D. 在火灾现场,可以用湿毛巾捂住口鼻,并弯下腰尽快远离现场
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】金属(Ti)是航空、宇航、军工、电子等方面的必需原料。在生产钛的过程中可用镁在加热条件下与TiCl4反应制得金属钛,反应的化学方程式为:TiCl4+2Mg![]() Ti+2MgCl2。该反应属于( )
Ti+2MgCl2。该反应属于( )
A. 化合反应B. 分解反应C. 置换反应D. 无法确定
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】印刷铜制电路板的腐蚀液选取和回收再利用一直是研究的热点。
(1)FeCl3溶液一直作为传统的腐蚀液。
① 腐蚀过程中的离子方程式为______。
![]()
② 腐蚀结束后,通过以下两步可分离出铜,并实现FeCl3溶液再生。
i. 步骤I所加试剂和操作分别为______。
ii. 可实现步骤II转化的物质或方法是______(填一种即可)。
(2)研究发现,CuCl2溶液添加盐酸或氨水配制成酸性腐蚀液或碱性腐蚀液,其效果优于FeCl3溶液。腐蚀液的主要成分及腐蚀原理如下:
腐蚀液类型 | 主要成分 | 腐蚀原理 |
酸性腐蚀液 | Cu2+、H+、Cl- | Cu+ Cu2++2Cl- CuCl+2Cl- |
碱性腐蚀液 | Cu(NH3)42+、NH4+、NH3、Cl- | Cu(NH3)42++ Cu === 2Cu(NH3)2+ |

①酸性腐蚀液中铜离子含量对腐蚀速率的影响如右图所示,为保持较快和较平稳的腐蚀速率,腐蚀液中铜离子含量应选择______ g/100mL的使用范围。
②酸性腐蚀废液经过处理后,倒入一定量的水中,可得CuCl沉淀,过滤、洗涤、干燥后即得产品CuCl。倒入一定量的水中,可得CuCl沉淀的原因是_______。
③ 通入适量的氧气可使碱性腐蚀液再生。将该过程的离子方程式补充完整:______________
![]()
(3)H2O2也常用来腐蚀金属铜,使用时加入盐酸或氨水将其配制成酸性或碱性腐蚀液。回收其废液的工艺如下:


① 酸性条件下H2O2腐蚀金属铜的离子方程式为______。
② 右图是研究碱性腐蚀液的温度对铜腐蚀量的实验结果,升高温度,腐蚀量变化的原因______。
③ 碱转时的反应为:Cu2(OH)3Cl+NaOH =CuO+Cu(OH)2+NaCl+H2O。检验转化完全的方法是:取少量洗涤后的碱转固体,_______。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】苯甲酸是常用的防腐剂和重要的医药原料。一种药用苯甲酸的制备方法如下:
Ⅰ.在反应罐中加入甲苯、饱和KMnO4溶液、Fe2O3(催化剂),加热、回流数小时,充分反应。
Ⅱ.反应结束后,改为蒸馏装置。加热蒸馏,直至冷凝管壁不再出现油珠。
Ⅲ.将反应罐中的混合物趁热过滤,滤渣用少量热水洗涤。
Ⅳ.向滤液中滴加浓盐酸酸化至pH=2,抽滤,用少量水洗涤,干燥得苯甲酸粗品。
Ⅴ.将粗苯甲酸加入……,结晶、洗涤、过滤,得到药用纯苯甲酸。
已知:相关物质的溶解度(g/mL)
温度(℃) | 25 | 50 | 60 | |
苯甲酸 | 在水中 | 0.0034 | 0.0085 | 0.0095 |
在乙醇中 | 0.4 | 0.7 | 1 | |
氯化钾 | 在乙醇中 | 难溶 | ||
(1)Ⅰ中发生的主要反应为:![]() (未配平),则Ⅳ中发生反应的离子方程式为______。
(未配平),则Ⅳ中发生反应的离子方程式为______。
(2)Ⅱ中蒸馏的目的是______。
(3)Ⅲ中趁热过滤的目的是______。
(4)将Ⅴ中操作补充完整:______。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在25mL 0.1mol/L NaOH溶液中逐滴加入0.2mol/L CH3COOH溶液,曲线如图所示,下列有关离子浓度关系的比较,正确的是

A. A、B之间任意一点,溶液中一定都有c(Na+)>c(CH3COO-)>c(OH-)>c(H+)
B. B点,a>12.5,且有c(Na+)=c(CH3COO-)=c(OH-)=c(H+)
C. C点:c(Na+)>c(CH3COO-)>c(H+)>c(OH-)
D. D点:c(CH3COO-)+c(CH3COOH)=2c(Na+)
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com