
【题目】计算后填空:
(1)在标准状况下,448 mL某气体的质量为0.64 g,计算这种气体的相对分子质量为________。
(2)某氯化铁与氯化钠的混合液,已知c(Fe3+)=0.2 mol·L-1,c(Cl-)=1 mol·L-1。则c(Na+)为 。
(3)19g某二价金属的氯化物RCl2中含有0.4mol的Cl-离子,则R的相对原子质量为 。
(4)V L Fe2(SO4)3溶液中含Fe3+ m g,则溶液中SO42-的物质的量浓度为 mol·L-1。
(5)在无土栽培中,配制1 L内含5 mol NH4Cl、1.6 mol KCl、2.4 mol K2SO4的某营养液,若用KCl、NH4Cl、(NH4)2SO4配制,则需KCl、NH4Cl的物质的量分别为 _____________ 、 ________ 。
(6)如图所示,分别向密闭容器内可移动活塞的两边充入空气(已知空气体积占整个容器容积的1/4)、H2和O2的混合气体,在标准状况下,若将H2、O2的混合气体点燃引爆。活塞先左弹,恢复原温度后,活塞右滑停留于容器的中央。则原来H2、O2的体积之比可能为 。

【答案】
(1)32;
(2)0.4 mol·L-1;
(3)24;
(4)3m/112V;
(5)6.4mol;0.2mol
(6)7:2 或4:5
【解析】
试题分析:(1)标准状况下,448mL气体的物质的量为:![]() =0.02mol,该气体的摩尔质量为:
=0.02mol,该气体的摩尔质量为:![]() =32g/mol,故答案为:32;
=32g/mol,故答案为:32;
(2)溶液呈电中性,根据电荷守恒3c(Fe3+)+c(Na+)=c(Cl-),则:3×0.2molL-1+c(Na+)=1molL-1,解得c(Na+)=0.4 molL-1,故答案为:0.4 molL-1;
(3)19g某二价金属的氯化物RCl2中含有0.4mol的Cl-离子,则19gRCl2的物质的量为0.4mol×![]() =0.2mol,RCl2的摩尔质量为
=0.2mol,RCl2的摩尔质量为![]() =95g/mol,则RCl2的相对分子质量为95,所以R的相对原子量为:95-35.5×2=24,故答案为:24;
=95g/mol,则RCl2的相对分子质量为95,所以R的相对原子量为:95-35.5×2=24,故答案为:24;
(4)VLFe2(SO4)3溶液中含Fe3+mg,含有铁离子的物质的量为:![]() =
=![]() mol,溶液中含有硫酸根离子的物质的量为:
mol,溶液中含有硫酸根离子的物质的量为:![]() mol×
mol×![]() =
=![]() mol,则溶液中SO42-的物质的量浓度为:
mol,则溶液中SO42-的物质的量浓度为: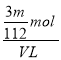 =
=![]() mol/L,故答案为:
mol/L,故答案为:![]() ;
;
(5)在无土栽培中,配制1L内含5molNH4Cl、1.6molKCl、2.4molK2SO4的某营养液,该培养液中含有钾离子的总物质的量为:1.6mol+2.4mol×2=6.4mol,根据钾离子守恒,需要氯化钾的物质的量为6.4mol;需要配制的溶液中含有氯离子的物质的量为:5mol+1.6mol=6.6mol,其中6.4mol氯化钾中提供了6.4mol氯离子,则还需要氯化铵的物质的量为:6.6mol-6.4mol=0.2mol,故答案为:6.4mol;0.2mol;
(6)令空气的物质的量为1mol,反应前,左右两室的体积之比为1:3,反应前右室的物质的量为3mol,反应后,活塞处于中央,两室体积相等,则两室中气体的物质的量相等,反应后右室气体物质的量为1mol,发生反应2H2+O2![]() 2H2O,
2H2O,
设H2、O2的物质的量分别为xmol、ymol,
若氢气过量,则:x2y=1,x+y=3,解得x:y=7:2,
若氧气过量,则:y0.5x=1,x+y=3,解得x:y=4
故答案为:7:2 或4:5。


科目:高中化学 来源: 题型:
【题目】现有三组溶液:①汽油和氯化钠溶液 ②39%的乙醇溶液 ⑧氯化钠和单质溴的水溶液,分离以上各混合液的正确方法依次是( )
A.分液、萃取、蒸馏 B.萃取、蒸馏、分液
C.分液、蒸馏、萃取 D.蒸馏、萃取、分液
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】当水发生如下变化时:H2O(s)→H2O(l) →H2O(g),此过程的△S(熵变)判断正确的是 ( )
A.<0
B.>0
C.不变
D.无法判断
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)工农业生产和生活中常常进行分离或提纯,请选择相应的方法代号填入空白处:
a.过滤 B.蒸馏 C..萃取 d分液
①分离水和菜籽油的混合物 。②海水淡化 。
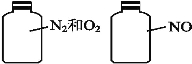
(2)如图,两瓶体积相等的气体,在同温、同压下,原子总数 (填“相等”、“不相等”),当两瓶气体质量相等时,N2和O2的体积比为 。
(3)下列物质所含分子数由多到少的顺序是 。(用A、B、C、D排序)
A.标准状况下33.6 L CO
B.所含电子为4 mol的H2
C.20 ℃时45 g H2O
D.常温下,0.5NA个CO2与0.5NA个CO的混合气体
(4)与50 mL 1mol·L-1 MgCl2溶液中的Cl-物质的量浓度相等的是
A.50 mL 1 mol·L-1 FeCl3溶液
B.25 mL 2 mol·L-1 CaCl2溶液
C.50 mL 2 mol·L-1 KCl溶液
(5)某状况下气体摩尔体积为Vm L/mol, 将a L NH3溶解于水中形成b mL氨水溶液,所得溶液的密度为ρ g/cm3,则氨水的溶质质量分数为 。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法正确的是 ( )
A.在原电池中,电子由正极流向负极
B.在电解池中,物质在阴极发生氧化反应
C.在原电池中,物质在负极发生氧化反应
D.在电解池中,与电源正极相连的电极是阴极
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】向一恒容密闭容器中充入2mol SO2和1mol O2,在一定条件下发生反应:2SO2+O2![]() 2SO3下列有关说法正确的是( )
2SO3下列有关说法正确的是( )
A.达到化学平衡时,正反应和逆反应的速率都为零
B.当O2的浓度不变时,反应达到平衡状态
C.当单位时间消耗a mol O2,同时消耗2a mol SO2时,反应达到平衡状态
D.当SO2、O2、SO3的分子数比为2:1:2,反应达到平衡状态
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用光洁的铂丝蘸取无色溶液在无色灯焰上灼烧时观察到黄色火焰,下列叙述正确的是( )
A. 只含有Na+ B. 一定含Na+,也可含K+
C. 既含Na+又含有K+ D. 可能含Na+或K+中一种
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】甲醇质子交换膜燃料电池中将甲醇蒸气转化为氢气的两种反应原理是
①CH3OH(g)+H2O(g)═CO2(g)+3H2(g)△H=+49.0kJmol﹣1
②CH3OH(g)+O2(g)═CO2(g)+2H2(g)△H=﹣192.9kJmol﹣1
下列说法正确的是( )

A.CH3OH的燃烧热(△H)为﹣192.9kJmol﹣1
B.反应①中的能量变化如图所示
C.CH3OH转变成H2的过程一定要吸收能量
D.根据②推知反应:CH3OH(l)+O2(g)
=CO2(g)+2H2(g)的△H>﹣192.9kJmol﹣1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列各项应用涉及的化学原理完全相同的是
A. 用氯化铁或液氯处理废水 B. 用铁槽车或铝槽车运输浓硫酸
C. 用二氧化硫或氯气漂自织物 D. 用亚硫酸钠或氯水处理二氧化硫尾气
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com