
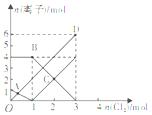
查阅资料知:2Fe3++M2—===2Fe2++M,向含有M2-、Fe2+的溶液中
缓慢通入氯气,溶液中相关的几种离子的物质的量变化如图所示
(其它离子不参与反应)。
下列说法正确的是
A.B点时溶液中含有Fe3+、Cl—、M2—
B.OD段表示n(Fe3+)的变化情况
C.原溶液中n(Fe2+):n(M2-)=1:4
D.当通入1molCl2后再通入Cl2时,溶液中发生了离子反应是:2Fe2++Cl2==2Fe3++2Cl—
 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:阅读理解
| 编号 | 操作 | 现象 |
| I | 先向2mL 0.1mol/L FeCl2溶液中滴加KSCN溶液,再滴加新制氯水 | |
| II | 先向2mL 0.1mol/L FeCl3溶液中滴加KSCN溶液,再滴加0.1mol/L KI溶液 | 滴加KSCN溶液后,溶液变成红色;滴加KI溶液后,红色无明显变化 |
| 编号 | 操作 | 现象 |
| III | 向2mL 0.1mol/L KI溶液中滴加1mL 0.1mol/L FeCl3溶液,再滴加KSCN溶液 | 滴加FeCl3溶液后,溶液变成黄色;滴加KSCN溶液后,溶液变成红色 |
| 编号 | 操作 | 预期现象及结论 |
| IV | 向2mL 0.1mol/L KI溶液中滴加1mL0.1mol/L FeCl3溶液, | 预期现象:溶液变蓝(或溶液分层,下层溶液为紫色;或生成蓝色沉淀),结论:Fe3+能与I-发生氧化还原反应,生成I2(或Fe2+) 预期现象:溶液变蓝(或溶液分层,下层溶液为紫色;或生成蓝色沉淀),结论:Fe3+能与I-发生氧化还原反应,生成I2(或Fe2+) |
查看答案和解析>>
科目:高中化学 来源: 题型:阅读理解

| 9(b-a) |
| a |
| 900(b-a) |
| a |
| 9(b-a) |
| a |
| 900(b-a) |
| a |
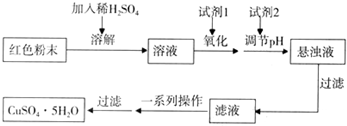
| 物质 | Cu(OH)2 | Fe(OH)2 | Fe(OH)3 |
| 开始沉淀pH | 6.0 | 7.5 | 1.4 |
| 沉淀完全pH | 13 | 14 | 3.7 |
查看答案和解析>>
科目:高中化学 来源: 题型:阅读理解
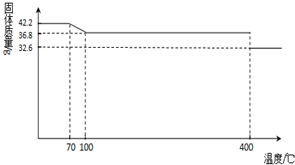 (2013?德州模拟)食盐中的抗结剂是亚铁氰化钾,其化学式为K4[Fe(CN)6]?3H2O.
(2013?德州模拟)食盐中的抗结剂是亚铁氰化钾,其化学式为K4[Fe(CN)6]?3H2O.查看答案和解析>>
科目:高中化学 来源: 题型:
 查阅资料知:2Fe3++M2-═2Fe2++M,向含有M2-、Fe2+的溶液中缓慢通入氯气,溶液中相关的几种离子的物质的量变化如图所示(其它离子不参与反应)下列说法正确的是( )
查阅资料知:2Fe3++M2-═2Fe2++M,向含有M2-、Fe2+的溶液中缓慢通入氯气,溶液中相关的几种离子的物质的量变化如图所示(其它离子不参与反应)下列说法正确的是( )| A、B点时溶液中含有Fe3+、Cl-、M2- | B、OD段表示n(Fe3+)的变化情况 | C、原溶液中n(Fe2+):n(M2-)=1:4 | D、当通入1molCl2后再通入Cl2时,溶液中发生了离子反应是:2Fe2++Cl2═2Fe3++2Cl- |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com