
【题目】设NA表示阿伏加德罗常数的值,下列说法正确的是()
A. 分子总数为NA的NO2和CO2的混合气体中含有的氧原子数为2NA
B. 1mol NaCl中所含电子总数为20NA
C. 46g NO2和N2O4的混合气体中含有的原子总数为4.5NA
D. 常温常压下,22.4L CO2中含有的CO2分子数为NA
【答案】A
【解析】
A. 每个NO2和CO2分子中含有2个氧原子。
B. NaCl由钠离子和氯离子构成,每个钠离子含有10个电子,每个氯离子含有18个电子。
C. NO2和N2O4的最简式为NO2,计算46g NO2中的原子数。
D. 常温常压下气体摩尔体积大于,22.4L /mol。
A.每个NO2和CO2分子中含有2个氧原子,分子总数为NA的NO2和CO2的混合气体中含有的氧原子数为2NA,A正确。
B. NaCl由钠离子和氯离子构成,每个钠离子含有10个电子,每个氯离子含有18个电子,1mol NaCl中所含电子总数为28NA,B错误。
C. NO2和N2O4的最简式为NO2,46g NO2中含有的原子总数N=nNA×3=![]() ×NA×3=
×NA×3=![]() ×NA×3=3NA,C错误。
×NA×3=3NA,C错误。
D. 常温常压下气体摩尔体积大于22.4L /mol,常温常压下22.4L CO2的物质的量小于1mol,含有的CO2分子数小于NA,D错误。
答案为A。


科目:高中化学 来源: 题型:
【题目】对某难溶电解质AnBm的饱和溶液中,下列说法正确的是
A. 加同温度的水,其溶度积减小、溶解度增大
B. 升高温度,它的溶解度和溶度积都增大
C. 饱和溶液中c(Am+)=c(Bn﹣)
D. 加同温度的水,其溶度积、溶解度均不变
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】掌握仪器名称、组装及使用方法是中学化学实验的基础,下图为两套实验装置。
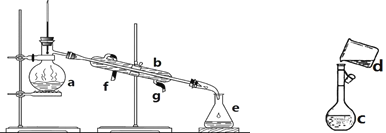
(1)写出下列仪器的名称:a. __________,b. __________,c. ___________。
(2)仪器a~e中,使用前必须检查是否漏水的有____________________________。(填序号)
(3)若利用装置I分离四氯化碳和酒精的混合物,还缺少的仪器是_______________,将仪器补充完整后进行的实验操作的名称为:____________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】镓是制作高性能半导体的重要原料。在工业上经常从锌矿冶炼的废渣中回收镓。已知锌矿渣中含有Zn、Fe、Pb、Ga以及二氧化硅等,目前综合利用锌矿渣的流程如下:
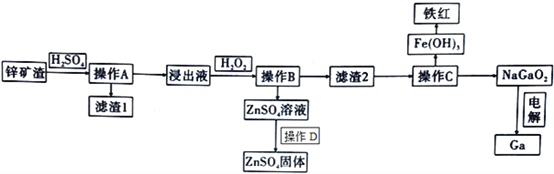
已知:①Ga性质与铝相似。
②lg2=0.3,lg3=0.48。
③如下表所示。
Zn(OH)2 | Ga(OH)3 | Fe(OH)2 | Fe(OH)3 | |
Ksp | 1.6×10-17 | 2.7×10-31 | 8×10-16 | 2.8×10-39 |
(1)写出Ga的原子结构示意图______________________________。
(2)滤渣1的成分为________________________。
(3)加入H2O2的目的( 用离子方程式和适当语言回答) ____________________________________。
(4)室温条件下,若浸出液中各种阳离子的浓度均为0.01mo/L且某种离子浓度小于1×10-5 mol/L即认为该离子已完全除去,问操作B调节pH的范围是________________________。
(5)操作C中,需要加入氢氧化钠溶液,其目的是_____________________ (用离子方程式解释);能否用氨水代替NaOH溶液,为什么? ________________________;如何检测Fe(OH)3洗涤干净? ________________________。
(6)在工业上,经常用电解NaGaO2溶液的方法生产Ga,写出阴极的电极反应方程式:____________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法正确的是( )
A.ⅥA族元素中氢化物最稳定的其沸点一定最高
B.醋酸铵是含有极性键的共价化合物
C.离子化合物中不可能含有非极性共价键
D.二氯甲烷分子为正四面体结构
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】工业上用电解法处理含镍酸性废水并得到单质镍的原理如图所示。下列说法错误的是

已知:①Ni2+在弱酸性溶液中发生水解;
②氧化性:Ni2+(高浓度)>H+>Ni2+(低浓度)
A. 碳棒上发生的电极反应:4OH4e= O2↑+2H2O
B. 为了提高镍的产率,电解过程中需要控制废水的pH
C. 电解过程中,B中NaCl溶液的物质的量浓度将不断减少
D. 若将图中阳离子膜去掉,将A、B两室合并,则电解反应总方程式发生改变
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】回答下列问题。
(1)下列物质能导电且属于电解质的是________(填序号)。
A. 固态氯化镁(MgCl2) B. 液态氯化镁(MgCl2)
C. 氯化钠溶液D. 铝
(2)写出下列物质在水溶液中的电离方程式:
①Na2CO3______________;
②H2SO4______________;
③KHSO4_____________。
(3)有人说可将无机化合物KHSO4与NaHCO3归为同一类别,你认为他的理由主要是_____;有人说可将无机化合物KHSO4与H2SO4归为同一类别,你认为他的理由主要是_________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(2018·天津市十二重点中学毕业班联考)已知:25℃时H2C2O4的pKa1=1.22,pKa2=4.19,CH3COOH的pK a=4.76,K代表电离平衡常数,pK = -1gK。下列说法正确的是
A. 浓度均为0.1mol·L-1NH4HC2O4和CH3COONH4溶液中:c(NH4+)前者小于后者
B. 将0.1mol·L-1的K2C2O4溶液从25℃升温至35℃,![]() 减小
减小
C. 0.1 mol·L-1K2C2O4溶液滴加盐酸至pH=1.22:c(H+)-c(OH-)=c(Cl-)-3c(HC2O4-)
D. 向0.1 mol·L-1CH3COONa溶液中滴加少量0.1 mol·L-1H2C2O4溶液:CH3COO- + H2C2O4 = CH3COOH + HC2O4-
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com