
 随着世界工业经济的发展、人口的剧增,全球能源紧张及世界气候面临越来越严重的问题,如何降低大气中CO2的含量及有效地开发利用CO2引起了全世界的普遍重视.
随着世界工业经济的发展、人口的剧增,全球能源紧张及世界气候面临越来越严重的问题,如何降低大气中CO2的含量及有效地开发利用CO2引起了全世界的普遍重视.分析 (1)O2与C完全反应生成14g即0.5molCO放热60kJ热量,生成2molCO放热240KJ,反应为放热反应,反应的焓变为-240KJ/mol,依据热化学方程式书写得到;
(2)根据盖斯定律可知,反应热只与始态和终态有关,而与反应的途径无关;由盖斯定律,将途径Ⅱ的三个化学方程式乘以适当的系数进行加减,反应热也乘以相应的系数进行相应的加减,构造出途径I的热化学方程式,据此判断△H1、△H2、△H3、△H4的数学关系式;
(3)题干所给量计算32g甲醇燃烧生成二氧化碳和液态水放热,结合热化学方程式书写方法,标注物质聚集状态和对应焓变;正极通氧气该电极上氧气得电子和氢离子反应生成水;负极通燃料失电子发生还原反应;
(4)根据盖斯定律,将所给的已知反应通过加减乘除等变形,来得到目标反应,并将反应热也做相应的变形即可;
(5)①6Ag(s)+O3(g)═3Ag2O(s),△H=-260kJ•mol-1,
②2Ag2O(s)═4Ag(s)+O2(g),△H=+70kJ•mol-1,
根据盖斯定律可知①×2+②×3可得到,2O3(g)═3O2(g),以此计算反应热.
解答 解:(1)O2与C完全反应生成14g即0.5molCO放热60kJ热量,生成2molCO放热240KJ,反应为放热反应,反应的焓变为-240KJ/mol,反应的热化学方程式为:2C(s)+O2( s )=2CO(s)△H=-240kJ/mol,
故答案为:2C(s)+O2( s )=2CO(s)△H=-240kJ/mol;
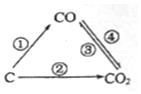
(2)根据盖斯定律可知,反应热只与始态和终态有关,而与反应的途径无关,通过观察可知途径Ⅰ和途径Ⅱ是等效的,途径Ⅰ和途径Ⅱ等量的煤燃烧消耗的氧气相等,两途径最终生成物只有二氧化碳,所以途径Ⅰ放出的热量等于途径Ⅱ放出的热量;
途径Ⅱ:C(s)+H2O(g)═CO(g)+H2(g)△H2>0 ②
再燃烧水煤气:2CO(g)+O2(g)═2CO2(g)△H3<0 ③
2H2(g)+O2 (g)═2H2O(g)△H4<0 ④
由盖斯定律可知,②×2+③+④得2C(s)+2O2 (g)═2CO2(g)△H=2△H2+△H3+△H4.
所以△H1=$\frac{1}{2}$△H=$\frac{1}{2}$(2△H2+△H3+△H4)=△H2+$\frac{1}{2}$(△H3+△H4).
故答案为:等于;△H1=△H2+$\frac{1}{2}$(△H3+△H4);
(3)在25℃、101kPa下,1g甲醇(CH3OH)燃烧生成CO2和液态水时放热25kJ.32g甲醇燃烧生成1molCO2和液态水放出热量为800KJ;则表示甲醇燃烧的热化学方程式为:CH3OH(l)+$\frac{3}{2}$O2(g)=CO2(g)+2H2O(l)△H=-800kJ•mol-1,正极通氧气该电极上氧气得电子和氢离子反应生成水,故电极反应方程式为3O2+12e-+12H+=6H20;负极通燃料失电子发生还原反应,故电极反应方程式为2CH3OH-12e-+2H20=2CO2+12H+;
故答案为:CH3OH(l)+$\frac{3}{2}$O2(g)=CO2(g)+2H2O(l)△H=-800kJ•mol-1;3O2+12e-+12H+=6H20;2CH3OH-12e-+2H20=2CO2+12H+;
(4)已知:①C(S)+O2(g)=CO2(g)△H=-400KJ/mol
②2CO(g)+O2=2CO2(g)△H=-560KJ/mol
③TiO2(s)+2Cl2(g)=TiCl4(s)+O2(g)△H=+140KJ/mol
金红石与氯气、石墨制取TiCl4(s)和CO的化学反应方程式可以通过③+①×2-②得到,
所以TiO2(s)+2Cl2(g)+2C(s)=TiCl4(s)+2CO(g)△H=140kJ/mol-400kJ/mol×2+560kJ/mol=-100KJ/mol,
即TiO2(s)+2Cl2(g)+2C(s)=TiCl4(s)+2CO(g)△H=-100KJ/mol,
故答案为:TiO2(s)+2Cl2(g)+2C(s)=TiCl4(s)+2CO(g)△H=-100KJ/mol,
故答案为:-100KJ/mol;
(5)①6Ag(s)+O3(g)═3Ag2O(s),△H=-260kJ•mol-1,
②2Ag2O(s)═4Ag(s)+O2(g),△H=+70kJ•mol-1,
根据盖斯定律可知①×2+②×3可得到,2O3(g)═3O2(g),则反应热△H=(-260kJ•mol-1)×2+(+70kJ•mol-1)×3=-310kJ/mol,
故答案为:2O3(g)═3O2(g)△H=-310kJ/mol.
点评 本题考查较综合,涉及热化学反应方程式、盖斯定律的应用,侧重反应原理的考查,注重知识的迁移应用,题目难度中等.


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:选择题
| A. | ①②⑤ | B. | ①③④ | C. | ①②③⑤ | D. | ①③⑤ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| X | Y | |
| Z | ′ | R |
| W |
| A. | 原子半径大小关系为:R>Y>X | |
| B. | X有多种同素异形体,而Y不存在同素异形体 | |
| C. | 根据元素周期律t可以推测W元素的单质具有半导体特性,W2Y3具有氧化性和还原性 | |
| D. | 氢化物熔沸点:H2R>H2Y |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
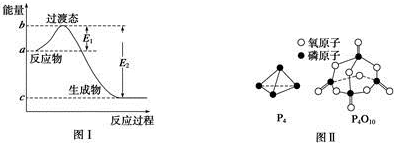
| 化学键 | P-P | P-O | O═O | P═O |
| 键能/kJ•mol-1 | a | b | c | x |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 许多含碳、含氢物质是重要的化工原料.
许多含碳、含氢物质是重要的化工原料.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 食用醋就是冰醋酸 | B. | 医用酒精浓度为75% | ||
| C. | 钢铁生锈主要是发生了析氢腐蚀 | D. | 汽车尾气的排放会引起臭氧空洞 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | CH3CH2OH | B. | CH3COOC2H5 | C. | CH3OH | D. | CH3COOCH3 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com