
| A. | 向水中通入氯气:Cl2+H2O═H++Cl-+HClO | |
| B. | 向明矾溶液中加过量氨水:Al3++4NH3•H2O═AlO2-+4NH4++2H2O | |
| C. | 硫酸氢钠溶液中逐滴加入氢氧化钡溶液,至溶液恰好呈中性:Ba2++OH一+SO42-+H+═BaSO4↓+H2O | |
| D. | 溴乙烷与6mol/L氢氧化钠水溶液共热:C2H5Br+OH-CH2═CH2↑+Br-+H2O |
分析 A.次氯酸为弱电解质,应保留化学式;
B.不符合反应的客观事实,铝离子与氨水反应生成氢氧化铝和氨根离子;
C.硫酸氢钠溶液中逐滴加入氢氧化钡溶液,至溶液恰好呈中性,二者按2:1反应;
D.溴乙烷与6mol/L氢氧化钠水溶液共热发生取代反应,生成乙醇.
解答 解:A.向水中通入氯气,离子方程式:Cl2+H2O═H++Cl-+HClO,故A正确;
B.向明矾溶液中滴加过量氨水,氢氧化铝不溶于氨水,反应的离子方程式为Al3++3NH3•H2O=Al(OH)3↓+3NH4+,故B错误;
C.硫酸氢钠溶液中逐滴加入氢氧化钡溶液,至溶液恰好呈中性,二者按2:1反应,离子方程式为Ba2++2OH-+SO42-+2H+═BaSO4↓+2H2O,故C错误;
D.溴乙烷与6mol/L氢氧化钠水溶液共热反应生成乙醇和溴化钠,离子方程式:C2H5Br+OH-→CH3-CH2-OH+Br-,故D错误;
故选:A.
点评 本题考查了离子方程式的书写,明确反应实质是解题关键,注意卤代烃发生取代反应和消去反应的条件为易错点,注意反应物用量对反应的影响,题目难度不大.


科目:高中化学 来源: 题型:选择题
| A. | 小苏打可以用作胃溃疡患者的胃酸中和剂 | |
| B. | 二氧化硫可以用来漂白纸浆、毛、丝、草帽辫、银耳、米粉等 | |
| C. | 飞机播撒碘化银或干冰可实现人工降雨 | |
| D. | 为防止中秋月饼等富脂食品因被氧化而变质,常在包装袋中放入生石灰或硅酸 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | KSCN | B. | BaCl2 | C. | NaOH | D. | HCl |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 用高效催化剂,可提高CO2的利用率 | |
| B. | 单位时间内消耗CO2和H2的物质的量比为1:3时,反应达到平衡 | |
| C. | 及时分离出CH3OH和H2O可提高CO2和H2的利用率 | |
| D. | 升高温度可使该反应向正反应方向移动 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

| 编号 | Ⅰ | Ⅱ | Ⅲ |
| a | 干燥的有色布条 | 碱石灰 | 湿润的有色布条 |
| b | 干燥的有色布条 | 无水硫酸铜 | 湿润的有色布条 |
| c | 湿润的有色布条 | 浓硫酸 | 干燥的有色布条 |
| d | 湿润的有色布条 | 无水氯化钙 | 干燥的有色布条 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 氮原子的价电子排布图: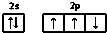 | |
| B. | 2p和3p轨道形状均为哑铃形,能量也相等 | |
| C. | 价电子排布为4s24p3的元素位于第四周期第ⅤA族,是p区元素 | |
| D. | 钠原子由1s22s22p63s1→1s22s22p63p1时,原子释放能量,由基态转化成激发态 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 族 周期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 |
| 二 | ① | ⑩ | ② | ③ | ||||
| 三 | ④ | ⑤ | ⑥ | ⑦ | ⑧ | ⑨ |
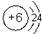 ,元素⑩的单质与氢气反应的化学方程式为N2+3H2$\frac{\underline{\;\;催化剂\;\;}}{高温高压}$2NH3.
,元素⑩的单质与氢气反应的化学方程式为N2+3H2$\frac{\underline{\;\;催化剂\;\;}}{高温高压}$2NH3.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com