
Ⅰ.有一透明溶液,可能含有较大量的Mg2+、Fe3+、Al3+、Cu2+、Na+、H+、SO42-、CO32-中的一种或几种,取此溶液做下列实验
①取少量溶液加入用盐酸酸化的BaCl2溶液,有白色沉淀生成;
②取少量溶液加入过氧化钠粉末,溶液中有白色沉淀产生并逸出无色无味的气体,加入Na2O2的物质的量与析出沉淀的物质的量如图所示;

试推断:
(1)溶液中一定含有的离子是_________________;
(2)溶液中肯定不含有的离子是_________________;
(3)可能含有的离子是________________;
(4)为了进一步确定可能含有的离子,应增加的实验操作为___________________。
Ⅱ.某溶液中含有Ba2+、Cu2+、Ag+,现用NaOH溶液、盐酸和Na2SO4溶液将这三种离子逐一沉淀分离,其流程如右图,已知沉淀2为蓝色。
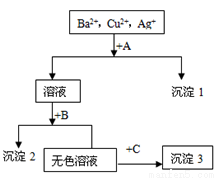
(1)沉淀的化学式:沉淀1____________、沉淀3____________;
(2)写出混合液+A的离子方程式 _________________;
写出溶液+B生成沉淀2的离子方程式_________________;
科目:高中化学 来源:2015-2016学年山西省高二上11月月考化学试卷(解析版) 题型:选择题
高铁电池是一种新型可充电电池,与普通高能电池相比,该电池能长时间保持稳定的放电电压。高铁电池的总反应为: 下列叙述不正确的是( )
下列叙述不正确的是( )
A.放电时负极反应为:Zn-2e- +2OH-= Zn(OH)2
B.充电时阳极反应为:Fe(OH)3-3e-+5OH-= FeO42-+4H2O
C.放电时每转移3 mol电子,正极有1 mol K2FeO4被氧化
D.放电时正极附近溶液的碱性增强
查看答案和解析>>
科目:高中化学 来源:2015-2016学年贵州省高一上半期测试化学试卷(解析版) 题型:选择题
下列离子方程式书写正确的是
A.石灰石与盐酸反应:CO +2H+ == CO2↑ + H2O
+2H+ == CO2↑ + H2O
B.铁与盐酸反应:2Fe + 6H+ == 2Fe3+ + 3H2↑
C.氢氧化钡溶液中滴加硫酸:Ba2+ + OH- + H+ + SO42- == BaSO4↓ + H2O
D.硫酸铜溶液与烧碱溶液反应:Cu2+ + 2OH﹣== Cu(OH)2↓
查看答案和解析>>
科目:高中化学 来源:2015-2016学年江苏省高二上第二次质检化学试卷(解析版) 题型:选择题
对原电池的电极名称,下列叙述中错误的是
A.电子流入的一极为正极
B.比较不活泼的一极为正极
C.电子流出的一极为负极
D.发生氧化反应的一极为正极
查看答案和解析>>
科目:高中化学 来源:2015-2016学年内蒙古赤峰二中高一上第二次月考化学试卷(解析版) 题型:选择题
根据下列反应的化学方程式,判断有关物质的还原性强弱顺序是 ( )
①I2 + SO2 + 2H2O = H2SO4 + 2HI;
② 2FeBr2 + Br2 = 2FeBr3;
③2FeCl3 + 2HI = 2FeCl2 + 2HCl+I2
A.SO2>I->Fe2+>Br- B.Br->Fe2+>SO2>I-
C.Fe2+>I->Br->SO2 D.I->Fe2+>Br->SO2
查看答案和解析>>
科目:高中化学 来源:2015-2016学年山西省高一12月月考化学试卷(解析版) 题型:选择题
将Fe、Cu、Fe2+、Fe3+和Cu2+置于同一容器中充分反应,如Fe有剩余,则容器中只能有
A.Cu,Fe3+ B.Fe2+,Fe3+ C.Cu,Cu2+,Fe D.Cu,Fe2+,Fe
查看答案和解析>>
科目:高中化学 来源:2016届福建省高三上12月月考化学试卷(解析版) 题型:选择题
某溶液可能含有Na+、Ag+、Al3+、S2-、CO32-、SO42-、NO3-等离子中的数种。向此溶液中加入稀盐酸,有浅黄色沉淀和气体出现,此溶液的焰色为黄色.根据以上实验现象,下列关于原溶液中离子成分的推测正确的是( )
A.一定有S2-、SO32-、Na+ B.一定没有Ag+、Al3+
C.可能只有Na+、S2-、CO32- D.一定有Na+、S2-、NO3
查看答案和解析>>
科目:高中化学 来源:2015-2016学年安徽省高二上期中测试化学试卷(解析版) 题型:选择题
下列说法中有明显错误的是( )
A、对有气体参加的反应,增大压强,体系体积减小,可使单位体积内活化分子数增加,反应速率增大
B、活化分子之间发生的碰撞一定为有效碰撞
C、升高温度,一般可使活化分子的百分数增大,因而反应速率增大
D、加入适宜的催化剂,可使活化分子的百分数大大增加,从而增大反应速率
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com