
【题目】下列有关概念或原理的叙述正确的是 ( )
A.氨基酸、蛋白质和氧化铝一样既能与酸反应,又能与碱反应,所以它们都是两性氧化物
B.制造婴儿用的一次性纸尿片采用的吸水保水的材料可以是![]()
C.乙烯和聚乙烯都能使酸性![]() 溶液褪色
溶液褪色
D.甲酸乙酯、葡萄糖、麦芽糖、淀粉这四种物质的共同性质是,它们既可以发生水解反应,又可以发生银镜反应
 全优测试卷系列答案
全优测试卷系列答案 冲刺100分1号卷系列答案
冲刺100分1号卷系列答案科目:高中化学 来源: 题型:
【题目】下列图示与对应的叙述相符的是

A.图I表示某吸热反应分别在有、无催化剂的情况下反应过程中的能量变化
B.图Ⅱ表示常温下,0.100 mol/L NaOH溶液滴定20.00 mL、0.100 mol/L HC1溶液所得到的滴定曲线。
C.图Ⅲ表示一定质量的冰醋酸加水稀释过程中,醋酸溶液电离程度:c<a<b
D.图Ⅳ表示反应4CO(g)+2NO2(g)![]() N2(g)+4CO2(g),在其他条件不变的情况下改变起始物CO的物质的量,平衡时N2的体积分数变化情况,由图可知的转化率c>b>a
N2(g)+4CO2(g),在其他条件不变的情况下改变起始物CO的物质的量,平衡时N2的体积分数变化情况,由图可知的转化率c>b>a
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列关于甲、乙、丙、丁四种有机物的说法正确的是

A.分别加入AgNO3溶液,均有沉淀生成
B.加入NaOH溶液共热,然后加入稀硝酸调至酸性,再滴入AgNO3溶液,均有沉淀生成
C.加入NaOH的醇溶液共热,后加入稀硝酸至酸性,再滴入AgNO3溶液,均有沉淀生成
D.乙发生消去反应得到两种烯烃
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温下,将![]() 缓慢通入100mL水中至饱和,然后向所得饱和氯水中逐滴加人
缓慢通入100mL水中至饱和,然后向所得饱和氯水中逐滴加人![]() 溶液,整个过程中pH的变化如图所示,下列有关叙述正确的是( )
溶液,整个过程中pH的变化如图所示,下列有关叙述正确的是( )

A.曲线③④段有离子反应:![]()
B.可依据②处数据计算所溶解的![]()
C.③处表示氯气与氢氧化钠溶液恰好反应完全
D.①处![]() 约为
约为![]() 处
处![]() 的两倍
的两倍
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】烃A是一种重要的化工原料,其产量可以用来衡量一个国家的石油化工发展水平。A可发生如图所示的一系列化学反应,其中①②③属于同种反应类型。根据如图回答下列问题:
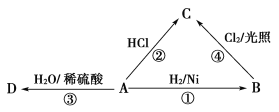
(1)写出A的电子式及空间构型:电子式___,空间构型___。
(2)②、④两种制备氯乙烷的方法中,方法___好。原因是__。
(3)写出③、④两步反应的化学方程式,并注明反应类型:
③___,反应类型___。
④__,反应类型__。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】Ⅰ.如图为原电池装置示意图。
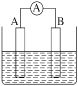
(1)若A为Pb,B为PbO2,电解质为H2SO4溶液,工作时的总反应为Pb+PbO2+2H2SO4=2PbSO4+2H2O,写出B电极反应式:__。该电池在工作时,A电极的质量将___(填“增加”“减小”或“不变”),若该电池反应消耗了0.1molH2SO4,则转移电子的数目为__。
(2)若A、B均为铂片,电解质为KOH溶液,分别从A、B两极通入H2和O2,该电池即为氢氧燃料电池,写出A电极反应式:___。该电池在工作一段时间后,溶液的碱性将___(填“增强”“减弱”或“不变”)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】25℃时,向一定浓度的Na2X溶液中滴入盐酸,溶液的pH与离子浓度变化关系如图所示。

已知:H2X是二元弱酸,Y表示![]() 或
或![]() ,pY=﹣lgY.下列叙述不正确的是( )
,pY=﹣lgY.下列叙述不正确的是( )
A. 曲线n表示pH与p![]() 的变化关系
的变化关系
B. Ka2(H2X)=1.0×10﹣10.3
C. NaHX溶液中c(H+)>c(OH﹣)
D. 当溶液呈中性时,c(Na+)=c(HX﹣)+2c(X2﹣)+c(Cl﹣)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】铜及其化合物有着十分重要的用途:如氨基乙酸铜[结构简式为(H2NCH2COO)2Cu]常用作食品补铜剂及矿物元素饲料添加剂,硒化铜纳米晶在光电转化中有着广泛地应用;硫酸铜可用作配制农药等。
(1)基态硒原子的电子排布式为____,基态氮原子电子的空间运动状态有__种,与硒同周期相邻的三种元素第一电离能由大到小的顺序为______
(2)(H2NCH2COO)2Cu氨基乙酸铜中,碳原子的杂化轨道类型是______;与氮原子成键的原子(含氮原子本身)形成的空间构型是__________。
(3)硫酸铜晶体的组成可表示为[Cu(H2O)4]SO4·H2O,实验测得该物质中存在氢键且水分子成“键”情况与冰中类似,则1mol[Cu(H2O)4]SO4·H2O中氢键数目为__NA。
(4)硫酸铜在高温下分解有可能得到CuO、Cu2O、SO2、SO3等物质,其中CuO的熔点为1026℃。
①CuO的晶体类型是_____,熔点Cu2O>Cu2S的原因是______
②SO2与SO3中,属于非极性分子的是__,SO2在溶剂水与溶剂CCl4中,相同温度能溶解更多SO2的溶剂是___________
③铜的某种氧化物的晶胞如下图所示,则该氧化物的化学式为_______,若组成粒子氧、铜的半径分别为rOpm、rCupm,密度ρg/cm3,阿伏加德罗常数值为NA,则该晶胞的空间利用率为______(用含π的式子表示)。
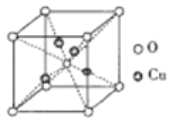
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用如图所示装置制备FeSO4溶液,再与等物质的量的(NH4)2SO4反应,制备硫酸亚铁铵晶体[(NH4)xFe(SO4)y·6H2O]。硫酸亚铁铵晶体在空气中不易被氧化,易溶于水,不溶于乙醇。
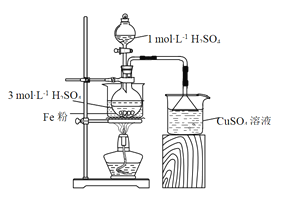
(1)实验装置:反应过程中会产生少量PH3气体,需使用封闭装置。用CuSO4溶液吸收PH3时会生成H3PO4和Cu。该反应的化学方程式为_______。
(2)药品用量:将2 g Fe粉、10 mL 3 mol·L-1 H2SO4溶液加入烧瓶中反应。采取该原料配比的主要原因是_______。
(3)制备FeSO4溶液:保持温度70~80 ℃,至反应无明显气泡产生,停止加热,过滤。
(4)制备(NH4)xFe(SO4)y·6H2O:向FeSO4溶液中加入一定质量的(NH4)2SO4固体,70~80 ℃条件下溶解后,趁热倒入50 mL乙醇中,析出晶体。乙醇的作用为_______。
(5)测定化学式:将一定量(NH4)xFe(SO4)y·6H2O晶体加入到过量NaOH溶液中,并加热,生NH3 1.12 L(标准状况),过滤、洗涤、灼烧,得Fe2O3固体2.0 g。通过计算确定硫酸亚铁铵晶体的化学式。(写出计算过程)_______
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com