
| A. | ②③ | B. | ①③ | C. | ① | D. | ①④⑤ |
分析 ①常温下,c(H+)/c(OH-)=1×10-12的溶液中存在大量氢氧根离子,四种离子之间不反应,都不与氢氧根离子反应;
②加入苯酚显紫色的溶液中存在铁离子,铁离子能够氧化硫离子;
③四种离子之间不反应,为澄清透明溶液;
④使pH试纸变蓝的溶液中存在大量氢氧根离子,铵根离子与氢氧根离子反应;
⑤铝离子与碳酸氢根离子发生双水解反应.
解答 解:①常温下,c(H+)/c(OH-)=1×10-12的溶液中存在大量氢氧根离子,K+、AlO2-、CO32-、Na+之间不发生反应,都不与氢氧根离子反应,在溶液中能够大量共存,故①正确;
②加入苯酚显紫色的溶液中存在铁离子,铁离子能够氧化S2-,在溶液中不能大量共存,故②错误;
③Cu2+、Fe3+、NO3-、Cl-之间不发生反应,为澄清透明溶液,在溶液中能够共存,故③正确;
④使pH试纸变蓝的溶液呈碱性,溶液中存在大量氢氧根离子,NH4+与氢氧根离子反应,在溶液中不能大量共存,故④错误;
⑤Al3+、HCO3-之间发生双水解反应生成氢氧化铝沉淀和二氧化碳气体,在溶液中不能大量共存,故⑤错误;
故选B.
点评 本题考查离子共存的判断,为高考的高频题,题目难度不大,注意明确离子不能大量共存的一般情况:能发生复分解反应的离子之间;能发生氧化还原反应的离子之间等;还应该注意题目所隐含的条件,如:溶液的酸碱性,据此来判断溶液中是否有大量的 H+或OH-;溶液的颜色,如无色时可排除 Cu2+、Fe2+、Fe3+、MnO4-等有色离子的存在;试题侧重对学生基础知识的训练和检验,有利于培养学生灵活运用基础知识解决实际问题的能力.


科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
科目:高中化学 来源: 题型:推断题

 .
. .
. 与过量的
与过量的 也可以发生Reformatsky反应,试写出该生成物的结构简式
也可以发生Reformatsky反应,试写出该生成物的结构简式 .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 常温下pH=4的NaHC2O4溶液中:c(H2C2O4)>c(C2O42-) | |
| B. | 当温度不变时,在纯水中加入强碱溶液不会影响水的离子积常数 | |
| C. | 常温下,向AgCl的饱和溶液中加入NaCl固体,有固体析出,且AgCl的Ksp变小 | |
| D. | 25℃时,Ksp(AgCl)=1.56×10-10,Ksp(Ag2CrO4)=9.0×10-12,向同浓度的Na2CrO4和NaCl混合溶液中滴加AgNO3溶液,Ag2CrO4先析出 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 20% | B. | 40% | C. | 60% | D. | 80% |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
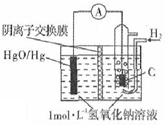 某原电池的装置如图所示,总反应为H2(g)+HgO(s)=H20(1)+Hg(1),其中阴离子交换膜只允许阴离子和水分子通过.下列说法正确的是( )
某原电池的装置如图所示,总反应为H2(g)+HgO(s)=H20(1)+Hg(1),其中阴离子交换膜只允许阴离子和水分子通过.下列说法正确的是( )| A. | 正极反应为:HgO(s)-2e-+H20=Hg(l)+2OH- | |
| B. | 放电结束后,溶液中的pH值下降 | |
| C. | 每反应2.24L氢气,交换膜通过0.2mol离子 | |
| D. | 电子通过离子交换膜从负极向正极移动,保持溶液中电荷平衡 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 2N5 →5N2是化学变化 | B. | N5和N2互为同位素 | ||
| C. | 原子半径:r(N)<r(O) | D. | 18O2中含18个中子 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 7.8gNa2O2中所含有的阴离子数目是0.2NA | |
| B. | 标准状况下,2.24L18O2中含有的中子的数目是NA | |
| C. | 在20℃、1.01×105 Pa时,2.8g C2H4和CO的混合气体含气体分子数是0.1 NA | |
| D. | 标准状况下,a L CH4和a L C6H14中所含分子数均约为$\frac{a{N}_{A}}{22.4}$ |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com