
| A.CCl4和SiCl4的熔点 |
B.邻羟基苯甲醛(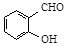 )和对羟基苯甲醛( )和对羟基苯甲醛(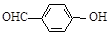 )的沸点 )的沸点 |
| C.SO2和CO2在水中的溶解度 |
| D.H2SO3和H2SO4的酸性 |
科目:高中化学 来源:不详 题型:单选题
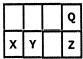
| A.最高价氧化物对应水化物的酸性Z>Y |
| B.原子半径X>Y |
| C.一定条件下,Q可分别与X、Y、Z形成化合物,这些化合物都可溶于NaOH溶液 |
| D.元素Y的氧化物是形成酸雨的罪魁祸首 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.沸点:H2O>H2S>H2Se>H2Te | B.稳定性:SiH4>PH3>H2S >HCl |
| C.熔点:SiC >KCl> I2>CO2 | D.沸点:CH4 >SiH4>GeH4>SnH4 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
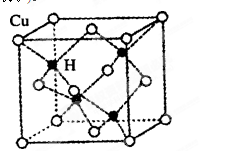
查看答案和解析>>
科目:高中化学 来源:不详 题型:问答题
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
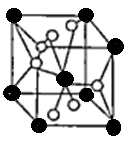
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.主族元素的原子核外电子最后填入的能级是d能级或f能级 |
| B.镁型和铜型金属晶体的配位数均为12 |
| C.中心原子上的孤电子对不参与决定分子的空间结构 |
| D.分子中键角越大,价电子对相互排斥力越大,分子越稳定 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
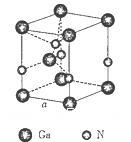
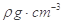 。列出计算氮化镓晶胞边长a的表达式:a=_______cm。
。列出计算氮化镓晶胞边长a的表达式:a=_______cm。查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com