
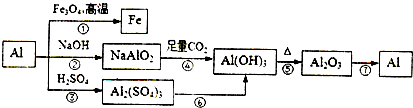
| A、反应①又称铝热反应,可用于野外焊接铁轨 | B、反应②、③都有氢气生成,产生等量的氢气时转移的电子数相等 | C、常用反应⑥制备Al(OH)3,方法是向Al2(SO4)3溶液中滴加足量的NaOH溶液 | D、工业上用反应⑦制备铝时,常加入冰晶石以降低氧化铝的熔融温度 |


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
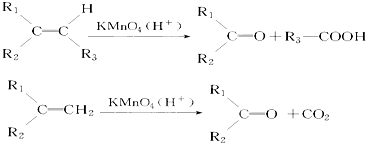
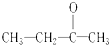 ),则此烯烃的结构简式是
),则此烯烃的结构简式是查看答案和解析>>
科目:高中化学 来源: 题型:
| A、主族金属单质与酸溶液反应置换出氢气的能力一定比过渡金属单质强 | B、第二周期元素的原子形成的阴离子半径随核电荷数的增大而增大 | C、同周期主族元素的原子形成简单离子的电子层结构相同 | D、元素原子的最外层电子数的多少与其非金属性的强弱无必然联系 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、无水醋酸铯的化学式为CH3COOCs,易溶于水,其水溶液显碱性 | B、碳酸氢铯加热即分解生成碳酸铯、二氧化碳和水 | C、在Na、K、Rb、Cs中,Cs熔点最高,密度最大 | D、CsH是离子化合物,与水反应可以生成H2 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、小苏打可与酸反应,可用作治疗胃酸过多的药剂 | B、氯化铝是电解质,可电解其水溶液获得金属铝 | C、SO2具有漂白性,可用于将银耳漂白为“雪耳” | D、二氧化硅具有导电性,可用于生产光导纤维 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、SiO2既能与HF溶液反应,又能与NaOH溶液反应,说明SiO2是两性氧化物 | B、鸡蛋清溶液中加入饱和(NH4)2SO4溶液有白色沉淀产生,说明蛋白质发生了变性 | C、将少量某有机物滴加到新制氢氧化铜中,充分振荡,未见砖红色沉淀生成,说明该有机物不含醛基 | D、相同体积pH均为3的HA和HB两种酸分别与足量的锌充分反应,HA放出的氢气多,说明HB的酸性比HA的酸性强 |
查看答案和解析>>
科目:高中化学 来源:2015届广东省湛江市高三第一次月考理综化学试卷(解析版) 题型:选择题
用NA表示阿伏加德罗常数的值。下列叙述中正确的是
A.78 g 苯含有碳碳双键的数目为3NA
B.常温常压下,22.4 L二氧化碳含有的原子总数为3NA
C.1 L 1 mol·L-1的NaClO 溶液中含有ClO-的数目为NA
D.1 mol Fe与足量稀HNO3反应,转移3 NA个电子
查看答案和解析>>
科目:高中化学 来源:2015届广东省广州市高三9月第二次月考化学试卷(解析版) 题型:选择题
(15分)化合物G的合成路线如下:
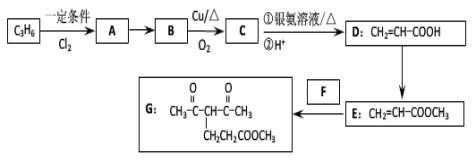
(1)D中含氧官能团的名称为 ,1 molG发生加成反应最多消耗 mol H2 。
(2)去掉E中含有少量D的试剂和操作是 ;下列有关E的说法正确的是 (填字母序号)。
A.可发生氧化反应B.催化条件下可发生缩聚反应
C.可发生取代反应D.是CH2=CHCOOCH2CH3的同系物
E.易溶于水
(3)写出A→B的化学反应方程式:
(4)反应E + F→G属于下列麦克尔加成反应类型,则F的结构简式为 。
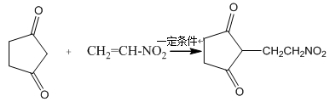
(5)比G少2个氢原子的物质具有下列性质:任写一种该物质的结构简式 。
①遇FeCl3溶液显紫色; ②苯环上的一氯取代物只有一种;
③1mol物质最多可消耗2mol Na和1mol NaOH。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com