
【题目】已知:在一定温度下,H2(g)+I2(g)2HI(g)的平衡常数为K1; ![]() H2(g)+
H2(g)+ ![]() I2(g)HI(g)的平衡常数为K2 , 则K1、K2的关系为( )
I2(g)HI(g)的平衡常数为K2 , 则K1、K2的关系为( )
A.K1=K2
B.K1=2K2
C.K1=1/2K2
D.K1=K22
科目:高中化学 来源: 题型:
【题目】乙二酸﹣1,4﹣环己二醇酯可以通过下列路线合成.请回答下列问题: 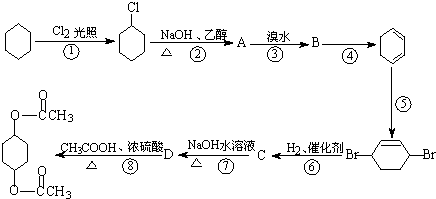
(1)上述反应①﹣④中,属于取代反应的有(填序号);
反应⑥﹣⑧中,属于加成反应的有(填序号).
(2)写出下列物质的结构简式:B , C .
(3)写出下列反应的方程式:
反应②:;
反应⑦: .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知H2(g)+ ![]() O2(g)═H2O(g)△H=﹣241.8kJmol﹣1 . 下列说法中不正确的是( )
O2(g)═H2O(g)△H=﹣241.8kJmol﹣1 . 下列说法中不正确的是( )
A.H2的燃烧热为241.8 kJmol﹣1
B.2H2(g)+O2(g)═2H2O(g)△H=﹣483.6 kJmol﹣1
C.1 mol H2完全燃烧生成液态水放出的热量大于241.8 kJ
D.断开1 mol H2O的化学键吸收的总能量大于断裂1 mol H2和0.5 mol O2的化学键所吸收的总能量
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】化学与社会、生产和生活密切相关。下列说法错误的是
A.科学家在室温下将气态二氧化碳转化为固体碳材料,该变化是化学变化
B.我国科学家合成了钛掺杂、镧镍锂氧化物正极材料,涉及的金属元素都是过渡元素
C.“辽宁舰”上用于舰载机降落拦阻索的特种钢缆,属于新型无机金属材料
D.看电影时,我们可以看到放映机投射的光柱,这是气溶胶发生的丁达尔现象
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列关于胶体的说法不正确的是 ( )
A. 制备Fe(OH)3胶体后可以用渗析的方法净化
B. 利用丁达尔效应可以区分溶液和胶体
C. 电泳现象可证明胶体都带电
D. 胶体是分散质粒子直径在1 nm~100 nm之间的分散系
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某课外小组研究铝土矿中Al2O3的含量。已知铝土矿的主要成分是Al2O3,杂质有Fe2O3、SiO2等。从铝土矿中提取Al2O3的流程如下:
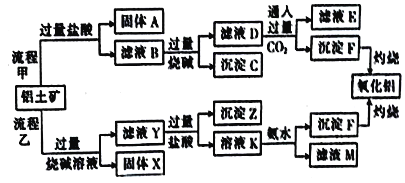
(1)固体A是_______________(填化学式)。
(2)流程甲中加入盐酸后生成Fe3+的离子方程式为___________________________。
(3)沉淀F转化为氧化铝的化学方程式是________________________________。
(4)流程乙中,由溶液K生成沉淀F的离子方程式是________________________________。
(5)工业上用Al2O3与C、Cl2在高温条件下反应制取AlCl3,每消耗0.5mol碳单质,转移1mol电子,该反应的化学方程式是_____________________。
(6)流程乙中,将实验过程中所得固体精确称量,课外小组发现所得氢氧化铝固体的质量与原铝土矿质量相等,则该铅土矿中Al2O3的质量分数是______(保留一位小数,可能用到的相对原子质量:H-1,O-16,A1-27)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】北京时间11月1日清晨5时58分07秒,中国“长征二号F”遥八运载火箭在酒泉卫星发射中心载人航天发射场点火发射,火箭的第三级使用的推进剂是液氢和液氧。
已知下面在298K时的热化学方程式:
2H2(g)+O2(g)== 2H2O(l) ΔH=-571.6 kJ·mol-1
CH4(g)+2O2(g)==CO2(g)+2H2O (l)ΔH=-890.3 kJ·mol-1
C(s)+O2(g)== CO2(g)ΔH=-393.5 kJ·mol-1
根据上面的热化学方程式完成下列问题:
(1)通过计算说明等质量的H2、C、CH4完全燃烧时放出热量最多的是_________。
(2)根据以上反应,则C(s)+2H2(g)== CH4(g)的焓变ΔH=________________。
(3)已知H2O(l)== H2O(g) ΔH=+44.0 kJ·mol-1
试写出甲烷燃烧生成二氧化碳和水蒸气的热化学方程式:________________
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com