
有机物甲的分子式为C5H10O2,已知:①甲可以发生银镜反应;②甲是具有水果香味的物质;③在酸性或碱性条件下甲可以发生水解反应;则甲的可能结构有
A.1种 B.2种 C.3种 D.4种
 提分百分百检测卷单元期末测试卷系列答案
提分百分百检测卷单元期末测试卷系列答案 小学期末标准试卷系列答案
小学期末标准试卷系列答案科目:高中化学 来源:2015-2016学年河北省高二上二调考试化学试卷(解析版) 题型:选择题
用pH试纸测定某溶液的pH,如果先将pH试纸用蒸馏水润湿后,再把待测液滴到pH试纸上,跟比色卡对照,溶液的pH测得值为8,则该溶液的实际pH
A.大于8 B.小于8 C.等于8 D.小于7
查看答案和解析>>
科目:高中化学 来源:2016届浙江绍兴市高三上学期期中考试化学试卷(解析版) 题型:选择题
下列各组物质的性质比较,正确的是
A.熔点:CO2<H2O<SiO2<KCl B.稳定性:H2O<NH3<PH3<SiH4
C.酸性:H3PO4>H2SO4>HClO4>H2SiO3 D.粒子半径:K+>Na+>Mg2+>Al3+
查看答案和解析>>
科目:高中化学 来源:2016届安徽省高三上第四次段考化学试卷(解析版) 题型:选择题
某溶液中含有HCO、SO、CO、CH3COO-四种阴离子,向其中加入足量的Na2O2固体后,溶液中离子浓度基本保持不变的是(假设溶液体积无变化)( )
A. CH3COO- B. SO C. CO D. HCO
查看答案和解析>>
科目:高中化学 来源:2016届江西师大附中,九江一中高三上期中化学试卷(解析版) 题型:选择题
下列各组溶液,不用外加试剂,就能实现鉴别的是( )
① CuSO4 K2SO4 KNO3 KOH
② Na2CO3 BaCl2 HCl Na2SO4
③ NH4NO3 Na2SO4 Ba(OH)2 AlCl3
④ NaAlO2 Na2SiO3 H2SO4 NaCl
A. ①③ B. ②④ C. ①③④ D. ②③④
查看答案和解析>>
科目:高中化学 来源:2016届福建省高三上学期期中考试化学试卷(解析版) 题型:推断题
A、B、C、D、E为原子序数递增的短周期元素,在周期表中A是原子半径最小的元素,B、C左右相邻,C、D同主族,D和E的气态氢化物具有相同的电子数,C的单质只有氧化性。
(1)写出实验室制取E2反应的离子方程式_______________________________;
(2)A、C元素按原子个数比为1:1形成化合物的电子式_________________;
(3)某小组设计如图所示的装置(图中夹持和加热装置略去),分别研究DC2和E2的性质.
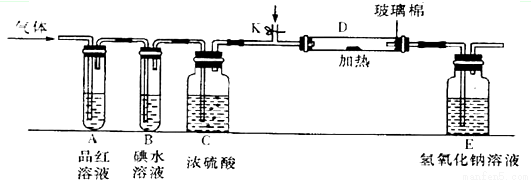
①分别通入DC2和E2,在装置A中观察到的现象是否相同(填“相同”或“不相同”)________;若装置D中装的是铁粉,当通入E2时D中观察到的现象为____________;若装置D中装的是五氧化二钒,当通入DC2时,打开K通入适量C2,化学反应方程式为________________________________。
②若装置B中装有5.0mL l.0×10-3mol/L的碘水,当通入足量E2完全反应后,转 移了5.0×10-5mol电子,则该反应的化学方程式为_______________________________。
(4)某同学将足量的DC2通入一支装有氯化钡溶液的试管,未见沉淀生成,向该试管中加入过量(填字母)_________,可以看到白色沉淀生成;
A、氨水 B、稀盐酸 C、稀硝酸 D、氯化钙
(5)若由元素D和C组成一2价酸根Z,Z中D和C的质量比为D:C=4:3,当E2与含Z的溶液完全反应后,有浅黄色沉淀产生,取上层清液加入氯化铡溶液,有白色沉淀产生.与出E2与Z的溶液完全反应产生浅黄色沉淀的离子方程式______________________________。
(6)A、B、C三种元素组成的碱性物质N,A、B、C、D和一种常见金属元素组成相对分子质量为392的化合物M,1molM中含有6mol结晶水,对化合物M进行如下实验:
a.取含有0.1molM的溶液加入过量浓NaOH溶液并加热,产生白色沉淀和4.48L(标况)无色刺激性气味气体,经一段时间白色沉淀变为灰绿色,最终变为红褪色;
b.另以含有0.1molM的溶液,加入过量BaCl2溶液产生46.6g白色沉淀,加盐酸沉淀不溶解。
①M的化学式为____________________________。
②在25℃下,测定浓度均为amol/L的化合物N和M的混合溶液pH=7,且含金属离子的浓度为bmol/L,则溶液里除H+、金属阳离子外的阳离子浓度为__________mol/L。
查看答案和解析>>
科目:高中化学 来源:2016届安徽马鞍山、淮北、铜陵四校高三上第三次联考化学试卷(解析版) 题型:实验题
在无机化工中,硫酸亚铁铵[(NH4)2Fe(SO4)2]是制取其它铁系化合物的原料,如制取氧化伯系颜料、磁性材料和黄血盐等。某化学兴趣小组设计如下实验方案,探究(NH4)2Fe(SO4)2完全分解的产物。
已知:①隔绝空气受热完全分解是氧化还原反应。
②98%浓硫酸能顺利吸收SO3。
Ⅰ.甲同学根据以下流程探究分解的部分产物,试回答下列问题:
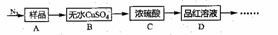
(1)B装置预期的现象是_____;C装置的作用可能是______,D装置可以检验分解产物中是否含有_____。
(2)加热前先通一会儿N2,再关闭气阀,其目的是_______。
Ⅱ.乙同学猜想(NH4)2Fe(SO4)2分解时可能生成了SO3,为了验证他的猜想,小组同学又提供了如右图装置,试回答下列问题:
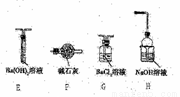
(3)不能选择E和F装置的原因是________。
(4)加热装置A与G、H连接并进行实验,请你提出需要改进的方案________。
(5)已知饱和SO2水溶液中c(SO32-)=6.0×10-8mol•L-1,Ksp(BaSO3)=5.4×10-7。通过计算判断在1.0mol•L-1的BaCl2溶液中,通入足量纯净的SO2能否生成BaSO3沉淀?
(6)当G中出现大量白色沉淀时,并不能说明A中生成了SO3,理由是_______;为了进一步证明是否有SO3生成,请你补充实验方案(不要求写具体的操作过程)_________。
查看答案和解析>>
科目:高中化学 来源:2016届福建省高三上学期期中测试化学试卷(解析版) 题型:选择题
一定是的CuS和Cu2S的混合物投入足量的HNO3中,收集到气体VL(标准状况),向反应后的溶液中(存在Cu2+和SO42-)加入足量NaOH,产生蓝色沉淀,过滤,洗涤,灼烧,得到CuO12.0g,若上述气体为NO和NO2的混合物,且体积比为1﹕1,则V可能为( )
A.13.5L B.9.0L C.16.8L D.15.7L
查看答案和解析>>
科目:高中化学 来源:2015-2016学年湖南常德石门第一中学高二上期中文化学卷(解析版) 题型:选择题
果汁是人们喜爱的饮料,由于其中含有Fe2+,在榨取后不久往往会变为棕黄色,生产上常在其中加入维生素C以防止其变色,这是利用了维生素C的
A.氧化性 B.还原性 C.酸性 D.碱性
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com