
有机物A是农药生产中的一种中间体,结构简式如下图所示。下列叙述中正确的是( )
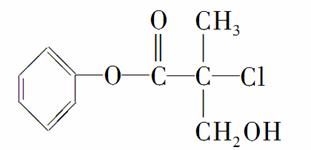
A.1 mol A最多能与4 mol H2发生加成反应
B.有机物A可以在一定条件下与HBr发生反应
C.有机物A与浓硫酸混合加热,可以发生消去反应
D.1 mol A与足量的NaOH溶液反应,最多可以消耗2 mol NaOH
科目:高中化学 来源: 题型:
碘及其化合物在合成杀菌剂、药物等方面具有广泛用途。回答下列问题:
(1)大量的碘富集在海藻中,用水浸取后浓缩,再向浓缩液中加MnO2和H2SO4,即可得到I2,该反应的还原产物为____________。
(2)上述浓缩液中含有I-、Cl-等离子,取一定量的浓缩液,向其中滴加AgNO3溶液,当AgCl开始沉淀时,溶液中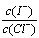 为:_____________,已知Ksp(AgCl)=1.8×10-10,Ksp(AgI)=8.5×10-17。
为:_____________,已知Ksp(AgCl)=1.8×10-10,Ksp(AgI)=8.5×10-17。
(3)已知反应2HI(g) ===H2(g) + I2(g)的ΔH= +11kJ·mol-1,1mol H2(g)、1mol I2(g)分子中化学键断裂时分别需要吸收436kJ、151kJ的能量,则1molHI(g)分子中化学键断裂时需吸收的能量为______________kJ。
(4)Bodensteins研究了下列反应:
2HI(g) H2(g) + I2(g)
H2(g) + I2(g)
在716K时,气体混合物中碘化氢的物质的量分数x(HI)与反应时间t的关系如下表:
| t/min | 0 | 20 | 40 | 60 | 80 | 120 |
| x(HI) | 1 | 0.91 | 0.85 | 0.815 | 0.795 | 0.784 |
| x(HI) | 0 | 0.60 | 0. | 0.773 | 0.780 | 0.784 |
① 根据上述实验结果,该反应的平衡常数K的计算式为:___________。
② 上述反应中,正反应速率为v正= k正·x2(HI),逆反应速率为v逆=k逆·x(H2)·x(I2),其中k正、k逆为速率常数,则k逆为________(以K和k正表示)。若k正 = 0.0027min-1,在t=40min时,v正=__________min-1
③ 由上述实验数据计算得到v正~x(HI)和v逆~x(H2)的关系可用下图表示。当升高到某一温度时,反应重新达到平衡,相应的点分别为_________________(填字母)

查看答案和解析>>
科目:高中化学 来源: 题型:
下列叙述中正确的是( )
A.在稀溶液中,1 mol酸和1 mol碱完全反应所放出的热量,叫做中和热
B.在101 kPa时,1 mol物质燃烧时所放出的热量叫做该物质的燃烧热
C.热化学方程式中,各物质前的化学计量数不表示分子个数
D.如果反应物所具有的总能量小于生成物所具有的总能量,则发生的反应是放热反应
查看答案和解析>>
科目:高中化学 来源: 题型:
碘及其化合物在合成杀菌剂、药物等方面具有广泛用途。回答下列问题:
(1)大量的碘富集在海藻中,用水浸取后浓缩,再向浓缩液中加MnO2和H2SO4,即可得到I2,该反应的还原产物为____________。
(2)上述浓缩液中含有I-、Cl-等离子,取一定量的浓缩液,向其中滴加AgNO3溶液,当AgCl开始沉淀时,溶液中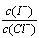 为:_____________,已知Ksp(AgCl)=1.8×10-10,Ksp(AgI)=8.5×10-17。
为:_____________,已知Ksp(AgCl)=1.8×10-10,Ksp(AgI)=8.5×10-17。
(3)已知反应2HI(g) ===H2(g) + I2(g)的ΔH= +11kJ·mol-1,1mol H2(g)、1mol I2(g)分子中化学键断裂时分别需要吸收436kJ、151kJ的能量,则1molHI(g)分子中化学键断裂时需吸收的能量为______________kJ。
(4)Bodensteins研究了下列反应:
2HI(g) H2(g) + I2(g)
H2(g) + I2(g)
在716K时,气体混合物中碘化氢的物质的量分数x(HI)与反应时间t的关系如下表:
| t/min | 0 | 20 | 40 | 60 | 80 | 120 |
| x(HI) | 1 | 0.91 | 0.85 | 0.815 | 0.795 | 0.784 |
| x(HI) | 0 | 0.60 | 0.73 | 0.773 | 0.780 | 0.784 |
① 根据上述实验结果,该反应的平衡常数K的计算式为:___________。
② 上述反应中,正反应速率为v正= k正·x2(HI),逆反应速率为v逆=k逆·x(H2)·x(I2),其中k正、k逆为速率常数,则k逆为________(以K和k正表示)。若k正 = 0.0027min-1,在t=40min时,v正=__________min-1
③ 由上述实验数据计算得到v正~x(HI)和v逆~x(H2)的关系可用下图表示。当升高到某一温度时,反应重新达到平衡,相应的点分别为_________________(填字母)

查看答案和解析>>
科目:高中化学 来源: 题型:
下列有关有机物的说法正确的是( )
A.甲烷、乙烯、苯分子中所有原子都在同一平面上
B.淀粉和纤维素的化学式都是(C6H10O5)n,因此它们互为同分异构体
C.煤井中的瓦斯气和家庭使用的液化石油气的主要成分都是甲烷
D.乙醇、乙酸和乙酸乙酯能用饱和Na2CO3溶液鉴别
查看答案和解析>>
科目:高中化学 来源: 题型:
下列实验方案中,合理的是( )
A.可用生石灰除去乙酸中少量水
B.用5 mL苯与1 mL浓溴水反应(Fe粉做催化剂)制溴苯
C.向适量浓硝酸、浓硫酸的混合物中逐滴加入苯,在50~60℃的水浴中加热以制取硝基苯
D.将2.5 g苯酚、2.5 mL 40%的甲醛溶液混合,沸水浴加热制酚醛树脂
查看答案和解析>>
科目:高中化学 来源: 题型:
有机物X是淀粉水解的最终产物;Y俗名酒精;Z是一种植物生长调节剂,可以把果实催熟,在催化剂作用下,Z可以制得重要的 包装材料P。请回答下列问题:
包装材料P。请回答下列问题:
(1)X的分子式为________。
(2)物质Z生成化合物CH3CHO是原子利用率100%的反应,所需另一反应物的名称为________。
(3)Y+Na―→Q反应的化学方程式为____________________。
(4)Z―→P反应的化学方程式为_________________________,
属________反应。
(5)Y与酸性高锰酸钾溶液反应可生成W,在加热和浓H2SO4的作用下,Y与W反应可生成一种有香味的物质I。若60 g W与足量的Y反应能生成53 g I,计算该反应中W的转化率(要求写出计算过程)。
查看答案和解析>>
科目:高中化学 来源: 题型:
已知NaNO2的化学式量为69,则500mL 1.0 mol·L-1 NaNO2溶液含有溶质质量为( )。
A.13.8g B.69g C.34.5g D.138g
查看答案和解析>>
科目:高中化学 来源: 题型:
下列说法中,正确的是( )。
A.铅笔芯的主要成分是金属铅,儿童在使用是不可用嘴吮吸,以免引起铅中毒
B.CO气体有毒,在生有炉火的居室中多放几盆水,可吸收CO,防止煤气中毒
C.含氟冰箱产生的氟利昂是造成臭氧空洞的主要原因
D.油条制作中常加入明矾作膨化剂,有利于补充身体所需微量元素,是理想的早餐
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com