
����Ŀ��ij�¶��£��ڼס��ҡ��������ĸ������ܱ�������Ͷ��H2��I2��������Ӧ:H2(g)+I2(g) ![]() 2HI(g)����Ӧ��ϵ�и�����Ũ�ȵ��й��������¡�
2HI(g)����Ӧ��ϵ�и�����Ũ�ȵ��й��������¡�
���� | ��ʼŨ�� | ƽ��Ũ�� | |
c(H2)/(mol��L-1) | c(I2)/(mol��L-1) | c(HI)/(mol��L-1) | |
�� | 0.01 | 0.01 | 0.004 |
�� | 0.01 | 0.02 | a |
�� | 0.02 | 0.01 | b |
�� | 0.02 | 0.02 | c |
�����жϲ���ȷ����
A. HI��ƽ��Ũ��:a=b>0.004��c=0.008 B. ƽ��ʱ��H2��ת����:��>��
C. ƽ��ʱ������H2��ת���ʴ���20% D. ���������£��÷�Ӧ��ƽ�ⳣ��K=0.25
���𰸡�B
��������
ij�¶��£���ӦH2��g��+I2��g��![]() 2HI��g������Ӧǰ������������䣬����ѹǿ���ı仯ѧƽ�⣬A���ס��ұȽϣ����е��Ũ�ȴٽ�������ת�����ס����Ƚϣ���������Ũ�ȴٽ��ⵥ��ת����B���ס����Ƚϣ���ʼ���ʵ���Ϊ2����ϵ�������ʵ����ȵ��ڻ�ѧ������֮�ȣ�����ѹǿƽ�ⲻ�ƶ���C���ɼ������ݿ�֪����������ת����Ϊ0.004��0.5/0.01��100%=20%�����ס��ұȽϣ����е��Ũ�ȴٽ�������ת����D���ס����¶���ͬ��K��ͬ����ϱ��������ݿ�֪��K=(0.04)2/(0.01-0.002)(0.01-0.002)=0.25��
2HI��g������Ӧǰ������������䣬����ѹǿ���ı仯ѧƽ�⣬A���ס��ұȽϣ����е��Ũ�ȴٽ�������ת�����ס����Ƚϣ���������Ũ�ȴٽ��ⵥ��ת����B���ס����Ƚϣ���ʼ���ʵ���Ϊ2����ϵ�������ʵ����ȵ��ڻ�ѧ������֮�ȣ�����ѹǿƽ�ⲻ�ƶ���C���ɼ������ݿ�֪����������ת����Ϊ0.004��0.5/0.01��100%=20%�����ס��ұȽϣ����е��Ũ�ȴٽ�������ת����D���ס����¶���ͬ��K��ͬ����ϱ��������ݿ�֪��K=(0.04)2/(0.01-0.002)(0.01-0.002)=0.25��
A���ס��ұȽϣ����е��Ũ�ȴٽ�������ת�����ס����Ƚϣ���������Ũ�ȴٽ��ⵥ��ת�����ұ��ﵽ��ͬƽ��״̬����HI��ƽ��Ũ�ȣ�a=b��0.004����ӦH2��g��+I2��g��![]() 2HI��g������Ӧǰ������������䣬��Ͷ���Ǽ�2����c=0.008����A��ȷ��B���ס����Ƚϣ���ʼ���ʵ���Ϊ2����ϵ�������ʵ����ȵ��ڻ�ѧ������֮�ȣ�����ѹǿƽ�ⲻ�ƶ�����ƽ��ʱ��H2��ת���ʣ���=������B����C���ɼ������ݿ�֪����������ת����Ϊ0.004��1/(2��0.01)��100%=20%�����ס��ұȽϣ����е��Ũ�ȴٽ�������ת������C��ȷ��D���ס����¶���ͬ��K��ͬ����ϱ��������ݿ�֪��K=(0.04)2/(0.01-0.002)(0.01-0.002)=0.25����D��ȷ����ѡB��
2HI��g������Ӧǰ������������䣬��Ͷ���Ǽ�2����c=0.008����A��ȷ��B���ס����Ƚϣ���ʼ���ʵ���Ϊ2����ϵ�������ʵ����ȵ��ڻ�ѧ������֮�ȣ�����ѹǿƽ�ⲻ�ƶ�����ƽ��ʱ��H2��ת���ʣ���=������B����C���ɼ������ݿ�֪����������ת����Ϊ0.004��1/(2��0.01)��100%=20%�����ס��ұȽϣ����е��Ũ�ȴٽ�������ת������C��ȷ��D���ס����¶���ͬ��K��ͬ����ϱ��������ݿ�֪��K=(0.04)2/(0.01-0.002)(0.01-0.002)=0.25����D��ȷ����ѡB��



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ʵ���ұ����������ʵķ����У�����ȷ����
A.���������Ʊ�����ú����
B.�ռ���Һʢװ��ʹ�ò��������Լ�ƿ��
C.FeSO4��Һ����ڼ����������۵��Լ�ƿ��
D.������ˮͨ����������ɫ�Լ�ƿ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ú��ʯ���п�������������ԭ��A��H����֪A��ʯ���ѽ�������Ҫ����֮һ��������Ǻ���һ������ʯ�ͻ�����չˮƽ�ı�־��H��һ�ֱ�ˮ�����״Һ�壬H����̼������Ԫ����ɣ�H����ʹ����KMnO4��Һ��ɫ����̼Ԫ������Ԫ�ص�������Ϊ12:1��H����Է�������Ϊ78���������л���A��G֮���ת����ϵ��
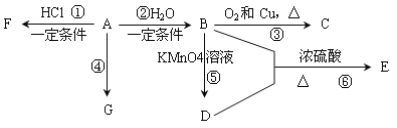
��ش��������⣺
��1��E�����������ŵ�������___________________________��
��2��д����Ӧ�۵Ļ�ѧ����ʽ_____________________________________________��
��3��G��һ�ָ߷��ӻ������������������ְ�װ���Ϻ�ũ�ñ�Ĥ���ϵȣ���ṹ��ʽ��______________________��
��4�����������������У����˶�Ա������˻�Ť��ʱ�����ҽ�������������˲�λ��������F(�е�12.27��)����Ӧ��������д����A�Ʊ�F�Ļ�ѧ����ʽ��_______________��
��5����������A��H��ȫȼ��ʱ����O2�����ʵ���_______(�A>H��A<H��A��H��)��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����֪![]() ��Ϊͬ���칹�壬����˵������ȷ����
��Ϊͬ���칹�壬����˵������ȷ����
A. z�Ķ��ȴ���������
B. x��y��һ�ȴ����ֻ������
C. x��y ��ʹ������Ȼ�̼��Һ�����ӳɷ�Ӧ����ɫ
D. x��y��z��ֻ��x������ԭ�ӿ��ܴ���ͬһƽ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ͨ����ú���ۺ����ã����Ի�ö����л��������A����̼���⡢��3��Ԫ�أ�����������12��3��8��Һ̬��B��һ����Ҫ�Ļ���ԭ�ϣ���Ħ������Ϊ78 gmol-1��E���з�����ζ����������֮���ת����ϵ���£�������ͬ�����ŵ��л���ͨ���������ƵĻ�ѧ���ʣ���
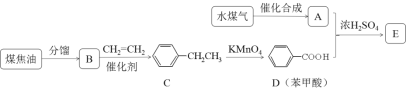
��ش�
(1)������A����������������_____________��
(2)B��CH2=CH2��Ӧ����C�ķ�Ӧ������_____________��
(3)E������������Һ��ˮ��Ļ�ѧ����ʽ��_____________��
(4)����˵����ȷ����_____________��
A.��ͭ˿�ڿ��������պ�Ѹ�ٲ���A�У���Ӧ��Σ��ɵõ��ܷ���������Ӧ������
B.��һ�������£�C��ͨ��ȡ����Ӧת��Ϊ![]()
C.�������ƣ�����������������ͨ��D���������Ʒ�Ӧ�õ�
D.��a mol��B ��D���������������ȫȼ�գ�������������7.5a mol
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ZnO��ҽҩ��ʯ���������й㷺����;���о�С����ij��п��(��Ҫ�ɷ�ZnS������FeS��SiO2��MnCO3������)�Ʊ�����п�����ʣ������������:
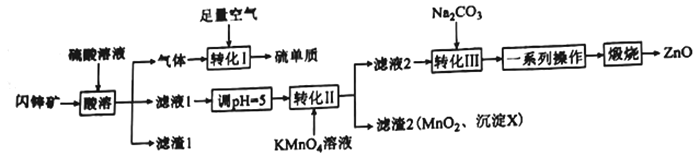
��ش���������:
��1������1�Ļ�ѧʽΪ____________________����дһ�ָ����ʵ���:______________________��
��2������X�Ļ�ѧʽΪ_______________________________��
��3����ת��I�����������ͻ�ԭ�������ʵ���֮��Ϊ________________________��
��4����ת��II������Ҫ��Ӧ�����ӷ���ʽΪ_____________________________________��
��5����Ksp(ZnCO3)=1.5��10-10����Һ������Ũ����1.0��10-5 mol/Lʱ����Ϊ�����ӳ�����ȫ������ʹ1 L c(Zn2+)=1.5 mol/L��Һ��Zn2+������ȫ�������������Na2CO3��Һ�����ʵ���Ũ������Ϊ____________________(�г�����ʽ����Һ���ʱ����仯���Բ���)��
��6����һϵ�в������������ˡ�ϴ�ӡ�����������õIJ���������___________________________��ϴ�ӳ����IJ���Ϊ______________________________________________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����ܱ������н��з�Ӧ2SO2��O2![]() 2SO3����Ӧ��ƽ��ı�־��
2SO3����Ӧ��ƽ��ı�־��
�ٵ�λʱ��������2 mol SO2��ͬʱ����2 mol SO3
�ڷ�Ӧ������У�SO2��O2��SO3�����ʵ���֮��Ϊ2��1��2
�۷�Ӧ������У�SO3�������������ٸı�
A. �٢�B. �٢�C. ��D. ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ij�¶��¿��淴Ӧ��Fe2(SO4)3��6KSCN![]() 2Fe(SCN)3��3K2SO4�ﵽƽ��״̬������������к��ֹ������ʣ���ƽ�⼸���������ƶ�( )
2Fe(SCN)3��3K2SO4�ﵽƽ��״̬������������к��ֹ������ʣ���ƽ�⼸���������ƶ�( )
A. NH4SCN B. K2SO4 C. NaOH D. FeCl3��6H2O
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ij��ѧ��ȤС�飬������ͼ��ʾװ��̽��Ԫ�طǽ�����ǿ���ı仯���ɡ�
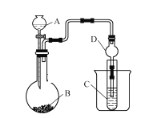
��1������A������Ϊ_________�������D��������_____��
��2��ʵ����������ҩƷNa2S��Ũ���ᡢϡ���ᡢMnO2����ѡ�����ҩƷ���ʵ��̽���Ⱥ���ķǽ�����ǿ������Ҫʱ���Լ��ȣ�ͼ��ʡ�ԣ���
��װ��A����װҩƷΪ_________��
��װ��C�е�ʵ������Ϊ���е���ɫ�������ɣ���װ���еĻ�ѧ��Ӧ����ʽΪ__________��
�۸��ݸ�ʵ��̽�����Ľ������֪HCl���ȶ��Ա�H2S���ȶ���____��������ǿ������������
��3����Ҫ̽�����̼Ԫ�صķǽ�����ǿ����B��C����װҩƷ�ֱ�ΪNa2CO3���塢����ʯ��ˮ����A�з�Ӧ�����ӷ���ʽΪ__________���۲쵽Cװ���е�����Ϊ_________��
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com