
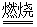 2NaAlO2+CO2������ش�
2NaAlO2+CO2������ش� ���ټ�������������δ��������Ba2+����������Ա��κ�ķ�ˮ��Ba2+��Ũ��Ӧ��С�� mol/L��������ˮ�������ܴﵽ�����ŷű���
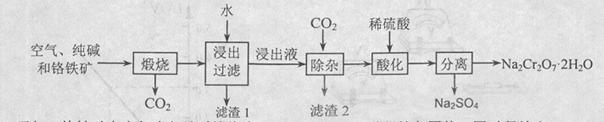
���ټ�������������δ��������Ba2+����������Ա��κ�ķ�ˮ��Ba2+��Ũ��Ӧ��С�� mol/L��������ˮ�������ܴﵽ�����ŷű���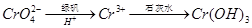 ��д������������ CrO42�����̷�����Һ�з�Ӧ�����ӷ���ʽ ��
��д������������ CrO42�����̷�����Һ�з�Ӧ�����ӷ���ʽ �� 4Al + 3O2����1�֣�
4Al + 3O2����1�֣� 4Al + 3O2����
4Al + 3O2����

 �Ķ��쳵ϵ�д�
�Ķ��쳵ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ������ ���ͣ�ʵ����
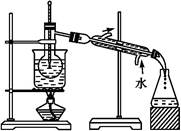
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
| A����ȥFe���л��е�I2������ʹI2���� |
| B����ȥNaCl�����л��е�MgCl2������KOH��Һ����ˣ���Һ�����ᾧ |
| C����ȥ̼�����л��е�̼�����ƣ��������������������Һ�������ᾧ |
| D����ȥ������þ�л��е��������ƣ�����ˮ�н���ɽ�״���������Ȼ�þ��Һ��������ˮ����ϴ�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ������
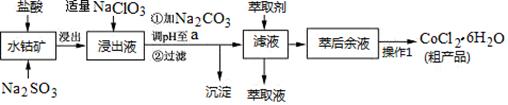
| ������ | Fe(OH)3 | Fe(OH)2 | Co(OH)2 | Al(OH)3 | Mn(OH)2 |
| ��ʼ���� | 2.7 | 7.6 | 7.6 | 4.0 | 7.7 |
| ��ȫ���� | 3.7 | 9.6 | 9.2 | 5.2 | 9.8 |
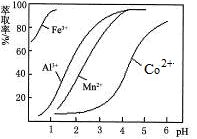
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
 | 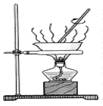 | 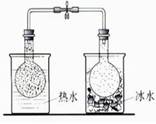 | 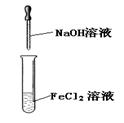 |
| �þƾ���ȡ��ˮ�е��� | ������ͭ��Һֱ�����ɵõ����� | ˵��2NO2(g)  N2O4��g�� ��H<0 N2O4��g�� ��H<0 | ʵ�����Ʊ�Fe(OH)2 |
| A | B | C | D |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
| ѡ�� | ʵ���������ʵ | ʵ��Ŀ�Ļ���� |
| A | ȡ������Һ���Թ��У�������HNO3�ữ��BaCl2��Һ��������ɫ���� | ˵����Һ��һ������SO42�� |
| B | �ֱ�����֧�Թ��м�����������Ũ�ȵĹ���������Һ����������һ֧�Թ��м�������MnO2 | �о������Թ�������ֽ����ʵ�Ӱ�� |
| C | ��NaHCO3��HCl������Һ��μ� | ���Լ�����������Һ |
| D | C2H5Br��AgNO3��Һ��ϼ��� | ����C2H5Br�е���Ԫ�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ�ʵ����
| ����ʽ | ��� | �ȷֽ��¶� | �۵� | ˮ���ԣ�20�棩 |
| CO(NH2)2��H2O2 | ��ɫ���� | 45�� | 75��85�� | 500g��L��1 |
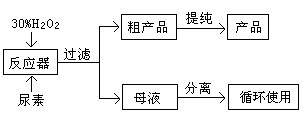


�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ������
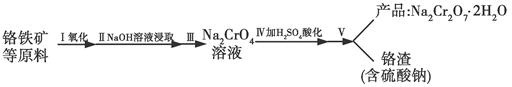
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
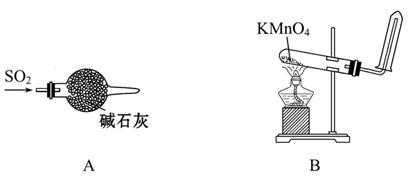
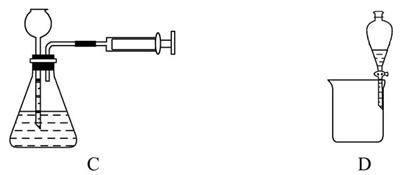
| A������SO2 |
| B��ʵ������ȡ���ռ�O2 |
| C��װ�������Եļ�� |
| D�������Ҵ�������Ļ��Һ |
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com