
| A. | 该元素位于元素周期表第三周期表ⅢB族 | |
| B. | 该元素位于s区 | |
| C. | 该元素为金属元素 | |
| D. | 该元素原子M能层共有8个电子 |
分析 若某基态原子的外围电子排布式为3d14s2,应为Sc元素,其核外有21个电子,位于周期表第四周期、第ⅢB族,以此解答该题.
解答 解:若某基态原子的外围电子排布式为3d14s2,应为Sc元素,其核外有21个电子,根据核外电子排布规律,该元素基态原子的电子排布式为1s22s22p63s23p63d14s2.
A.该原子外围电子排布式为3d14s2,位于周期表第四周期、第ⅢB族,故A错误;
B.该原子外围电子排布式为3d14s2,位于周期表第四周期、第ⅢB族,属于d区,故B错误;
C.为过渡金属元素,故C正确;
D.由电子排布式可知M层有9个电子,故D错误.
故选C.
点评 本题考查原子核外电子排布,题目难度不大,本题注意元素价层电子排布特点以及与在周期表位置的关系,熟练掌握元素周期表的结构.


科目:高中化学 来源: 题型:选择题
| A. | 1.2×10-5 mol•L-1 | B. | 2.4×10-4 mol•L-1 | ||
| C. | 3.6×10-4 mol•L-1 | D. | 4.8×10-4 mol•L-1 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | X与Y不可能位于同一周期 | |
| B. | X与Y不可能形成原子个数比为1:1型离子化合物 | |
| C. | X离子与Y离子的电子层结构可以相同 | |
| D. | X与Y形成的共价化合物中,各原子最外层一定满足8电子的稳定结构 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
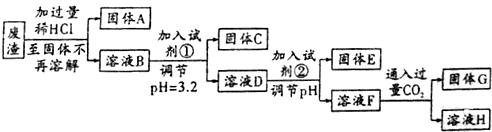
| 离子 | 以氢氧化物形式完全沉淀时所需pH | 氢氧化物沉淀完全溶解时所需pH |
| Fe3+ | 3.2 | |
| A13+ | 5.3 | 11.9 |
| Mg2+ | 12.3 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ③④ | B. | ③④⑥ | C. | ④⑤ | D. | ④⑥ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | SiO2晶体结构中,每个Si原子与2个O原子直接相连 | |
| B. | 通常状况下,60gSiO2晶体中含有的分子数为NA(NA表示阿伏加德罗常数) | |
| C. | 12g金刚石含4molC-C键 | |
| D. | 金刚石网状结构中,由共价键形成的碳原子环中,最小的环上有6个碳原子 |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | 辛烯和3-甲基-1-丁烯 | B. | 苯和乙炔 | ||
| C. | 2-甲基-3-乙基-1-戊烯和环丙烷 | D. | 软脂酸和硬脂酸 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
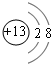 、
、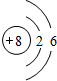 .
.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 金属的用途 | 对应的金属物理性质 |
| 金可制成比纸还薄的金箔 | ③ |
| 用铁、铝等做炊具 | ② |
| 用铜制作印刷电路 | ① |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com