
| A.稳定性:NH3<PH3<AsH3 | B.离子半径:阴离子>阳离子 |
| C.熔沸点:离子化合物>共价化合物 | D.酸性:H2SO4>H3PO4>H2SiO3 |
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源:不详 题型:单选题
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
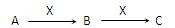
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
A.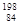 Po和 Po和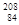 Po互为同位素 Po互为同位素 |
B.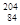 Po和 Po和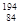 Po中子数差为20 Po中子数差为20 |
| C.α-Po和β-Po互为同素异形体 |
D.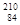 Po和 Po和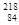 Po的核外电子总数相同,但不是同一种核素 Po的核外电子总数相同,但不是同一种核素 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
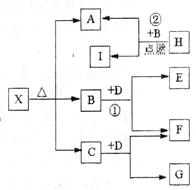

查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
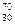 Zn撞入一个
Zn撞入一个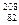 Pb的原子核,并立即释放一个中子而产生的一种新元素的原子。该元素的原子序数是( )
Pb的原子核,并立即释放一个中子而产生的一种新元素的原子。该元素的原子序数是( )| A.111 | B.112 | C.113 | D.114 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com