
| A. | 锗是一种金属性很强的元素 | B. | 锗酸(H4GeO4)是难溶于水的强酸 | ||
| C. | 锗化氢(GeH4)稳定性很强 | D. | 锗的单质具有半导体的性能 |
分析 处于金属区与非金属区的交界线上的元素常用于做半导体材料,锗和硅处于同一主族,根据同主族元素的金属性、非金属性的递变规律比较最高价含氧酸的酸性,结合元素周期律知识进行解答.
解答 解:A.锗处于金属区与非金属区的交界线上,元素金属性和非金属性都较弱,反应中既不易得电子,也不易失去电子,故A错误;
B.锗和硅处于同一主族,主族元素的非金属性从上到下逐渐减弱,则硅的非金属性大于锗,非金属性越强,对应的最高价氧化物的水化物的酸性越强,所以酸性比硅酸弱,为弱酸.碳酸溶液水,硅酸不溶于水,推知锗酸(H4GeO4)应难溶于水,故B错误;
C.锗处于金属区与非金属区的交界线上,元素金属性和非金属性都较弱,锗化氢(GeH4)稳定性很弱,故C错误;
D.锗处于金属区与非金属区的交界线上,既有金属性又有非金属性,常用于做半导体材料,故D正确;
故选D.
点评 本题考查了元素周期表结构及其应用,题目难度不大,明确元素周期律的内容为解答关键,注意熟练掌握原子结构与元素周期表、元素周期律的关系,试题培养了学生的分析能力及灵活应用能力.


科目:高中化学 来源: 题型:实验题
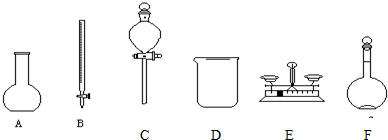
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 浓硫酸的装运包装箱应贴上如图所示标志  | |
| B. | 少量金属金属钠保存在CCl4中 | |
| C. | 镁带着火应用干粉灭火器灭火,不能用泡沫灭火器灭火 | |
| D. | 用25ml酸式滴定管量取20.00ml0.01 mol/L的Na2CO3溶液 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 碳酸锶难溶于水 | B. | 氢氧化锶的碱性比氢氧化钙弱 | ||
| C. | 单质锶跟冷水不反应 | D. | 锶是第四周期元素 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题

| A. | 可与NaOH溶液反应 | B. | 可发生酯化反应 | ||
| C. | 可使酸性KMnO4溶液褪色 | D. | 可在碱性条件下水解 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
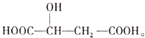 下列说法不正确的是( )
下列说法不正确的是( )| A. | 苹果酸在一定条件下能与乙醇发生反应 | |
| B. | 苹果酸在一定条件下能发生催化氧化反应 | |
| C. | 苹果酸在一定条件下能与乙酸发生反应 | |
| D. | 1mol苹果酸与Na2CO3溶液反应最多消耗3mol Na2CO3 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 氯化镁溶液中加氨水:Mg2++2NH3•H2O=Mg(OH)2↓+2NH4+ | |
| B. | 钠与水反应:Na+2H2O=Na++2OH-+H2↑ | |
| C. | 稀硫酸与氢氧化钡溶液混合:H++SO42-+Ba2++OH-=BaSO4↓+H2O | |
| D. | 碳酸钙溶于醋酸溶液:CaCO3+2H+=Ca2++CO2↑+H2O |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
| 实验步骤与实验现象 | 实验结论 |
| Ⅰ.观察溶液:无色透明 | ①原溶液中一定不含的离子是Cu2+、MnO4-、Fe2+ |
| Ⅱ.取适量该溶液,加入过量的硝酸,有气体生成,并得到无色溶液 | ②原溶液中一定不含的离子是Mg2+、Ag+、Ba2+、Al3+、I-、SiO32-,一定含有的离子是CO32-、K+ |
| Ⅲ.在Ⅱ所得溶液中再加入过量的碳酸氢铵溶液,有气体生成,同时析出白色沉淀A | ③原溶液中还一定含有的离子是AlO2-,生成沉淀A的离子方程式为Al3++3HCO3-=Al(OH)3↓+3CO2↑ |
| Ⅳ.在Ⅲ所得溶液中再逐滴加入氢氧化钡溶液至过量,加热也有气体生成,同时析出白色沉淀B | ④白色沉淀B中一定含有BaCO3,可能含有BaSO4 |
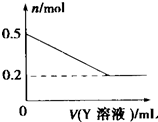 (3)该化学兴趣小组的同学为了进一步确定B的成分,取一定量经洗涤后的B与Y溶液反应,白色固体的物质的量与Y溶液体积之间的关系如图所示.
(3)该化学兴趣小组的同学为了进一步确定B的成分,取一定量经洗涤后的B与Y溶液反应,白色固体的物质的量与Y溶液体积之间的关系如图所示.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 1 mol甲苯含有6NA个C-H键 | |
| B. | 标准状况下,22.4 L氨水含有NA个NH3分子 | |
| C. | 18 g H2O含有10NA个质子 | |
| D. | 56 g铁片投入足量浓H2SO4中生成NA个SO2分子 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com